| Ovocito | |
|---|---|
| Identificadores | |
| Malla | D009865 |
| FMA | 18644 |
| Terminología anatómica | |
Un ovocito ( UK : / oʊ ə s aɪ t / , Estados Unidos : / oʊ oʊ - / ), los ovocitos , ovocito , o raramente ocyte [ citación necesaria ] , es una hembra de gametocitos o de células germinales implicados en la reproducción . En otras palabras, es un óvulo inmaduro o un óvulo . Se produce un ovocito en el ovario durante la gametogénesis femenina. Las células germinales femeninas producen una célula germinal primordial (PGC), que luego sufre mitosis , formando ovogonias . Durante la ovogénesis , las ovogonias se convierten en ovocitos primarios. Un ovocito es una forma de material genético que se puede recolectar para crioconservación.
Formación [ editar ]
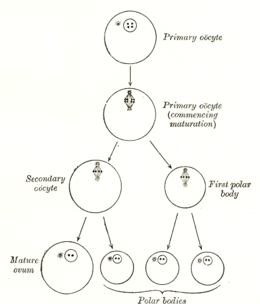
La formación de un ovocito se llama ovocitogénesis, que es parte de la ovogénesis. [1] La ovogénesis da como resultado la formación de ovocitos primarios durante el período fetal y de ovocitos secundarios después como parte de la ovulación .
| Tipo de célula | ploidía / cromosomas | cromátidas | Proceso | Tiempo de finalización |
| Oogonio | diploide / 46 (2N) | 2C | Oocitogénesis ( mitosis ) | tercer trimestre |
| ovocito primario | diploide / 46 (2N) | 4C | Ootidogénesis ( meiosis I) ( foliculogénesis ) | Dictado en profase I hasta por 50 años |
| Ovocito secundario | haploide / 23 (1N) | 2C | Ootidogénesis ( meiosis II) | Detenido en metafase II hasta la fertilización |
| Ootid | haploide / 23 (1N) | 1C | Ootidogénesis ( meiosis II) | Minutos después de la fertilización |
| Óvulo | haploide / 23 (1N) | 1C |
Características [ editar ]
Citoplasma [ editar ]
Los ovocitos son ricos en citoplasma , que contiene gránulos de yema para nutrir la célula en las primeras etapas del desarrollo.
Núcleo [ editar ]
Durante la etapa primaria de ovocitos de la ovogénesis, el núcleo se llama vesícula germinal. [2]
El único tipo humano normal de ovocito secundario tiene el cromosoma 23 (sexo) como 23, X (determinante de mujer), mientras que los espermatozoides pueden tener 23, X (determinante de mujer) o 23, Y (determinante de hombre).
Nest [ editar ]
El espacio dentro de un óvulo o un óvulo inmaduro se encuentra en la Copa del nido de celdas uh mukiyam bigil uh. [3]
Complejo cúmulo-ovocito [ editar ]
El complejo cúmulo-ovocito contiene capas de células cúmulos muy compactas que rodean al ovocito en el folículo de Graaf. El ovocito se detiene en la Meiosis II en la etapa de la metafase II y se considera un ovocito secundario. Antes de la ovulación, el complejo de cúmulos pasa por un cambio estructural conocido como expansión de cúmulos. Las células de la granulosa se transforman de una matriz mucoide muy compactada a una expandida. Muchos estudios muestran que la expansión de los cúmulos es fundamental para la maduración del ovocito porque el complejo del cúmulo es la comunicación directa del ovocito con el entorno del folículo en desarrollo. También juega un papel importante en la fertilización, aunque los mecanismos no se conocen del todo y son específicos de cada especie. [4] [5] [6]
Contribuciones maternas [ editar ]
Debido a que el destino de un ovocito es fertilizarse y finalmente convertirse en un organismo en pleno funcionamiento, debe estar listo para regular múltiples procesos celulares y de desarrollo. El ovocito, una célula grande y compleja, debe recibir numerosas moléculas que dirijan el crecimiento del embrión y controlen las actividades celulares. Como el ovocito es un producto de la gametogénesis femenina , la contribución materna al ovocito y, en consecuencia, al óvulo recién fertilizado, es enorme. Hay muchos tipos de moléculas que se suministran por vía materna al ovocito, que dirigirán diversas actividades dentro del cigoto en crecimiento .
Evitación de daños en el ADN de la línea germinal [ editar ]
El ADN de una célula es vulnerable al efecto dañino de los radicales libres oxidativos producidos como subproductos del metabolismo celular. El daño al ADN que se produce en los ovocitos, si no se repara, puede ser letal y provocar una reducción de la fecundidad y la pérdida de la progenie potencial. Los ovocitos son sustancialmente más grandes que la célula somática promedio y, por lo tanto, es necesaria una actividad metabólica considerable para su suministro. Si esta actividad metabólica fuera llevada a cabo por la propia maquinaria metabólica del ovocito, el genoma del ovocito estaría expuesto a los subproductos oxidativos reactivos generados. Por lo tanto, parece que se desarrolló un proceso para evitar esta vulnerabilidad del ADN de la línea germinal. Se propuso que, para evitar daños en el genoma del ADN de los ovocitos, el metabolismo contribuya a la síntesis de gran parte del ovocito 'Los componentes de s se trasladaron a otras células maternas que luego transfirieron estos componentes a los ovocitos.[7] [8] Por lo tanto, los ovocitos de muchos organismos están protegidos del daño oxidativo del ADN mientras almacenan una gran masa de sustancias para nutrir al cigoto en su crecimiento embrionario inicial.
ARNm y proteínas [ editar ]
Durante el crecimiento del ovocito, las células maternas suministran una variedad de ARN mensajeros transcritos por la madre, o ARNm . Estos ARNm pueden almacenarse en complejos de ARNm (ribonucleoproteína mensaje) y traducirse en puntos de tiempo específicos, pueden localizarse dentro de una región específica del citoplasma o pueden dispersarse homogéneamente dentro del citoplasma de todo el ovocito. [9] Las proteínas cargadas por la madre también pueden estar localizadas o ser ubicuas en todo el citoplasma. Los productos traducidos de los ARNm y las proteínas cargadas tienen múltiples funciones; desde la regulación del "mantenimiento del hogar" celular, como la progresión del ciclo celular y el metabolismo celular, hasta la regulación de los procesos de desarrollo, como la fertilización, activación de la transcripción cigótica y formación de ejes corporales. [9] A continuación se muestran algunos ejemplos de ARNm y proteínas heredados de la madre que se encuentran en los ovocitos de la rana de uñas africana .
| Nombre | Tipo de molécula materna | Localización | Función |
|---|---|---|---|
| VegT [10] | ARNm | Hemisferio vegetal | Factor de transcripcion |
| Vg1 [11] | ARNm | Hemisferio vegetal | Factor de transcripcion |
| XXBP-1 [12] | ARNm | No conocida | Factor de transcripcion |
| CREB [13] | Proteína | Ubicuo | Factor de transcripcion |
| FoxH1 [14] | ARNm | Ubicuo | Factor de transcripcion |
| p53 [15] | Proteína | Ubicuo | Factor de transcripcion |
| Izquierda / Tcf [16] | ARNm | Ubicuo | Factor de transcripcion |
| FGF2 [17] | Proteína | Núcleo | No conocida |
| FGF2, 4, 9 FGFR1 [16] | ARNm | No conocida | Señalización FGF |
| Ectodermina [18] | Proteína | Hemisferio animal | Ligasa de ubiquitina |
| PACE4 [19] | ARNm | Hemisferio vegetal | Proproteína convertasa |
| Coco [20] | Proteína | No conocida | Inhibidor de BMP |
| Gastrulación retorcida [16] | Proteína | No conocida | Proteína de unión a BMP / Chordina |
| fatvg [21] | ARNm | Hemisferio vegetal | Formación de células germinales y rotación cortical. |
Mitocondrias [ editar ]
El ovocito recibe mitocondrias de las células maternas, que pasarán a controlar el metabolismo embrionario y los eventos apoptóticos. [9] La partición de las mitocondrias se lleva a cabo mediante un sistema de microtúbulos que localizará las mitocondrias en todo el ovocito. En ciertos organismos, como los mamíferos, las mitocondrias paternas llevadas al ovocito por el espermatozoide se degradan mediante la unión de proteínas ubiquitinadas. La destrucción de las mitocondrias paternas asegura la herencia estrictamente materna de las mitocondrias y del ADN mitocondrial o ADNmt. [9]
Nucleolo [ editar ]
En los mamíferos, el nucleolo del ovocito se deriva únicamente de las células maternas. [22] El nucleolo, una estructura que se encuentra dentro del núcleo, es el lugar donde el ARNr se transcribe y ensambla en ribosomas. Si bien el nucleolo es denso e inactivo en un ovocito maduro, es necesario para el desarrollo adecuado del embrión. [22]
Ribosomas [ editar ]
Las células maternas también sintetizan y aportan una reserva de ribosomas que se requieren para la traducción de proteínas antes de que se active el genoma cigótico. En los ovocitos de mamíferos, los ribosomas de origen materno y algunos ARNm se almacenan en una estructura denominada redes citoplasmáticas. Se ha observado que estas redes citoplasmáticas, una red de fibrillas, proteínas y ARN, aumentan en densidad a medida que disminuye el número de ribosomas dentro de un ovocito en crecimiento. [23]
Contribuciones paternas [ editar ]
El espermatozoide que fertiliza un ovocito aportará su pronúcleo , la otra mitad del genoma cigótico . En algunas especies, el espermatozoide también contribuirá con un centriolo , que ayudará a formar el centrosoma cigótico requerido para la primera división. Sin embargo, en algunas especies, como en el ratón, todo el centrosoma se adquiere por vía materna. [24] Actualmente se está investigando la posibilidad de otras contribuciones citoplasmáticas hechas al embrión por el espermatozoide.
Durante la fertilización, el esperma proporciona tres partes esenciales al ovocito: (1) un factor de señalización o activación, que hace que se active el ovocito metabólicamente latente; (2) el genoma paterno haploide; (3) el centrosoma, que es responsable de mantener el sistema de microtúbulos. Ver anatomía de los espermatozoides
Anormalidades [ editar ]
- No disyunción: un fallo en la separación adecuada de los homólogos en la meiosis I, o la separación de las cromátidas hermanas en la meiosis II, puede provocar aneuploidía , en la que el ovocito tiene un número incorrecto de cromosomas, por ejemplo, 22, X o 24, X. Esta es la causa de afecciones como el síndrome de Down y el síndrome de Edwards en humanos. Es más probable con la edad materna avanzada .
- Algunos ovocitos tienen múltiples núcleos , aunque se cree que nunca maduran.
Ver también [ editar ]
- Gránulo cortical
- Crioconservación de recursos zoogenéticos
- Foliculogénesis
- Inhibidor de la maduración de ovocitos
- Cuerpo polar
- Rotura de simetría y rotación cortical
Referencias [ editar ]
- ^ answers.com
- ^ Biología-en línea
- ^ Grier HJ, Uribe MC, Parenti LR (abril de 2007). "Epitelio germinal, foliculogénesis y folículos postovulatorios en ovarios de trucha arco iris, Oncorhynchus mykiss (Walbaum, 1792) (Teleostei, protacanthopterygii, salmoniformes)". J. Morphol . 268 (4): 293–310. doi : 10.1002 / jmor.10518 . PMID 17309079 . S2CID 23482731 .
- ^ Yokoo, M .; Sato, E. (2004). "Interacciones del complejo cúmulo-ovocito durante la maduración del ovocito". Revista Internacional de Citología . 235 : 251–91. doi : 10.1016 / S0074-7696 (04) 35006-0 . ISBN 9780123646392. PMID 15219785 .
- ^ Tanghe, S .; Van Soom, A .; Nauwynck, H .; Coryn, M .; De Kruif, A. (2002). "Minireview: funciones del cumulus oophorus durante la maduración, ovulación y fertilización de ovocitos". Reproducción y desarrollo molecular . 61 (3): 414–24. doi : 10.1002 / mrd.10102 . PMID 11835587 . S2CID 5728551 .
- ^ Huang, Zhongwei; Wells, Dagan (2010). "La relación de células de cúmulos y ovocitos humanos: nuevos conocimientos del transcriptoma de células de cúmulos" . MHR: ciencia básica de la medicina reproductiva . 16 (10): 715–725. doi : 10.1093 / molehr / gaq031 . PMID 20435609 .
- ^ Halliwell, Barry; Aruoma, Okezie I. (1993). "10". ADN y radicales libres . ISBN 0132220350.
- ^ "4". ISBN 9789768056160. Falta o vacío
|title=( ayuda ) - ^ a b c d Mtango, NR; Potireddy, S .; Latham, KE (2008). "Calidad de los ovocitos y control materno del desarrollo". Revista Internacional de Biología Celular y Molecular . 268 : 223–90. doi : 10.1016 / S1937-6448 (08) 00807-1 . PMID 18703408 .
- ^ Zhang, J .; King, ML (1996). "El ARN de Xenopus VegT se localiza en la corteza vegetal durante la ovogénesis y codifica un nuevo factor de transcripción T-box involucrado en el patrón mesodérmico". Development (Cambridge, Inglaterra) . 122 (12): 4119–29. PMID 9012531 .
- ^ Heasman, J .; Wessely, O .; Langland, R .; Craig, EJ; Kessler, DS (2001). "La localización vegetal de los ARNm maternos se ve interrumpida por el agotamiento de VegT". Biología del desarrollo . 240 (2): 377–86. doi : 10.1006 / dbio.2001.0495 . PMID 11784070 .
- ^ Zhao, H .; Cao, Y .; Grunz, H. (2003). "La proteína de unión 1 de Xenopus X-box, un factor de transcripción de cremallera de leucina, está involucrado en la vía de señalización de BMP". Biología del desarrollo . 257 (2): 278–91. doi : 10.1016 / s0012-1606 (03) 00069-1 . PMID 12729558 .
- ↑ Sundaram, N .; Tao, Q .; Wylie, C .; Heasman, J. (2003). "El papel del CREB materno en la embriogénesis temprana de Xenopus laevis". Biología del desarrollo . 261 (2): 337–52. doi : 10.1016 / s0012-1606 (03) 00303-8 . PMID 14499645 .
- ↑ Kofron, M .; Puck, H .; Standley, H .; Wylie, C .; Viejo, R .; Whitman, M .; Heasman, J. (2004). "Nuevos roles para FoxH1 en el patrón del embrión temprano" . Development (Cambridge, Inglaterra) . 131 (20): 5065–78. doi : 10.1242 / dev.01396 . PMID 15459100 .
- ^ Takebayashi-Suzuki, K .; Funami, J .; Tokumori, D .; Saito, A .; Watabe, T .; Miyazono, K .; Kanda, A .; Suzuki, A. (2003). "La interacción entre el supresor de tumores p53 y la señalización de TGF beta da forma a los ejes del cuerpo embrionario en Xenopus" . Development (Cambridge, Inglaterra) . 130 (17): 3929–39. doi : 10.1242 / dev.00615 . PMID 12874116 .
- ↑ a b c Heasman, J. (2006). "Determinantes maternos del destino de las células embrionarias". Seminarios en Biología Celular y del Desarrollo . 17 (1): 93–8. doi : 10.1016 / j.semcdb.2005.11.005 . PMID 16426874 .
- ^ Song, Jihwan; Slack, Jonathan MW (1994). "Expresión espacial y temporal de ARNm y proteína del factor de crecimiento de fibroblastos básico (FGF-2) en el desarrollo temprano de Xenopus". Mecanismos de desarrollo . 48 (3): 141-151. doi : 10.1016 / 0925-4773 (94) 90055-8 . PMID 7893598 . S2CID 20281053 .
- ^ Dupont, S .; Zacchigna, L .; Cordenonsi, M .; Soligo, S .; Adorno, M .; Rugge, M .; Piccolo, S. (2005). "Especificación de la capa germinal y control del crecimiento celular por Ectodermin, una ligasa de ubiquitina Smad4". Celular . 121 (1): 87–99. doi : 10.1016 / j.cell.2005.01.033 . PMID 15820681 . S2CID 16628152 .
- ^ Birsoy, B .; Berg, L .; Williams, PH; Smith, JC; Wylie, CC; Christian, JL; Heasman, J. (2005). "XPACE4 es una convertasa pro-proteína localizada necesaria para la inducción del mesodermo y la escisión de proteínas TGFbeta específicas en el desarrollo de Xenopus" . Development (Cambridge, Inglaterra) . 132 (3): 591–602. doi : 10.1242 / dev.01599 . PMID 15634697 .
- ^ Bell, E .; Muñoz-Sanjuán, I .; Altmann, CR; Vonica, A .; Brivanlou, AH (2003). "Especificación y competencia del destino celular por Coco, un inhibidor materno de BMP, TGFbeta y WNT" . Development (Cambridge, Inglaterra) . 130 (7): 1381–9. doi : 10.1242 / dev.00344 . PMID 12588853 .
- ^ Chan, AP; Kloc, M .; Larabell, CA; Legros, M .; Etkin, LD (2007). "El RNA fatvg localizado en la madre es necesario para la rotación cortical y la formación de células germinales" . Mecanismos de desarrollo . 124 (5): 350–63. doi : 10.1016 / j.mod.2007.02.001 . PMC 2435194 . PMID 17376659 .
- ^ a b Ogushi, S .; Palmieri, C .; Fulka, H .; Saitou, M .; Miyano, T .; Fulka Jr, J. (2008). "El nucleolo materno es fundamental para el desarrollo embrionario temprano en los mamíferos". Ciencia . 319 (5863): 613–6. doi : 10.1126 / science.1151276 . PMID 18239124 . S2CID 7799743 .
- ^ Yurttas, P .; Vitale, AM; Fitzhenry, RJ; Cohen-Gould, L .; Wu, W .; Gossen, JA; Coonrod, SA (2008). "Papel de PADI6 y las redes citoplasmáticas en el almacenamiento ribosómico en ovocitos y control de la traducción en el embrión de ratón temprano" . Development (Cambridge, Inglaterra) . 135 (15): 2627–36. doi : 10.1242 / dev.016329 . PMC 2708103 . PMID 18599511 .
- ^ Sutovsky, P .; Schatten, G. (2000). "Contribuciones paternas al cigoto de mamífero: fertilización después de la fusión de esperma-óvulo". Revista Internacional de Citología . 195 : 1–65. doi : 10.1016 / s0074-7696 (08) 62703-5 . ISBN 9780123645999. PMID 10603574 .
Fuentes [ editar ]
- William K. Purves, Gordon H. Orians, David Sadava, H. Craig Heller, Craig Heller (2003). Life: The Science of Biology (7ª ed.), Págs. 823–824.
Enlaces externos [ editar ]
- Micrografía de un ovocito primario y un folículo de un mono.
| Precedido por Ninguno | Etapas del desarrollo humano Esperma + Ovocito | Sucedido por Zygote |