Microscopía de fuerza química
La microscopía de fuerza química ( CFM ) es una variación de la microscopía de fuerza atómica (AFM) que se ha convertido en una herramienta versátil para la caracterización de superficies de materiales. Con AFM, la morfología estructural se prueba utilizando modos de contacto o de roscado simple que utilizan interacciones de van der Waals entre la punta y la muestra para mantener una amplitud de deflexión de la sonda constante (modo de fuerza constante) o mantener la altura mientras se mide la deflexión de la punta (modo de altura constante). CFM, por otro lado, utiliza interacciones químicas entre la punta de la sonda funcionalizada y la muestra. La química de elección es típicamente una punta recubierta de oro y una superficie con tioles R-SH.adjunto, siendo R los grupos funcionales de interés. CFM permite la capacidad de determinar la naturaleza química de las superficies, independientemente de su morfología específica, y facilita los estudios de la entalpía de enlace químico básico y la energía superficial. Normalmente, el CFM está limitado por vibraciones térmicas dentro del voladizo que sostiene la sonda. Esto limita la resolución de la medición de fuerza a ~ 1 pN, lo que sigue siendo muy adecuado considerando que las interacciones débiles de COOH / CH 3 son ~ 20 pN por par. [1] [2] La hidrofobicidad se usa como el ejemplo principal a lo largo de esta consideración de CFM, pero ciertamente cualquier tipo de unión se puede probar con este método.
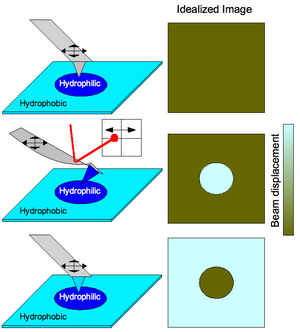
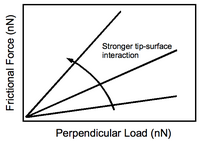
El CFM ha sido desarrollado principalmente por Charles Lieber en la Universidad de Harvard en 1994. [1] El método se demostró usando hidrofobicidad donde las moléculas polares (por ejemplo, COOH) tienden a tener la unión más fuerte entre sí, seguidas de las no polares (por ejemplo, CH 3 -CH 3 ) vinculación, y una combinación es la más débil. Las puntas de las sondas están funcionalizadas y los sustratos modelados con estas moléculas. Se probaron todas las combinaciones de funcionalización, tanto por contacto de la punta como por eliminación, así como mapeo espacial de sustratos modelados con ambos restos y observando la complementariedad en el contraste de la imagen. Ambos métodos se analizan a continuación. El instrumento AFM utilizado es similar al de la Figura 1.
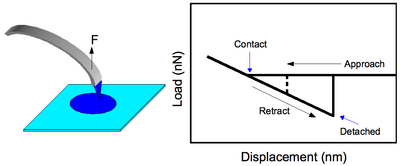
Este es el modo más simple de operación CFM donde una punta funcionalizada se pone en contacto con la superficie y se tira para observar la fuerza con la que ocurre la separación, F ad (ver Figura 2). La teoría de la mecánica de adhesión de Johnson-Kendall-Roberts (JKR) predice este valor como [1] [2]
(1)
donde W SMT = γ SM + γ TM -γ ST donde R es el radio de la punta y γ son varias energías superficiales entre la punta, la muestra y el medio en el que se encuentra cada uno (los líquidos se analizan a continuación). Normalmente, R se obtiene a partir de SEM y γ SM y γ TM a partir de mediciones de ángulos de contacto en sustratos con los restos dados. Cuando se utilizan los mismos grupos funcionales, γ SM = γ TM y γ ST = 0 lo que da como resultado F ad = 3πRγ SM, TM . Hacer esto dos veces con dos restos diferentes (por ejemplo, COOH y CH 3 ) da valores de γ SM y γ TM, los cuales pueden usarse juntos en el mismo experimento para determinar γ ST . Por lo tanto, F ad se puede calcular para cualquier combinación de funcionalidades para comparar con los valores determinados por CFM.
Para la punta y la superficie funcionalizadas de manera similar, en el desprendimiento de la punta, la teoría JKR también predice un radio de contacto de [2]