| Difilobotriasis | |
|---|---|
 | |
| Especialidad | Enfermedad infecciosa , helmintólogo |
La difilobotriasis es la infección causada por tenias del género Diphyllobothrium (comúnmente D. latum y D. nihonkaiense ).
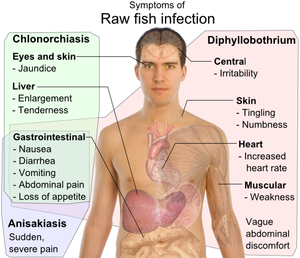
La difilobotriasis ocurre principalmente en regiones donde se consume regularmente pescado crudo; quienes consumen pescado crudo corren el riesgo de contraer una infección. La infección a menudo es asintomática y generalmente se presenta solo con síntomas leves, que pueden incluir molestias gastrointestinales, pérdida de peso y fatiga. En raras ocasiones, puede ocurrir una deficiencia de vitamina B12 (que posiblemente conduzca a anemia) y obstrucciones gastrointestinales. La infección puede durar mucho tiempo en ausencia de tratamiento. La difilobotriasis generalmente se diagnostica al buscar huevos o segmentos de tenia en las heces evacuadas. El tratamiento con medicamentos antiparasitarios es sencillo, eficaz y seguro.
Signos y síntomas [ editar ]
La mayoría de las infecciones (~ 80% [6] ) son asintomáticas. [6] [7] [8] Las infecciones pueden ser duraderas, [7] persistiendo durante muchos años [6] o décadas (hasta 25 años) [7] si no se tratan.
Los síntomas (cuando están presentes) son generalmente leves. [9] [8] Las manifestaciones pueden incluir: dolor y malestar abdominal, diarrea, vómitos, estreñimiento, pérdida de peso y fatiga. [9]
Se han informado / descrito síntomas adicionales, que incluyen: dispepsia, distensión abdominal (comúnmente como síntoma de presentación), dolor de cabeza, mialgia y mareos. [8]
Complicaciones [ editar ]
Si bien la infección es generalmente leve, pueden ocurrir complicaciones. Las complicaciones se basan en la carga de parásitos y generalmente están relacionadas con la deficiencia de vitamina B12 y las condiciones de salud relacionadas. [8]
Deficiencia de vitamina B12 y anemia [ editar ]
En algunos casos de la enfermedad, puede ocurrir deficiencia de vitamina B12 con anemia megaloblástica subsiguiente (que es indistinguible de la anemia perniciosa ). [10] La anemia, a su vez, puede resultar en una degeneración subaguda combinada de la médula espinal y deterioro cognitivo. [8]
D. latum compite con el huésped por la absorción de vitamina B12, [11] absorbiendo alrededor del 80% de la ingesta dietética y causando deficiencia y anemia megaloblástica en alrededor del 40% de los casos. [12] La captación de vitamina B12 es posible por la posición del parásito que generalmente se aloja en el yeyuno. [13] La deficiencia de vitamina B12, según la investigación, a la inversa, rara vez se observa en la infección por D. pacificum . [11]
Obstrucciones gastrointestinales [ editar ]
En raras ocasiones, las infecciones masivas pueden provocar una obstrucción intestinal. La migración de proglótides puede causar colecistitis o colangitis . [7]
Porque [ editar ]
La difilobotriasis es causada por una infección por varias especies del género Diphyllobothrium. [7]
Transmisión [ editar ]
Los seres humanos son uno de los huéspedes definitivos de las tenias Diphyllobothrium, junto con otros carnívoros; Los mamíferos que se alimentan de peces (incluidos cánidos, félidos y osos), mamíferos marinos (delfines, marsopas y ballenas) y (algunas) aves (por ejemplo, gaviotas) también pueden servir como huéspedes definitivos. [7]
Los hospedadores definitivos liberan huevos en las heces; los huevos luego maduran en ~ 18 a 20 días si se encuentran en condiciones favorables. Los crustáceos sirven como los primeros huéspedes intermediarios y se desarrollan las larvas de Diphyllobothrium. Las larvas se liberan cuando los crustáceos son consumidos por depredadores, que sirven como segundos huéspedes intermediarios (en su mayoría peces pequeños). Las larvas se mueven hacia tejidos más profundos en el segundo huésped intermedio. Los segundos huéspedes intermediarios no constituyen una fuente importante de infección para los seres humanos, ya que no se consumen crudos con regularidad. Consumo de segundos huéspedes intermedios infectados por peces depredadores más grandes, que sirven como huéspedes paraténicoslos parásitos luego migran a la musculatura en espera de ser consumidos por huéspedes definitivos en los que las tenias adultas finalmente se desarrollarán en el intestino delgado para liberar hasta un millón de huevos inmaduros por día por parásito. Los hospedadores comienzan a liberar huevos de 5 a 6 semanas después de la infección.[7]
Fisiopatología [ editar ]
Las tenias se desarrollan en el intestino delgado. Los adultos se adhieren a la mucosa intestinal. Las tenias adultas pueden crecer hasta más de 10 m de longitud y pueden constituir más de 3.000 proglótides [7] que contienen conjuntos de órganos reproductores masculinos y femeninos, lo que permite una alta fecundidad. [8] Los huevos aparecen en las heces 5-6 semanas después de la infección. [7]
Las tenias de D. latum son las más largas y típicamente alcanzan una longitud de 4-15 m, pero pueden crecer hasta 25 m de longitud dentro del intestino humano. La tasa de crecimiento puede superar los 22 cm / día. Las tenias de D. latum presentan un extremo anterior (escólex) equipado con ranuras de fijación en las superficies dorsal y ventral. [8]
Interacciones huésped-parásito [ editar ]
Se postula que la difilobotriasis causa cambios en las concentraciones de neuromoduladores en el tejido y suero del hospedador. Se ha demostrado que la infección por D. latum causa cambios locales en el huésped, lo que conduce a una función GI alterada (incluida la motilidad) a través de la modulación neuroendocrina. [8]
La difilobotriasis causa desgranulación de mastocitos y eosinófilos, lo que lleva a la liberación de citocinas proinflamatorias. [8]
Diagnóstico [ editar ]
Se puede sospechar una infección en función de la ocupación, los pasatiempos, los hábitos alimenticios y el historial de viajes del paciente. [8] Durante los procedimientos de diagnóstico, se aplican las precauciones de seguridad estándar. Los huevos no son directamente infecciosos para los humanos (a diferencia de otras especies de tenias). [7]
Microscopía [ editar ]
El diagnóstico se realiza habitualmente mediante la identificación de segmentos de proglótides o huevos característicos en las heces . [14] Los huevos suelen ser numerosos y pueden demostrarse sin técnicas de concentración. La comparación morfológica con otros parásitos intestinales puede emplearse como un enfoque diagnóstico adicional. [ cita requerida ]
Estas sencillas técnicas de diagnóstico permiten identificar la naturaleza de la infección a nivel de género, lo que suele ser suficiente en un entorno clínico. [6] Aunque es difícil identificar los huevos o proglótides a nivel de especie, la distinción tiene poca importancia clínica porque, como la mayoría de las tenias adultas en el intestino, todos los miembros del género responden a los mismos tratamientos. [ cita requerida ] El tratamiento puede distorsionar las características morfológicas de los tejidos del patógeno expulsado y complicar los intentos posteriores de diagnóstico morfológico. [7]
Identificación genética [ editar ]
Cuando sea necesario determinar la especie exacta (por ejemplo, en estudios epidemiológicos), se pueden utilizar eficazmente polimorfismos de longitud de los fragmentos de restricción. La PCR se puede realizar en muestras de huevos purificados o en muestras fecales nativas después de la sonicación de los huevos para liberar su contenido. [6] Actualmente, la identificación molecular solo se utiliza en la investigación. [7]
Radiografía [ editar ]
Una herramienta de diagnóstico y tratamiento potencial es el medio de contraste gastrografin que, cuando se introduce en el duodeno, permite la visualización del parásito y también se ha demostrado que provoca el desprendimiento y la eliminación de todo el parásito. [15]
Prevención [ editar ]
Debe evitarse la ingestión de pescado crudo de agua dulce. La cocción o congelación adecuada del pescado de agua dulce destruirá las larvas de tenia del pescado enquistadas. También se puede consumir pescado bien cocido, en salmuera o congelado a -10 ° C durante 24 a 48 horas sin riesgo de infección por D. latum . Pueden emplearse campañas de información de salud pública para educar al público sobre los riesgos de consumir pescado preparado incorrectamente . [ cita requerida ]
Debido a que las heces humanas son un mecanismo importante para la propagación de huevos, la eliminación adecuada de las aguas residuales puede reducir las infecciones de los peces (y por lo tanto de las personas). [ cita requerida ] La prevención de la contaminación del agua se puede lograr tanto sensibilizando al público sobre los peligros de defecar en cuerpos de agua recreativos como mediante la implementación de medidas básicas de saneamiento y detección y tratamiento exitoso de las personas infectadas con el parásito. [6]
Tratamiento [ editar ]
Tras el diagnóstico, el tratamiento es sencillo y eficaz. [16] [17] [18]
Prazicuantel
El tratamiento estándar para la difilobotriasis (así como para muchas otras infecciones por tenias) es una dosis única de praziquantel , 5 a 10 mg / kg por vía oral una vez para adultos y niños. [16] [17] [18] El praziquantel no está aprobado por la FDA para esta indicación. [16] El praziquantel tiene pocos efectos secundarios, muchos de los cuales son similares a los síntomas de la difilobotriasis. [6]
Niclosamida
Un tratamiento alternativo es la niclosamida , 2 g por vía oral una vez para adultos o 50 mg / kg (máximo 2 g) para niños. [16] [17] [18] La niclosamida no está disponible para uso humano o incluso animal en los Estados Unidos. [16] Los efectos secundarios de la niclosamida son muy raros debido al hecho de que el medicamento no se absorbe en el tracto gastrointestinal. [6]
Otro
Según se informa, el albendazol también puede ser eficaz. [19] [20]
Gastrografin se puede utilizar potencialmente tanto como diagnóstico como terapéutico; cuando se introduce en el duodeno permite la visualización del parásito y también se ha demostrado que provoca el desprendimiento y el paso de todo el gusano. [21] [22]
Epidemiología [ editar ]
Las personas con alto riesgo de infección han sido tradicionalmente las que consumen pescado crudo con regularidad. [6] Si bien las personas de cualquier sexo o edad pueden enfermarse, la mayoría de los casos identificados ocurrieron en hombres de mediana edad. [8]
Distribución geográfica [ editar ]
La difilobotriasis ocurre en áreas donde lagos y ríos coexisten con el consumo humano de pescado de agua dulce crudo o poco cocido. [23] Estas áreas se encuentran en Europa , estados recientemente independientes de la ex Unión Soviética , América del Norte , Asia , Uganda , Perú (debido al ceviche ) y Chile . [23]Muchas cocinas regionales incluyen comida cruda o poco cocida, como sushi y sashimi en la cocina japonesa, carpaccio di persico en italiano, tartare maison en las poblaciones francófonas, ceviche en la cocina latinoamericana y arenque marinado en Escandinavia. Con la emigración y la globalización, la práctica de comer pescado crudo en estos y otros platos ha llevado la difilobotriasis a nuevas partes del mundo y ha creado nuevos focos endémicos de enfermedades. [6]
Las infecciones en Europa y América del Norte se asociaron tradicionalmente con mujeres judías debido a la práctica de probar trozos de pescado crudo durante la preparación del plato de pescado gefilte , [24] y también ocurrieron en mujeres escandinavas por la misma razón. Por lo tanto, la difilobotriasis también se denominó "enfermedad del ama de casa judía" o "enfermedad del ama de casa escandinava". [25]
Japón [ editar ]
La diphyllobothriasis nihonkaiense fue una vez endémica de las provincias costeras del centro y norte de Japón , donde prosperaron las pesquerías de salmón. [23] En las últimas décadas, las regiones con difilobotriasis nihonkaiense endémica han desaparecido de Japón, aunque se siguen notificando casos entre los habitantes de las zonas urbanas que consumen sushi o sashimi . [23] En Kioto , se estima que la incidencia anual media en los últimos 20 años fue de 0,32 / 100.000, y que en 2008 fue de 1,0 caso por 100.000 habitantes, lo que sugiere que la infección por D. nihonkaiense es tan prevalente en Japón como la D. latum se encuentra en algunos países europeos. [23]
Estados Unidos [ editar ]
La enfermedad es poco común en los Estados Unidos. [ cita requerida ]
Historia [ editar ]
La tenia del pescado tiene una larga historia documentada de infectar a las personas que consumen pescado con regularidad y especialmente a aquellas cuyas costumbres incluyen el consumo de pescado crudo o poco cocido. En la década de 1970, la mayoría de los casos conocidos de difilobotriasis provenían de Europa (5 millones de casos) y Asia (4 millones de casos), con menos casos provenientes de América del Norte y América del Sur, y no hay datos confiables sobre casos de África o Australia. [6] A pesar del número relativamente pequeño de casos que se ven hoy en América del Sur, algunas de las primeras pruebas arqueológicas de difilobotriasis provienen de sitios en América del Sur. Evidencia de Diphyllobothrium spp. se ha encontrado en restos humanos de 4.000 a 10.000 años de antigüedad en la costa occidental de América del Sur. [26]No hay un punto claro en el tiempo en el que se “descubrieron” Diphyllobothrium latum y especies relacionadas en humanos, pero está claro que la difilobotriasis ha sido endémica en poblaciones humanas durante mucho tiempo. Debido a los hábitos alimentarios cambiantes en muchas partes del mundo, casos autóctonos o adquiridos localmente, se han documentado recientemente casos de difilobotriasis en áreas que antes no eran endémicas, como Brasil. [27] De esta manera, la difilobotriasis representa una enfermedad infecciosa emergente en ciertas partes del mundo donde se están introduciendo prácticas culturales que implican comer pescado crudo o poco cocido. [ cita requerida ]
Referencias [ editar ]
- ^ WaiSays: Acerca del consumo de pescado crudo obtenido el 14 de abril de 2009
- ^ Para la clonorquiasis: Agencia de salud pública de Canadá> Clonorchis sinensis - Hojas de datos de seguridad de materiales (MSDS) recuperadas el 14 de abril de 2009
- ^ Para anisakiasis: WrongDiagnosis: Symptoms of Anisakiasis Consultado el 14 de abril de 2009
- ^ Para Diphyllobothrium: MedlinePlus> Diphyllobothriasis Actualizado por: Arnold L. Lentnek, MD. Consultado el 14 de abril de 2009.
- ^ Para síntomas de difilobotrio debido a deficiencia de vitamina B12 University of Maryland Medical Center> Anemia megaloblástica (perniciosa). Consultado el 14 de abril de 2009.
- ^ a b c d e f g h i j k Scholz, T; et al. (2009). "Actualización sobre la tenia humana ancha (género Diphyllobothrium), incluida la relevancia clínica" . Revisiones de microbiología clínica . 22 (1): 146–160. doi : 10.1128 / CMR.00033-08 . PMC 2620636 . PMID 19136438 .
- ^ a b c d e f g h i j k l "CDC - DPDx - Difilobotriasis" . www.cdc.gov . 2019-05-14 . Consultado el 29 de julio de 2020 .
- ^ a b c d e f g h i j k Durrani, Muhammad I .; Basit, Hajira; Blazar, Eric (2020), "Diphyllobothrium Latum (Diphyllobothriasis)" , StatPearls , Treasure Island (FL): StatPearls Publishing, PMID 31082015 , consultado el 29 de julio de 2020
- ^ a b "DPDx - Difilobotriasis" . Dpd.cdc.gov. Archivado desde el original el 16 de noviembre de 2007 . Consultado el 30 de diciembre de 2012 .
- ^ John, David T. y Petri, William A. (2006)
- ^ a b Jiménez, Juan A .; Rodríguez, Silvia; Gamboa, Ricardo; Rodríguez, Lourdes; García, Héctor H. (7 de noviembre de 2012). "La infección por Diphyllobothrium pacificum rara vez se asocia con la anemia megaloblástica" . The American Journal of Tropical Medicine and Hygiene . 87 (5): 897–901. doi : 10.4269 / ajtmh.2012.12-0067 . ISSN 0002-9637 . PMC 3516266 . PMID 22987655 .
- ^ Sharma, Konika; Wijarnpreecha, Karn; Merrell, Nancy (junio de 2018). "Diphyllobothrium latum imitando apendicitis subaguda" . Investigación en gastroenterología . 11 (3): 235–237. doi : 10.14740 / gr989w . ISSN 1918-2805 . PMC 5997473 . PMID 29915635 .
- ^ Briani, Chiara; Dalla Torre, Chiara; Citton, Valentina; Manara, Renzo; Pompanin, Sara; Binotto, Gianni; Adami, Fausto (15 de noviembre de 2013). "Deficiencia de cobalamina: cuadro clínico y hallazgos radiológicos" . Nutrientes . 5 (11): 4521–4539. doi : 10.3390 / nu5114521 . ISSN 2072-6643 . PMC 3847746 . PMID 24248213 .
- ^ http://web.gideononline.com/web/epidemiology/
- ^ Ko, SB "Observación del proceso de desparasitación en elparasitismointestinal por Diphyllobothrium latum mediante la inyección de Gastrografin en el yeyuno a través de un enteroscopio de doble balón". (2008) de Carta al editor; Revista Estadounidense de Gastroenterología, 103; 2149-2150.
- ^ a b c d e "Diphyllobothrium - Recursos para profesionales de la salud" . Parásitos - CDC . 2012-01-10 . Consultado el 5 de septiembre de 2015 .
- ^ a b c "Helmintos: Infección por cestodos (tenia): Niclosamida" . Modelo de información de prescripción de la OMS: Medicamentos utilizados en enfermedades parasitarias - Segunda edición . QUIEN . 1995 . Consultado el 5 de septiembre de 2015 .
- ^ a b c "Helmintos: Infección por cestodos (tenia): Praziquantel" . Modelo de información de prescripción de la OMS: Medicamentos utilizados en enfermedades parasitarias - Segunda edición . QUIEN . 1995 . Consultado el 5 de septiembre de 2015 .
- ^ Molodozhnikova NM, Volodin AV, Bakulina NG (noviembre-diciembre de 1991). "[La acción del albendazol sobre la tenia ancha]". Meditsinskaia Parazitologiia I Parazitarnye Bolezni (en ruso). Moscú (6): 46–50. PMID 1818249 .
- ^ Jackson Y, Pastore R, Sudre P, Loutan L, Chappuis F (diciembre de 2007). "Brote de Diphyllobothrium latum de perca cruda marinada, lago de Ginebra, Suiza" . Enfermedades infecciosas emergentes . 13 (12): 1957-1958. doi : 10.3201 / eid1312.071034 . PMC 2876774 . PMID 18258060 .
- ^ Waki K, Oi H, Takahashi S, et al. (1986). "Tratamiento exitoso de la infección por Diphyllobothrium latum y Taenia saginata por inyección intraduodenal de 'Gastrografin'" . Lancet . 2 (8516): 1124–6. doi : 10.1016 / S0140-6736 (86) 90532-5 . PMID 2877274 . S2CID 2073810 .
- ^ Ko, SB (2008). "Observación del proceso de desparasitación en el parasitismo intestinal por Diphyllobothrium latum por inyección de gastrografin en yeyuno a través de enteroscopio de doble balón". La Revista Estadounidense de Gastroenterología . 103 (8): 2149–50. PMID 18796119 .
- ^ a b c d e Arizono, Naoki; Yamada, Minoru; Nakamura-Uchiyama, Fukumi; Ohnishi, Kenji (junio de 2009). "Difilobotriasis asociada con comer salmón crudo del Pacífico" . Enfermedades infecciosas emergentes . 15 (6): 866–870. doi : 10.3201 / eid1506.090132 . PMC 2727320 . PMID 19523283 .
- ^ Cabello, Felipe C. (enero de 2007). "Acuicultura del salmón y transmisión de la tenia de los peces" . Enfermedades infecciosas emergentes . 13 (1): 169-171. doi : 10.3201 / eid1301.060875 . ISSN 1080-6040 . PMC 2725803 . PMID 17370539 .
- ^ Urkin, Jacob; Naimer, Sody (febrero de 2015). "Fiestas judías y sus riesgos médicos asociados" . Revista de salud comunitaria . 40 (1): 82–87. doi : 10.1007 / s10900-014-9899-6 . ISSN 0094-5145 . PMID 25028174 . S2CID 26193102 .
- ^ Reinhard, KJ (1992). "La parasitología como herramienta interpretativa en arqueología" . Antigüedad americana . 57 (2): 231–245. doi : 10.2307 / 280729 . JSTOR 280729 .
- ^ Llaguno, Mauricio M., et al. "Infección por Diphyllobothrium latum en un país no endémico: reporte de un caso". (2008) Revista da Sociedade Brasileira de Medicina Tropical, 41 (3), 301-303
Enlaces externos [ editar ]
| Clasificación | D
|
|---|---|
| Recursos externos |
|
- "Difilobotriasis" . CDC - DPDx - Identificación de laboratorio de enfermedades parasitarias de interés para la salud pública . 2013-11-29 . Consultado el 5 de septiembre de 2015 .