Tautómero
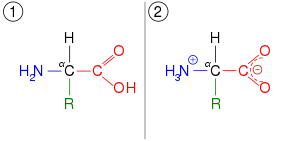
Los tautómeros ( / ˈ t ɔː t ə m ər / ) [1] son isómeros estructurales (isómeros constitucionales) de compuestos químicos que se interconvierten fácilmente. [2] [3] [4] [5] Esta reacción comúnmente resulta en la reubicación de un átomo de hidrógeno. El tautomerismo es, por ejemplo, relevante para el comportamiento de los aminoácidos y los ácidos nucleicos, dos de los componentes básicos de la vida.
El concepto de tautomerizaciones se denomina tautomerismo . El tautomerismo también se llama desmotropismo. La reacción química que interconvierte los dos se llama tautomerización .
Se debe tener cuidado de no confundir los tautómeros con representaciones de "estructuras contribuyentes" en resonancia química . Los tautómeros son especies químicas distintas que se pueden distinguir por sus diferentes conectividades atómicas, geometrías moleculares y propiedades fisicoquímicas y espectroscópicas, [6] mientras que las formas de resonancia son simplemente representaciones alternativas de la estructura de Lewis ( teoría del enlace de valencia ) de una sola especie química, cuya verdadera estructura se describe mejor como el "promedio" de las geometrías hipotéticas e idealizadas implícitas en estas formas de resonancia.
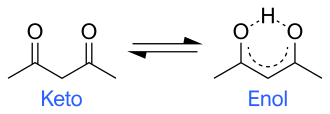
La tautomerización es omnipresente en la química orgánica . Por lo general, se asocia con moléculas polares e iones que contienen grupos funcionales que son al menos débilmente ácidos. Los tautómeros más comunes existen en pares, lo que significa que el hidrógeno está ubicado en una de dos posiciones, e incluso más específicamente, la forma más común implica que el hidrógeno cambie de lugar con un doble enlace: H−X−Y=Z ⇌ X=Y− Z-H. Los pares tautoméricos comunes incluyen: [7]
La prototropía es la forma más común de tautomerismo y se refiere a la reubicación de un átomo de hidrógeno. [8] El tautomerismo prototrópico puede considerarse un subconjunto del comportamiento ácido-base . Los tautómeros prototrópicos son conjuntos de estados de protonación isoméricos con la misma fórmula empírica y carga total . Las tautomerizaciones son catalizadas por: [ cita requerida ]
El tautomerismo de valencia es un tipo de tautomerismo en el que los enlaces simples y/o dobles se forman y rompen rápidamente, sin migración de átomos o grupos. [10] Es distinto del tautomerismo prototrópico e implica procesos con una rápida reorganización de los electrones de enlace.