Este artículo necesita citas adicionales para su verificación . ( septiembre de 2011 ) ( Aprenda cómo y cuándo eliminar este mensaje de plantilla ) |
El proceso de ácido sulfúrico húmedo ( proceso WSA ) es uno de los procesos de desulfuración de gas clave en el mercado actual. Desde que la empresa danesa de catalizadores Haldor Topsoe introdujo y patentó esta tecnología a fines de la década de 1980, ha sido reconocida como un proceso eficiente para recuperar azufre de varios gases de proceso en forma de ácido sulfúrico de calidad comercial (H 2 SO 4 ), con producción simultánea. de vapor de alta presión. El proceso WSA se aplica en todas las industrias donde la eliminación de azufre es un problema.
El proceso de catálisis húmeda es especialmente adecuado para procesar una o más corrientes que contienen azufre, tales como: [1]
- Gas H 2 S de, por ejemplo, una unidad de tratamiento de gas amina
- Gas de escape del gas del separador de agua ácida (SWS)
- Gas de escape de Rectisol
- Ácido gastado de una unidad de alquilación
- Gas de cola del proceso Claus
- Residuo pesado o coque de petróleo caldera utilidad -fired off-gas
- Gases de combustión de calderas de varios procesos Desulfuración de gases de combustión SNOX
- Gas de proceso metalúrgico
- Producción de ácido sulfúrico
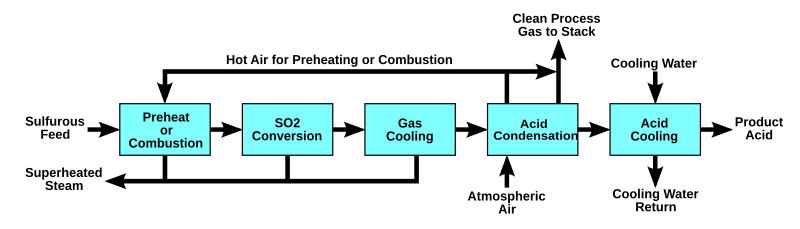
El proceso [ editar ]
- Las principales reacciones en el proceso de la WSA
- Combustión: 2 H 2 S + 3 O 2 ⇌ 2 H 2 O + 2 SO 2 + 518 kJ / mol
- Oxidación: 2 SO 2 + O 2 ⇌ 2 SO 3 + 99 kJ / mol (en presencia de un catalizador de óxido de vanadio (V) )
- Hidratación: SO 3 + H 2 O ⇌ H 2 SO 4 (g) + 101 kJ / mol
- Condensación: H 2 SO 4 (g) ⇌ H 2 SO 4 (l) + 90 kJ / mol
La energía liberada por las reacciones mencionadas anteriormente se utiliza para la producción de vapor. Aproximadamente 2 a 3 toneladas de vapor a alta presión por tonelada de ácido producido.
Aplicaciones industriales [ editar ]
Industrias donde están instaladas las plantas de proceso de WSA:
- Refinería y industria petroquímica
- Industria metalúrgica
- Industria del carbón ( coquización y gasificación)
- Industria de la energía
- Industria de la viscosa
- Industria del ácido sulfúrico
WSA para gasificadores [ editar ]
El gas ácido proveniente de un Rectisol -, Selexol -, tratamiento de amina o similar instalado después del gasificador contiene H 2 S, COS e hidrocarburos además de CO 2 . Anteriormente, estos gases solían quemarse y ventilarse a la atmósfera, pero ahora el gas ácido requiere purificación para no afectar el medio ambiente con la emisión de SO 2 . El proceso WSA no solo puede satisfacer las demandas de eliminación de SO 2 , el proceso también acepta una amplia gama de composiciones de gas de alimentación.
La planta de WSA proporciona una alta recuperación de azufre y el calor recuperado provoca una producción de vapor sustancial. La tasa de recuperación de calor es alta y el consumo de agua de refrigeración es bajo, lo que da como resultado un rendimiento superior en costes de este proceso. [ cita requerida ]
Ejemplos de proceso WSA para gasificación [ editar ]
Ejemplo 1:
- Caudal de gas de alimentación: 14.000 Nm 3 / h
- Composición [vol%]: 5.8% H 2 S, 1.2% COS, 9.7% HC y 77.4% CO 2
- Concentración de SOx [vol%]: 1,58%
- Producción de H 2 SO 4 : 106 MTPD
- Producción de vapor: 53 ton / h
- Consumo de agua de refrigeración: 8 m 3 / tonelada de ácido (delta T = 10 ° C)
- Consumo de combustible: 1.000 Nm 3 / h (LHV = 2.821 kcal / Nm 3 )
Ejemplo 2: Se construirá una planta de azufre en China en conexión con una planta de amoniaco, que producirá 500 kilotoneladas / año de amoniaco para la producción de fertilizantes [2]
Regeneración de ácido gastado y producción de ácido sulfúrico [ editar ]
El proceso WSA también se puede utilizar para la producción de ácido sulfúrico a partir de la quema de azufre o para la regeneración del ácido gastado de, por ejemplo, plantas de alquilación. Los procesos de catálisis húmeda se diferencian de otros procesos de contacto con ácido sulfúrico en que el gas de alimentación contiene un exceso de humedad cuando entra en contacto con el catalizador. El trióxido de azufre formado por oxidación catalítica del dióxido de azufre reacciona instantáneamente con la humedad para producir ácido sulfúrico en la fase de vapor en un grado determinado por la temperatura. Posteriormente se forma ácido líquido por condensación del vapor de ácido sulfúrico y no por absorción del trióxido de azufre en ácido sulfúrico concentrado, como es el caso de los procesos de contacto basados en gases secos.
La concentración del ácido del producto depende de la relación H 2 O / SO 3 en los gases convertidos catalíticamente y de la temperatura de condensación. [3] [4]
Los gases de combustión se enfrían a la temperatura de entrada del convertidor de aproximadamente 420–440 ° C. Para procesar estos gases húmedos en una planta convencional de proceso de contacto de gas frío (DCDA), sería necesario enfriar y secar el gas para eliminar toda la humedad. Por lo tanto, el proceso WSA es en muchos casos una forma más rentable de producir ácido sulfúrico.
Aproximadamente del 80% al 85% de la producción mundial de azufre se utiliza para fabricar ácido sulfúrico. El 50% de la producción mundial de ácido sulfúrico se utiliza en la producción de fertilizantes, principalmente para convertir fosfatos en formas solubles en agua, según el Manual de Fertilizantes, publicado conjuntamente por la Organización de las Naciones Unidas para el Desarrollo Industrial (ONUDI) y el Centro Internacional de Desarrollo de Fertilizantes .[5]
Referencias [ editar ]
- ^ Gary, JH y Handwerk, GE (1984). Tecnología y economía de refinación de petróleo (2ª ed.). Marcel Dekker, Inc. ISBN 0-8247-7150-8.
- ^ [1] ; Combustibles mundiales
- ^ Recuperación de azufre; (2007). Los Principios del Proceso en la recuperación de azufre por el proceso WSA.). Dinamarca: Jens Kristen Laursen, Haldor Topsoe A / S. Reimpreso de Hydrocarbonengineering agosto de 2007
- ^ Lijadora UHF; H. Fischer; U. Rothe; R. Kola (1984). Azufre, dióxido de azufre y ácido sulfúrico (1ª ed.). The British Sulphur Corporation Limited. ISBN 0-902777-64-5.
- ^ [2] ; (Julio de 2008). ENFOQUE DEL IFDC EN FERTILIZANTES Y SEGURIDAD ALIMENTARIA, Número 4; La escasez mundial de ácido sulfúrico contribuye al aumento de los costos de los fertilizantes. Archivado el 6 de enero de 2009 en Wayback Machine.