Acetilacetona
La acetilacetona es un compuesto orgánico con la fórmula química CH 3 COCH 2 COCH 3 . Es un líquido incoloro, clasificado como 1,3- dicetona . Existe en equilibrio con un tautómero CH 3 C (O) CH = (OH) CH 3 . Estos tautómeros se interconvierten tan rápidamente en la mayoría de las condiciones que se tratan como un solo compuesto en la mayoría de las aplicaciones. [2] Es un líquido incoloro que es un precursor del anión acetilacetonato (comúnmente abreviado acac - ), un ligando bidentado . También es un componente básico para la síntesis de compuestos heterocíclicos .
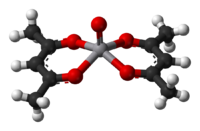
Los tautómeros ceto y enol de acetilacetona coexisten en solución. La forma enol tiene simetría C 2v , lo que significa que el átomo de hidrógeno se comparte por igual entre los dos átomos de oxígeno. [3] En la fase gaseosa, la constante de equilibrio , K ceto → enol , es 11,7, favoreciendo la forma enol. Las dos formas tautoméricas se pueden distinguir por espectroscopia de RMN , espectroscopia de IR y otros métodos. [4] [5]
La constante de equilibrio tiende a ser alta en disolventes apolares; la forma ceto se vuelve más favorable en disolventes polares con enlaces de hidrógeno, como el agua. [6] La forma enólica es un análogo vinílogo de un ácido carboxílico .
IUPAC recomienda p K a valores para este equilibrio en solución acuosa a 25 ° C son 8,99 ± 0,04 ( I = 0), 8,83 ± 0,02 ( I = 0,1 M NaClO 4 ) y 9,00 ± 0,03 ( I = 1,0 M NaClO 4 ; I = Fuerza iónica ). [8] Se dispone de valores para disolventes mixtos. Las bases muy fuertes, como los compuestos de organolitio , desprotonarán la acetilacetona dos veces. Las especies de dilithio resultantes pueden alquilarse luego en C-1.
Las rutas de laboratorio a la acetilacetona también comienzan con acetona . Acetona y anhídrido acético tras la adición de catalizador de trifluoruro de boro ( BF 3 ): [10]
Una segunda síntesis implica la condensación catalizada por bases de acetona y acetato de etilo , seguida de acidificación: [10]