Bombykol
Bombykol es una feromona liberada por la polilla del gusano de seda hembra para atraer parejas. También es la feromona sexual en la polilla de la seda salvaje ( Bombyx mandarina ). [1] [2] Descubierta por Adolf Butenandt en 1959, fue la primera feromona en ser caracterizada químicamente. [3]
Se pueden usar cantidades mínimas de esta feromona por acre de tierra para confundir a los insectos machos sobre la ubicación de sus parejas femeninas. Por lo tanto, puede servir como señuelo en trampas para eliminar insectos de manera efectiva sin rociar los cultivos con grandes cantidades de pesticidas. Butenandt nombró a la sustancia por el nombre latino de la polilla Bombyx mori. [4]
In vivo parece que bombykol es el ligando natural de una proteína de unión a feromonas, BmorPBP, que acompaña a la feromona al receptor de feromonas. [5]
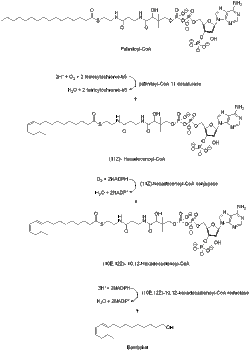
Se sabe que el bombykol se deriva de acetil-CoA a través del acil graso C-16 palmitoil-CoA . [6] Palmitoyl-CoA se convierte en bombykol en pasos que implican la desaturación y modificación reductora del carbono carbonilo. [7] En comparación con otras feromonas de Tipo I, la biosíntesis de bombykol no necesita acortamiento de cadena ni ningún otro tipo de modificación del grupo hidroxilo terminal.
Una enzima desaturasa codificada por el gen Bmpgdesat1 (Desat1) produce el monoeno (11 Z ) -hexadecenoil-CoA así como el dieno (10 E , 12 Z ) -10,12-hexadecadienoil-CoA. Esta desaturasa es la única enzima necesaria para catalizar estos dos pasos de desaturación consecutivos. [8]
El precursor de bombykol acil (10 E , 12 Z ) -10,12-hexadecadienoato se encuentra principalmente como un éster de triacilglicerol en las gotitas de lípidos citoplasmáticos de las células de la glándula de feromonas de la polilla. Y cuando las hembras adultas emergen de sus pupas, la neurohormona PBAN (neuropéptido activador de la biosíntesis de feromonas) comienza a señalar eventos que ayudan a controlar la lipólisis de los triacilgliceroles almacenados, liberando (10 E , 12 Z ) -10,12-hexadecadienoato para su final. modificación reductora. [9] [10] [11] El mecanismo de liberación lipolítica de (10 E , 12 Z) -10,12-hexadecadienoato de triacilgliceroles no se conoce completamente, pero se han identificado los genes candidatos que codifican la lipasa. [9] [10]