Reacción de Diels-Alder
| Reacción de Diels-Alder | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Lleva el nombre de | Otto Paul Hermann Diels Kurt Alder | ||||||||
| Tipo de reacción | Cicloadición | ||||||||
| Reacción | |||||||||
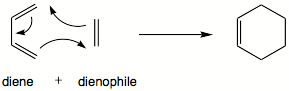
| |||||||||
| Identificadores | |||||||||
| Portal de química orgánica | reacción de diels-alder | ||||||||
| ID de ontología RSC | RXNO: 0000006 | ||||||||
En química orgánica , la reacción de Diels-Alder es una reacción química entre un dieno conjugado y un alqueno sustituido , comúnmente denominado dienófilo , para formar un derivado de ciclohexeno sustituido . Es el ejemplo prototípico de una reacción pericíclica con un mecanismo concertado . Más específicamente, se clasifica como una cicloadición [4 + 2] térmicamente permitida con el símbolo de Woodward-Hoffmann [ π 4 s + π 2 s ]. Fue descrito por primera vez por Otto Dielsy Kurt Alder en 1928. Por el descubrimiento de esta reacción, fueron galardonados con el Premio Nobel de Química en 1950. Mediante la construcción simultánea de dos nuevos enlaces carbono-carbono, la reacción Diels-Alder proporciona una forma fiable de formar seis miembros anillos con buen control sobre los resultados regio y estereoquímicos. [1] [2] En consecuencia, ha servido como una herramienta poderosa y ampliamente aplicada para la introducción de la complejidad química en la síntesis de productos naturales y nuevos materiales. [3] [4] El concepto subyacente también se ha aplicado a sistemas π que involucran heteroátomos , como carbonilos e iminas., que proporcionan los correspondientes heterociclos ; esta variante se conoce como reacción hetero-Diels-Alder . La reacción también se ha generalizado a otros tamaños de anillo, aunque ninguna de estas generalizaciones ha coincidido con la formación de anillos de seis miembros en términos de alcance o versatilidad. Debido a los valores negativos de Δ H ° y Δ S ° para una reacción típica de Diels-Alder, el reverso microscópico de una reacción de Diels-Alder se vuelve favorable a altas temperaturas, aunque esto es de importancia sintética solo para un rango limitado de Diels- Aductos de aliso, generalmente con algunas características estructurales especiales; esta reacción inversa se conoce como reacción retro-Diels-Alder . [5]
Mecanismo
La reacción es un ejemplo de una reacción pericíclica concertada. [6] Se cree que ocurre a través de un solo estado de transición cíclico, [7] sin que se generen intermedios durante el curso de la reacción. Como tal, la reacción de Diels-Alder se rige por consideraciones de simetría orbital: se clasifica como una cicloadición [ π 4 s + π 2 s ], lo que indica que procede a través de la suprafacial/ interacción suprafacial de un sistema de electrones de 4π (la estructura de dieno) con un sistema de electrones de 2π (la estructura de dienophile), una interacción que conduce a un estado de transición sin una barrera energética impuesta por simetría orbital adicional y permite que la reacción de Diels-Alder tome lugar con relativa facilidad. [8]
Una consideración de los orbitales moleculares de frontera de los reactivos (FMO) deja en claro por qué esto es así. (La misma conclusión puede extraerse de un diagrama de correlación orbital o de un análisis de Dewar-Zimmerman.) Para la reacción de Diels-Alder de demanda de electrones "normal" más común, la más importante de las dos interacciones HOMO / LUMO es que entre el electrón- rica de dieno ψ 2 como el orbital más alto ocupado (HOMO) con * π del dienófilo deficiente en electrones como la más baja orbital molecular desocupado (LUMO). Sin embargo, la brecha de energía HOMO – LUMO es lo suficientemente cercana como para que los roles se puedan revertir al cambiar los efectos electrónicos de los sustituyentes en los dos componentes. En una reacción de Diels-Alder de demanda de electrones inversa (inversa), los sustituyentes aceptores de electrones en el dieno reducen la energía de su orbital ψ 3 vacío y los sustituyentes donantes de electrones en el dienófilo aumentan la energía de su orbital π lleno lo suficiente como para que la interacción entre estos dos orbitales se convierta en la interacción orbital estabilizadora más significativa desde el punto de vista energético. Independientemente de la situación que corresponda, el HOMO y LUMO de los componentes están en fase y se produce una interacción de enlace como se puede ver en el diagrama siguiente. Dado que los reactivos están en su estado fundamental, la reacción se inicia térmicamente y no requiere activación por luz. [8]
La "opinión predominante" [9] [10] [11] [12] es que la mayoría de las reacciones Diels-Alder proceden a través de un mecanismo concertado; Sin embargo, la cuestión ha sido objeto de una polémica contundencia. A pesar del hecho de que la gran mayoría de las reacciones de Diels-Alder exhiben una adición sincrónica estereoespecífica de los dos componentes, se ha postulado un intermedio dirradical [7] (y se ha apoyado con evidencia computacional) sobre la base de que la estereoespecificidad observada no descarta un adición de dos pasos que involucra un intermedio que colapsa para producir un producto más rápido de lo que puede rotar para permitir la inversión de la estereoquímica.
Hay una mejora notable de la velocidad cuando ciertas reacciones de Diels-Alder se llevan a cabo en disolventes orgánicos polares como dimetilformamida y etilenglicol, [13] e incluso en agua. [14] La reacción del ciclopentadieno y la butenona, por ejemplo, es 700 veces más rápida en agua con respecto al 2,2,4-trimetilpentano como disolvente. [14] Se han propuesto varias explicaciones para este efecto, como un aumento en la concentración efectiva debido al empaquetamiento hidrófobo [15] o la estabilización del estado de transición por enlaces de hidrógeno. [dieciséis]
La geometría de los componentes dieno y dienophile se propaga cada uno en detalles estereoquímicos del producto. Para reacciones intermoleculares especialmente, la relación posicional y estereoquímica preferida de los subtítulos de los dos componentes comparados entre sí está controlada por efectos electrónicos. Sin embargo, para las reacciones de cicloadición intramolecular de Diels-Alder , la estabilidad conformacional de la estructura del estado de transición puede ser una influencia abrumadora.
Regioselectividad
La teoría de los orbitales moleculares de frontera también se ha utilizado para explicar los patrones de regioselectividad observados en las reacciones de Diels-Alder de sistemas sustituidos. El cálculo de los coeficientes de energía y orbitales de los orbitales fronterizos de los componentes [17] proporciona una imagen que concuerda con el análisis más sencillo de los efectos de resonancia de los sustituyentes, como se ilustra a continuación.
En general, la regioselectividad encontrada para la reacción de Diels-Alder de demanda de electrones normal e inversa sigue la regla orto-para , llamada así, porque el producto ciclohexeno tiene sustituyentes en posiciones que son análogas a las de orto y para.posiciones de arenos disustituidos. Por ejemplo, en un escenario de demanda normal, un dieno que lleva un grupo donante de electrones (EDG) en C1 tiene su mayor coeficiente de HOMO en C4, mientras que el dienófilo con un grupo de extracción de electrones (EWG) en C1 tiene el mayor coeficiente de LUMO en C2. Al emparejar estos dos coeficientes se obtiene el producto "orto" como se ve en el caso 1 en la figura siguiente. Un dieno sustituido en C2 como en el caso 2 a continuación tiene el mayor coeficiente HOMO en C1, dando lugar al producto "para". Análisis similares para los correspondientes escenarios de demanda inversa dan lugar a productos análogos como se ve en los casos 3 y 4. Al examinar las formas mesoméricas canónicas anteriores, es fácil verificar que estos resultados están de acuerdo con las expectativas basadas en la consideración de la densidad electrónica y polarización.
En general, con respecto al par HOMO-LUMO energéticamente mejor emparejado, maximizar la energía de interacción mediante la formación de enlaces entre los centros con los coeficientes orbitales de frontera más grandes permite predecir el regioisómero principal que resultará de una combinación dada de dieno-dienófilo. [8] En un tratamiento más sofisticado, tres tipos de sustituyentes ( retiro de Z : disminución de HOMO y LUMO (CF 3 , NO 2 , CN, C (O) CH 3 ), donación de X : aumento de HOMO y LUMO (Me, OMe, NMe 2 ), C conjugando : Se consideran la subida de HOMO y la bajada de LUMO (Ph, vinilo)), lo que da como resultado un total de 18 combinaciones posibles. La maximización de la interacción orbital predice correctamente el producto en todos los casos para los que se dispone de datos experimentales. Por ejemplo, en combinaciones poco comunes que involucran grupos X tanto en dieno como en dienófilo, se puede favorecer un patrón de sustitución 1,3, un resultado que no se explica por un argumento de estructura de resonancia simplista. [18] Sin embargo, los casos en los que el argumento de resonancia y la coincidencia de los coeficientes orbitales más grandes no concuerdan son raros.
Estereoespecificidad y estereoselectividad
Las reacciones de Diels-Alder, como cicloadiciones concertadas, son estereoespecíficas . La información estereoquímica del dieno y el dienófilo se retiene en el producto, como una adición sincrónica con respecto a cada componente. Por ejemplo, los sustituyentes en una relación cis ( trans , resp.) En el doble enlace del dienófilo dan lugar a sustituyentes que son cis ( trans , resp.) En esos mismos carbonos con respecto al anillo de ciclohexeno. Del mismo modo, los dienos cis , cis y trans , trans disustituidos dan sustituyentes cis en estos carbonos del producto, mientras que cis, los dienos trans- disustituidos dan sustituyentes trans : [19] [20]
Las reacciones de Diels-Alder en las que se generan estereocentros adyacentes en los dos extremos de los enlaces simples recién formados implican dos posibles resultados estereoquímicos diferentes. Esta es una situación estereoselectiva basada en la orientación relativa de los dos componentes separados cuando reaccionan entre sí. En el contexto de la reacción de Diels-Alder, el estado de transición en el que el sustituyente más significativo (un grupo conjugador y / o receptor de electrones) del dienófilo se orienta hacia el sistema dieno π y se desliza por debajo de él a medida que tiene lugar la reacción es conocido como el estado de transición endo . En el estado de transición exo alternativo , está orientado lejos de él. (Hay un uso más general de los términos endo yexo en nomenclatura estereoquímica.)
En los casos en los que el dienófilo tiene un solo sustituyente conjugador / atractor de electrones, o dos sustituyentes conjugadores / aceptores de electrones cis entre sí, el resultado a menudo puede predecirse. En estos escenarios Diels-Alder de "demanda normal", normalmente se prefiere el estado de transición endo , a pesar de que a menudo está más congestionado estéricamente. Esta preferencia se conoce como la regla Alder endo . Como dijo Alder originalmente, el estado de transición que se prefiere es el que tiene una "acumulación máxima de dobles enlaces". La endo selectividad es típicamente más alta para dienophiles rígidos tales como anhídrido maleico y benzoquinona ; para otros, como los acrilatos ycrotonatos , la selectividad no es muy pronunciada. [21]
La explicación más aceptada del origen de este efecto es una interacción favorable entre los sistemas π del dienófilo y el dieno, una interacción descrita como un efecto orbital secundario , aunque las atracciones dipolares y de van der Waals también pueden influir, y El disolvente a veces puede marcar una diferencia sustancial en la selectividad. [6] [22] [23] La explicación de superposición orbital secundaria fue propuesta por primera vez por Woodward y Hoffmann. [24] En esta explicación, los orbitales asociados con el grupo en conjugación con el doble enlace dienophile se superponen con los orbitales interiores del dieno, una situación que es posible sólo para el endoestado de transición. Aunque la explicación original solo invocaba el orbital en el átomo α para el doble enlace del dienófilo, Salem y Houk han propuesto posteriormente que los orbitales en los carbonos α y β participan cuando la geometría molecular lo permite. [25]
A menudo, como ocurre con los dienos altamente sustituidos, los dienófilos muy voluminosos o las reacciones reversibles (como en el caso del furano como dieno), los efectos estéricos pueden anular la endo selectividad normal a favor del isómero exo .
El dieno
El componente dieno de la reacción de Diels-Alder puede ser de cadena abierta o cíclico, y puede albergar muchos tipos diferentes de sustituyentes; [6] debe, sin embargo, poder existir en la conformación s- cis , ya que este es el único confórmero que puede participar en la reacción. Aunque los butadienos suelen ser más estables en la conformación s-trans, en la mayoría de los casos la diferencia de energía es pequeña (~ 2 a 5 kcal / mol). [26]
Un sustituyente voluminoso en la posición C2 o C3 puede aumentar la velocidad de reacción desestabilizando la conformación s- trans y forzando al dieno a la conformación s- cis reactiva . El 2- terc -butil-buta-1,3-dieno, por ejemplo, es 27 veces más reactivo que el butadieno simple. [6] [27] A la inversa, un dieno que tiene sustituyentes voluminosos tanto en C2 como en C3 es menos reactivo porque las interacciones estéricas entre los sustituyentes desestabilizan la conformación s- cis . [27]
Los dienos con sustituyentes terminales voluminosos (C1 y C4) disminuyen la velocidad de reacción, presumiblemente al impedir el acercamiento del dieno y el dienófilo. [28]
Un dieno especialmente reactivo es el 1-metoxi-3-trimetilsiloxi-buta-1,3-dieno, también conocido como dieno de Danishefsky . [29] Tiene una utilidad sintética particular como medio para proporcionar sistemas de ciclohexenona α, β-insaturados mediante la eliminación del sustituyente 1-metoxi después de la desprotección del enol silil éter. Otros derivados sintéticamente útiles del dieno de Danishefsky incluyen 1,3-alcoxi-1-trimetilsiloxi-1,3-butadienos (Brassard dienos) [30] y 1-dialquilamino-3-trimetilsiloxi-1,3-butadienos (Rawal dienos). [31] El aumento de la reactividad de estos y otros dienos similares es el resultado de contribuciones sinérgicas de los grupos donantes en C1 y C3, elevando el HOMO significativamente por encima del de un dieno monosustituido comparable. [3]
Los dienos inestables (y por tanto muy reactivos), de los cuales quizás los más útiles sintéticamente son los o - quinodimetanos , pueden generarse in situ. [32] Una fuerte fuerza impulsora de la cicloadición [4 + 2] de tales especies es el resultado del establecimiento (o restablecimiento) de la aromaticidad. Los métodos comunes para generar o- quinodimetanos incluyen la pirólisis de benzociclobutenos [6] o la correspondiente sulfona, [3] 1,4-eliminación de silanos ortobencílicos [33] o estannanos, [34] [35] [36] y reducción de α , dibromuros α'-ortobencílicos. [37]
Por el contrario, dienos estables son más bien no reactivo y se someten a reacciones de Diels-Alder sólo a temperaturas elevadas: por ejemplo, naftaleno puede funcionar como un dieno, que conduce a aductos solamente con dienófilos altamente reactivos, tales como N -fenil- maleimida . El antraceno , al ser menos aromático (y por tanto más reactivo para las síntesis de Diels-Alder) en su anillo central, puede formar un aducto 9,10 con anhídrido maleico a 80 ° C e incluso con acetileno , un dienófilo débil, a 250 ° C. [38]
El dienophile
En una reacción de Diels-Alder a demanda normal, el dienófilo tiene un grupo captador de electrones en conjugación con el alqueno; en un escenario de demanda inversa, el dienófilo se conjuga con un grupo donante de electrones. [9] Los dienophiles se pueden elegir para que contengan una "funcionalidad enmascarada". El dienófilo sufre una reacción de Diels-Alder con un dieno que introduce dicha funcionalidad en la molécula del producto. A continuación, sigue una serie de reacciones para transformar la funcionalidad en un grupo deseable. El producto final no se puede fabricar en un solo paso de DA porque el dienófilo equivalente no es reactivo o es inaccesible. Un ejemplo de tal enfoque es el uso de α-cloroacrilonitrilo (CH 2= CClCN). Cuando reacciona con un dieno, este dienófilo introducirá la funcionalidad α-cloronitrilo en la molécula del producto. Esta es una "funcionalidad enmascarada" que luego puede hidrolizarse para formar una cetona. El dienófilo de α-cloroacrilonitrilo es un equivalente del dienófilo de ceteno (CH 2 = C = O), que produciría el mismo producto en un paso de DA. El problema es que la cetena en sí misma no se puede usar en las reacciones de Diels-Alder porque reacciona con los dienos de manera no deseada (mediante cicloadición [2 + 2]) y, por lo tanto, se debe usar el enfoque de "funcionalidad enmascarada". [39] Otras funcionalidades de este tipo son sustituyentes de fosfonio (que producen dobles enlaces exocíclicos después de la reacción de Wittig), varias funciones de sulfóxido y sulfonilo (ambas son equivalentes de acetileno) y grupos nitro (equivalentes de cetena).[6]
Variantes de la reacción clásica de Diels-Alder
Hetero-Diels – Alder
También se conocen reacciones de Diels-Alder que involucran al menos un heteroátomo y se denominan colectivamente reacciones de hetero-Diels-Alder. [40] Los grupos carbonilo , por ejemplo, pueden reaccionar con éxito con dienos para producir anillos de dihidropirano , una reacción conocida como reacción oxo-Diels-Alder , y las iminas se pueden utilizar, ya sea como dienophile o en varios sitios del dieno, para forman varios compuestos N -heterocíclicos a través de la reacción de aza-Diels-Alder . Los compuestos nitrosos (RN = O) pueden reaccionar con dienos para formar oxazinas . El isocianato de clorosulfonilo se puede utilizar como dienófilo para preparar la lactama de Vince.. [6] [41]
Activación del ácido de Lewis
Los ácidos de Lewis , como el cloruro de zinc, el trifluoruro de boro, el tetracloruro de estaño, el cloruro de aluminio, etc., pueden actuar como catalizadores de reacciones de Diels-Alder de demanda normal por coordinación con el dienófilo. El dienófilo complejado se vuelve más electrófilo y más reactivo hacia el dieno, aumentando la velocidad de reacción y, a menudo, mejorando también la regio y la estereoselectividad. La catálisis ácida de Lewis también permite que las reacciones de Diels-Alder se desarrollen a bajas temperaturas, es decir, sin activación térmica. [6]
Diels-Alder asimétrico
Muchos métodos han sido desarrollados para influir sobre la estereoselectividad de la reacción de Diels-Alder, tales como el uso de auxiliares quirales, la catálisis por ácidos de Lewis quirales , [42] y pequeñas catalizadores molécula orgánica . [6] Oxazolidinonas de Evans , [43] oxazaborolidinas , [44] [45] [46] quelatos de bis -oxazolina- cobre , [47] catálisis de imidazolina , [48] y existen muchas otras metodologías para efectuar Diels diastereo- y enantioselectivos- Reacciones de aliso.
Hexadehydro Diels – Alder
En la reacción hexadehidro Diels-Alder , se utilizan alquinos y diinos en lugar de alquenos y dienos, formando un intermedio bencínico inestable que luego puede ser atrapado para formar un producto aromático. Esta reacción permite la formación de anillos aromáticos fuertemente funcionalizados en un solo paso. [49]
Aplicaciones
La reacción retro Diels-Alder se utiliza en la producción industrial de ciclopentadieno . El ciclopentadieno es un precursor de varios norbornenos , que son monómeros comunes . La reacción de Diels-Alder también se emplea en la producción de vitamina B6 .
Historia
El trabajo de Diels y Alder se describe en una serie de 28 artículos publicados en Justus Liebigs Annalen der Chemie y Berichte der deutschen chemischen Gesellschaft de 1928 a 1937. Los primeros 19 artículos fueron escritos por Diels y Alder, mientras que los artículos posteriores fueron escritos por por Diels y varios colaboradores. [51] [52]
La primera aplicación de la reacción de Diels-Alder en la síntesis total fue ilustrada por la síntesis de RB Woodward de los esteroides cortisona y colesterol . [53] La reacción del butadieno con la quinona a continuación proporcionó los anillos C y D del esqueleto de esteroides con la regioquímica deseada.
EJ Corey , en su síntesis original de 1969 de prostaglandinas F2α y E2, [54] utilizó una reacción de Diels-Alder al principio de la síntesis para establecer la estereoquímica relativa de tres estereocentros contiguos en el núcleo de prostaglandina ciclopentano. Para mitigar la isomerización del ciclopentadieno sustituido a través del desplazamiento de hidruro 1,5 , se consideró necesario mantener este intermedio por debajo de 0 ° C hasta que pudiera producirse el Diels-Alder. Por tanto, se requirió la activación por tetrafluoroborato cúprico fuertemente ácido de Lewis para permitir que tuviera lugar la reacción. El uso de 2-cloroacrilonitrilo como dienófilo es un equivalente sintético viable para la cetena, [9]una estructura que típicamente sufre una cicloadición [2 + 2] para dar un dímero de ciclobutanona en lugar de participar en reacciones de Diels-Alder con 1,3-dienos. [55] [56] La hidrólisis de la mezcla epimérica de aductos de cloronitrilo reveló la bicicloheptanona deseada con alto rendimiento.
Samuel J. Danishefsky utilizó una reacción de Diels-Alder para sintetizar el prefenato de disodio , [57] un precursor biosintético de los aminoácidos fenilalanina y tirosina, en 1979. Esta secuencia es notable como una de las primeras en presentar 1-metoxi-3-siloxibutadieno , el llamado dieno Danishefsky, en síntesis total. Su utilidad es evidente a continuación, a saber, el fácil suministro de sistemas de ciclohexenona α, β-insaturados.
En su síntesis de reserpina de 1980 , [58] Paul Wender y colaboradores utilizaron una reacción de Diels-Alder para establecer el marco de cis-decalina de los anillos D y E del producto natural. El Diels-Alder inicial entre el ácido 2-acetoxiacrílico y el 1,2-dihidropiridin-1-carboxilato que se muestra a continuación puso al grupo carboxilo recién instalado en una posición para reorganizarse exclusivamente en los anillos condensados en cis después de la conversión en el isoquinuclideno que se muestra a continuación. La fusión cis permitió el establecimiento de la estereoquímica en C17 y C18: primero por escisión del grupo acetato en C18 para dar una cetona que puede modular la estereoquímica del grupo metoxi C17, y luego por reducción de la cetona en C18 de la cara exo para lograr la estereoquímica del producto final.
En la síntesis de reserpina de Stephen F. Martin , [59] los anillos D y E fusionados en cis también se formaron mediante una reacción de Diels-Alder. Diels-Alder intramolecular de la piranona a continuación con la posterior extrusión de dióxido de carbono a través de un retro [4 + 2] produjo la lactama bicíclica. La epoxidación de la cara α menos impedida, seguida de la apertura del epóxido en el C18 menos impedido proporcionó la estereoquímica deseada en estas posiciones, mientras que la fusión en cis se logró con hidrogenación, procediendo de nuevo principalmente desde la cara menos impedida.
De manera similar, el grupo de KC Nicolaou utilizó una piranona como dienófilo en la síntesis total de taxol . [60] La reacción intermolecular de la hidroxipirona y el éster α, β-insaturado que se muestra a continuación sufrió un bajo rendimiento y regioselectividad; sin embargo, cuando está dirigido por ácido fenilborónico [61], el aducto deseado podría obtenerse con un rendimiento del 61% después de la escisión del boronato con 2,2-dimetil-1,3-propanodiol. La estereoespecificidad de la reacción de Diels-Alder en este caso permitió la definición de cuatro estereocentros que se llevaron al producto final.
Una reacción de Diels-Alder fue el paso clave en la síntesis de Amos Smith de (-) - furaquinocina C. [62] La diona 1 se convirtió en el dieno requerido por enolización usando dos sililaciones sucesivas con TMSCl. La cicloadición de Diels-Alder con bromoquinona fue seguida de una deshidrohalogenación espontánea para volver a formar el anillo aromático . El dieno en este caso es notable como un raro ejemplo de un derivado cíclico del dieno de Danishefsky.
Viresh Rawal y Sergey Kozmin , en su síntesis de 1998 de tabersonina, [63] utilizaron un Diels-Alder para establecer la estereoquímica relativa cis del núcleo del alcaloide. La conversión del cis-aldehído en su correspondiente alqueno por olefinación de Wittig y la subsiguiente metátesis de cierre del anillo con un catalizador Schrock dio el segundo anillo del núcleo del alcaloide. El dieno en este caso es notable como un ejemplo de 1-amino-3-siloxibutadieno, también conocido como dieno Rawal.
En 1988, William Okamura y Richard Gibbs informaron de una síntesis enantioselectiva de (+) - esterpureno [64] que presentaba una notable reacción intramolecular de Diels-Alder de un aleno. La transposición [2,3] -sigmatrópica del grupo tiofenilo para dar el sulfóxido como se indica a continuación procedió enantioespecíficamente debido a la estereoquímica predefinida del alcohol propargílico. De esta manera, el isómero de aleno único formado podría hacer que Diels-Alder se produzca en una sola cara del 'dieno' generado.
La síntesis de 2005 de Andrew Myers de (-) - tetraciclina [65] logró el núcleo tetracíclico lineal del antibiótico con una reacción de Diels-Alder. La apertura conrotatoria iniciada térmicamente del benzociclobuteno generó el o-quinodimetano, que reaccionó intermolecularmente para dar el esqueleto de tetraciclina; el diastereoisómero mostrado se cristalizó luego en metanol después de la purificación mediante cromatografía en columna. Los autores señalan que el grupo hidroxilo libre del dienófilo fue parte integral del éxito de la reacción, ya que las variantes protegidas con hidroxilo no reaccionaron en varias condiciones de reacción diferentes.
Takemura y col. cantharadrin sintetizado en 1980 por Diels-Alder, utilizando alta presión. [66]
Las aplicaciones sintéticas de la reacción de Diels-Alder se han revisado extensamente. [67] [68] [69] [70] [71]
Ver también
- Cicloadición Bradsher
- Reacción de Wagner-Jauregg
- Reacción de Imine Diels-Alder
- Reacción de Aza-Diels-Alder
Referencias
- ↑ Kloetzel, MC (1948). "La reacción de Diels-Alder con anhídrido maleico". Reacciones orgánicas . 4 . págs. 1-59. doi : 10.1002 / 0471264180.or004.01 . ISBN 978-0471264187.
- ^ Holmes, HL (1948). "Los dienophiles etilenicos y acetilénicos de la reacción de Diels-Alder". Reacciones orgánicas . 4 . págs. 60-173. doi : 10.1002 / 0471264180.or004.02 . ISBN 978-0471264187.
- ^ a b c Nicolaou, KC; Snyder, SA; Montagnon, T .; Vassilikogiannakis, G. (2002). "La reacción de Diels-Alder en síntesis total". Angewandte Chemie International Edition . 41 (10): 1668–1698. doi : 10.1002 / 1521-3773 (20020517) 41:10 <1668 :: AID-ANIE1668> 3.0.CO; 2-Z . PMID 19750686 .
- ^ Atilla Tasdelen, Mehmet (2011). Reacciones de "clic" de Diels-Alder: aplicaciones recientes en ciencia de materiales y polímeros ". Química de polímeros . 2 (10): 2133–2145. doi : 10.1039 / C1PY00041A .
- ^ Zweifel, GS; Nantz, MH (2007). Síntesis orgánica moderna: una introducción . WH Freeman and Co. ISBN 978-0-7167-7266-8.
- ^ a b c d e f g h i Carey , Parte B., págs. 474–526
- ^ a b Dewar, MJ; Olivella, S .; Stewart, JJ (1986). "Mecanismo de la reacción de Diels-Alder: reacciones de butadieno con etileno y cianoetilenos". Revista de la Sociedad Química Estadounidense . 108 (19): 5771–5779. doi : 10.1021 / ja00279a018 . PMID 22175326 .
- ^ a b c Carey , Parte A., págs. 836–50
- ↑ a b c Carey , Parte A., pág. 839
- ^ Gajewski, JJ; Peterson, KB; Kagel, JR (1987). "Variación de la estructura del estado de transición en la reacción de Diels-Alder de los efectos de isótopos cinéticos secundarios del deuterio: la reacción de un dieno y un dienophile casi simétricos es casi sincrónica". Revista de la Sociedad Química Estadounidense . 109 (18): 5545–5546. doi : 10.1021 / ja00252a052 .
- ^ Houk, KN; Lin, YT; Brown, FK (1986). "Evidencia del mecanismo concertado de la reacción de Diels-Alder de butadieno con etileno". Revista de la Sociedad Química Estadounidense . 108 (3): 554–556. doi : 10.1021 / ja00263a059 . PMID 22175504 .
- ^ Goldstein, E .; Beno, B .; Houk, KN (1996). "Predicción de la teoría funcional de la densidad de las energías relativas y efectos isotópicos para los mecanismos concertados y escalonados de la reacción de Diels-Alder de butadieno y etileno". Revista de la Sociedad Química Estadounidense . 118 (25): 6036–6043. doi : 10.1021 / ja9601494 .
- ^ Breslow, R .; Guo, T. (1988). "Reacciones de Diels-Alder en disolventes polares no acuosos. Efectos cinéticos de agentes caotrópicos y antichaotrópicos y de β-ciclodextrina". Revista de la Sociedad Química Estadounidense . 110 (17): 5613–5617. doi : 10.1021 / ja00225a003 .
- ^ a b Rideout, DC; Breslow, R. (1980). "Aceleración hidrofóbica de reacciones de Diels-Alder". Revista de la Sociedad Química Estadounidense . 102 (26): 7816–7817. doi : 10.1021 / ja00546a048 .
- ^ Breslow, R .; Rizzo, CJ (1991). "Efectos de la sal caotrópica en una reacción de Diels-Alder hidrofóbicamente acelerada". Revista de la Sociedad Química Estadounidense . 113 (11): 4340–4341. doi : 10.1021 / ja00011a052 .
- ^ Blokzijl, Wilfried; Engberts, Jan BFN (1992). "Efectos del estado inicial y del estado de transición sobre las reacciones de Diels-Alder en agua y disolventes acuosos mixtos". Revista de la Sociedad Química Estadounidense . 114 (13): 5440–5442. doi : 10.1021 / ja00039a074 .
- ^ Ashby, EC; Chao, L.-C .; Neumann, HM (1973). "Mecanismos de reacción organometálica. XII. Mecanismo de adición de bromuro de metilmagnesio al benzonitrilo". Revista de la Sociedad Química Estadounidense . 95 (15): 4896–4904. doi : 10.1021 / ja00796a022 .
- ^ Fleming, I. (1990). Frontier Orbital y Reacciones químicas orgánicas . Chichester, Reino Unido: Wiley. ISBN 978-0471018193.
- ^ Kirmse, W .; Mönch, D. (1991). "Umlagerungen von 1,4,4- und 2,2,5-trimetilbiciclo [3.2.1] oct-6-il-Kationen". Chemische Berichte . 124 (1): 237–240. doi : 10.1002 / cber.19911240136 .
- ^ Bérubé, G .; DesLongchamps, P. (1987). "Stéréosélection acyclique-1,5: Synthèse de la chaîne latérale optiquement active de la vitamine E". Bulletin de la Société Chimique de France . 1 : 103-115.
- ^ Houk, KN; Luskus, LJ (1971). "Influencia de las interacciones estéricas en la endoestereoselectividad". Revista de la Sociedad Química Estadounidense . 93 (18): 4606–4607. doi : 10.1021 / ja00747a052 .
- ^ Kobuke, Y .; Sugimoto, T .; Furukawa, J .; Fueno, T. (1972). "Papel de las interacciones atractivas en las estereoselectividades endo-exo de las reacciones de Diels-Alder". Revista de la Sociedad Química Estadounidense . 94 (10): 3633–3635. doi : 10.1021 / ja00765a066 .
- ^ Williamson, KL; Hsu, Y.-FL (1970). "Estereoquímica de la reacción de Diels-Alder. II. Catálisis ácida de Lewis de la isomería syn-anti". Revista de la Sociedad Química Estadounidense . 92 (25): 7385–7389. doi : 10.1021 / ja00728a022 .
- ^ 1917-1979, Woodward, RB (Robert Burns) (22 de octubre de 2013). La conservación de la simetría orbital . Hoffmann, R. Weinheim. ISBN 9781483282046. OCLC 915343522 .CS1 maint: nombres numéricos: lista de autores ( enlace )
- ^ Wannere, Chaitanya S .; Paul, Ankan; Herges, Rainer; Houk, KN; Schaefer, Henry F .; Schleyer, Paul Von Ragué (2007). "La existencia de interacciones orbitales secundarias" . Revista de Química Computacional . 28 (1): 344–361. doi : 10.1002 / jcc.20532 . ISSN 1096-987X . PMID 17109435 . S2CID 26096085 .
- ^ Carey , Parte A, p. 149
- ↑ a b Backer, HJ (1939). "Le 2,3-Ditertiobutylbutadiène". Recueil des Travaux Chimiques des Pays-Bas . 58 (7): 643–661. doi : 10.1002 / recl.19390580712 .
- ^ Craig, D .; Shipman, JJ; Fowler, RB (1961). "La tasa de reacción del anhídrido maleico con 1,3-dienos en relación con la conformación del dieno". Revista de la Sociedad Química Estadounidense . 83 (13): 2885–2891. doi : 10.1021 / ja01474a023 .
- ^ Danishefsky, S .; Kitahara, T. (1974). "Dieno útil para la reacción de Diels-Alder". Revista de la Sociedad Química Estadounidense . 96 (25): 7807–7808. doi : 10.1021 / ja00832a031 .
- ^ Savard, J .; Brassard, P. (1979). "Síntesis regioespecífica de quinonas utilizando acetales de vinilceteno derivados de ésteres insaturados". Letras de tetraedro . 20 (51): 4911–4914. doi : 10.1016 / S0040-4039 (01) 86747-2 .
- ^ Kozmin, SA; Rawal, VH (1997). "Preparación y reactividad de Diels-Alder de 1-amino-3-siloxi-1,3-butadienos". Revista de Química Orgánica . 62 (16): 5252–5253. doi : 10.1021 / jo970438q .
- ^ Klundt, IL (1970). "Benzociclobuteno y sus derivados". Revisiones químicas . 70 (4): 471–487. doi : 10.1021 / cr60266a002 .
- ^ Ito, Y .; Nakatsuka, M .; Saegusa, T. (1982). "Síntesis de sistemas de anillos policíclicos basados en la nueva generación de o- quinodimetanos". Revista de la Sociedad Química Estadounidense . 104 (26): 7609–7622. doi : 10.1021 / ja00390a036 .
- ^ Sano, H .; Ohtsuka, H .; Migita, T. (1988). "Un método conveniente para la generación de o- quinodimetanos por eliminación 1,4 inducida por protones de o - (1-hidroxialquil) benciltributilestannanes". Revista de la Sociedad Química Estadounidense . 110 (6): 2014-2015. doi : 10.1021 / ja00214a083 .
- ^ Pronto, HW (1993). "Un nuevo método para la generación de O -quinodimethane por la fragmentación selenio inducida de o vinil benzyltributylstannane". Letras de tetraedro . 34 (47): 7587–7590. doi : 10.1016 / S0040-4039 (00) 60407-0 .
- ^ Pronto, HW (1994). "Generación promovida por ácido de Lewis de α- oxi - o- quinodimetanos y reacciones de cicloadición". Letras de tetraedro . 35 (23): 3975–3978. doi : 10.1016 / S0040-4039 (00) 76717-7 .
- ^ Rubottom, GM; Way, JE (1984). "Un método mejorado para la preparación de o- quinodimetanos". Comunicaciones sintéticas . 14 (6): 507–514. doi : 10.1080 / 00397918408059572 .
- ^ Margareta Avram (1983). Chimie organica p. 318-323. Editura Academiei Republicii Socialiste România
- ^ Ranganathan, S .; Ranganathan, D .; Mehrotra, AK (1977). "Equivalentes de ceteno". Síntesis . 1977 (5): 289-296. doi : 10.1055 / s-1977-24362 .
- ^ Roush, WR (1991). "Reacciones intramoleculares de Diels-Alder". En Trost, BM; Flemming, I. (eds.). Síntesis orgánica integral . Vol. 5. págs. 513–550. doi : 10.1016 / B978-0-08-052349-1.00131-1 . ISBN 978-0-08-052349-1.
|volume=tiene texto extra ( ayuda ) - ^ Grieco, PA; Larsen, SD (1990). "Reacciones de diels-aliso basadas en iones de imino: N-bencil-2-azanorboreno" (PDF) . Síntesis orgánicas . 68 : 206. doi : 10.15227 / orgsyn.068.0206 .
- ^ White, James D .; Shaw, Subrata (2011). "cis-2,5-diaminobiciclo [2.2.2] octano, un nuevo andamio para catálisis asimétrica a través de complejos Salen-Metal". Org. Letón. 13 (9): 2488–91. doi : 10.1021 / ol2007378 . PMID 21462988 .
- ^ Evans, DA; Chapman, KT; Bisaha, J. (1988). "Reacciones asimétricas de cicloadición de Diels-Alder con N-aciloxazolidinonas quirales α, β-insaturadas". Revista de la Sociedad Química Estadounidense . 110 (4): 1238-1256. doi : 10.1021 / ja00212a037 .
- ^ Corey, EJ; Loh, TP (1991). "Primera aplicación de interacciones intramoleculares atractivas al diseño de catalizadores quirales para reacciones Diels-Alder altamente enantioselectivas". Revista de la Sociedad Química Estadounidense . 113 (23): 8966–8967. doi : 10.1021 / ja00023a066 .
- ^ Corey, EJ; Shibata, T .; Lee, TW (2002). "Reacciones asimétricas de Diels-Alder catalizadas por una oxazaborolidina quiral activada con ácido tríflico". Revista de la Sociedad Química Estadounidense . 124 (15): 3808–3809. doi : 10.1021 / ja025848x . PMID 11942799 .
- ^ Ryu, DH; Corey, EJ (2003). "La activación de triflimida de una oxazaborolidina quiral conduce a un sistema catalítico más general para la adición enantioselectiva de Diels-Alder". Revista de la Sociedad Química Estadounidense . 125 (21): 6388–6390. doi : 10.1021 / ja035393r . PMID 12785777 .
- ^ Johnson, JS; Evans, DA (2000). "Complejos quirales de bis (oxazolina) cobre (II): catalizadores versátiles para reacciones de cicloadición enantioselectiva, Aldol, Michael y carbonyl Ene". Cuentas de Investigación Química . 33 (6): 325–335. doi : 10.1021 / ar960062n . PMID 10891050 .
- ^ Ahrendt, KA; Borths, CJ; MacMillan, DWC (2000). "Nuevas estrategias para la catálisis orgánica: la primera reacción de Diels-Alder organocatalítica altamente enantioselectiva". Revista de la Sociedad Química Estadounidense . 122 (17): 4243–4244. doi : 10.1021 / ja000092s .
- ^ Hoye, TR; Baire, B .; Niu, D .; Willoughby, PH; Woods, BP Nature , 2012 , 490 , 208 [1]
- ^ Behr, Arno (2000). "Compuestos organometálicos y catálisis homogénea". Enciclopedia de química industrial de Ullmann . doi : 10.1002 / 14356007.a18_215 . ISBN 978-3527306732.
- ^
- Diels, O .; Alder, K. (1928). "Synthesen in der hydroaromatischen Reihe, I". Justus Liebigs Annalen der Chemie . 460 : 98-122. doi : 10.1002 / jlac.19284600106 .
- Diels, O .; Alder, K. (1929). "Synthesen in der hydroaromatischen Reihe, II". Berichte der Deutschen Chemischen Gesellschaft . 62 (3): 554–562. doi : 10.1002 / cber.19290620318 .
- Diels, O .; Alder, K. (1929). "Synthesen in der hydroaromatischen Reihe, III". Justus Liebigs Annalen der Chemie . 470 : 62-103. doi : 10.1002 / jlac.19294700106 .
- Diels, O .; Alder, K. (1929). "Synthesen in der hydroaromatischen Reihe, IV". Berichte der Deutschen Chemischen Gesellschaft . 62 (8): 2081-2087. doi : 10.1002 / cber.19290620829 .
- Diels, O .; Alder, K. (1929). "Synthesen in der hydroaromatischen Reihe, V". Berichte der Deutschen Chemischen Gesellschaft . 62 (8): 2087–2090. doi : 10.1002 / cber.19290620830 .
- Diels, O .; Alder, K. (1929). "Synthesen in der hydroaromatischen Reihe, VI". Berichte der Deutschen Chemischen Gesellschaft . 62 (8): 2337–2372. doi : 10.1002 / cber.19290620872 .
- Diels, O .; Alder, K. (1930). "Synthesen in der hydroaromatischen Reihe, VII". Justus Liebigs Annalen der Chemie . 478 : 137-154. doi : 10.1002 / jlac.19304780109 .
- Diels, O .; Alder, K. (1931). "Synthesen in der hydroaromatischen Reihe, VIII". Justus Liebigs Annalen der Chemie . 486 : 191-202. doi : 10.1002 / jlac.19314860110 .
- Diels, O .; Alder, K. (1931). "Synthesen in der hydroaromatischen Reihe, IX". Justus Liebigs Annalen der Chemie . 486 : 202–210. doi : 10.1002 / jlac.19314860111 .
- Diels, O .; Alder, K. (1931). "Synthesen in der hydroaromatischen Reihe, X". Justus Liebigs Annalen der Chemie . 486 : 211-225. doi : 10.1002 / jlac.19314860112 .
- Diels, O .; Alder, K. (1931). "Synthesen in der hydroaromatischen Reihe, XI". Justus Liebigs Annalen der Chemie . 490 : 236–242. doi : 10.1002 / jlac.19314900109 .
- Diels, O .; Alder, K. (1931). "Synthesen in der hydroaromatischen Reihe, XII". Justus Liebigs Annalen der Chemie . 490 : 243-257. doi : 10.1002 / jlac.19314900110 .
- Diels, O .; Alder, K. (1931). "Synthesen in der hydroaromatischen Reihe, XIII". Justus Liebigs Annalen der Chemie . 490 : 257–266. doi : 10.1002 / jlac.19314900111 .
- Diels, O .; Alder, K. (1931). "Synthesen in der hydroaromatischen Reihe, XIV". Justus Liebigs Annalen der Chemie . 490 : 267–276. doi : 10.1002 / jlac.19314900112 .
- Diels, O .; Alder, K. (1931). "Synthesen in der hydroaromatischen Reihe, XV". Justus Liebigs Annalen der Chemie . 490 : 277-294. doi : 10.1002 / jlac.19314900113 .
- Diels, O .; Alder, K. (1932). "Synthesen in der hydroaromatischen Reihe, XVI". Justus Liebigs Annalen der Chemie . 498 : 1-15. doi : 10.1002 / jlac.19324980102 .
- Diels, O .; Alder, K. (1932). "Synthesen in der hydroaromatischen Reihe, XVII". Justus Liebigs Annalen der Chemie . 498 : 16–49. doi : 10.1002 / jlac.19324980103 .
- Diels, O .; Alder, K. (1933). "Synthesen in der hydroaromatischen Reihe, XVIII". Justus Liebigs Annalen der Chemie . 505 : 103-150. doi : 10.1002 / jlac.19335050109 .
- Diels, O .; Alder, K. (1934). "Synthesen in der hydroaromatischen Reihe, XIX". Justus Liebigs Annalen der Chemie . 510 : 87-128. doi : 10.1002 / jlac.19345100106 .
- Diels, O .; Reese, J. (1934). "Synthesen in der hydroaromatischen Reihe, XX". Justus Liebigs Annalen der Chemie . 511 : 168-182. doi : 10.1002 / jlac.19345110114 .
- Diels, O .; Meyer, R. (1934). "Synthesen in der hydroaromatischen Reihe, XXI". Justus Liebigs Annalen der Chemie . 513 : 129-145. doi : 10.1002 / jlac.19345130108 .
- Diels, O .; Friedrichsen, W. (1934). "Synthesen in der hydroaromatischen Reihe, XXII". Justus Liebigs Annalen der Chemie . 513 : 145-155. doi : 10.1002 / jlac.19345130109 .
- Diels, O .; Möller, F. (1935). "Synthesen in der hydroaromatischen Reihe, XXIII". Justus Liebigs Annalen der Chemie . 516 : 45–61. doi : 10.1002 / jlac.19355160104 .
- Diels, O .; Kech, H. (1935). "Synthesen in der hydroaromatischen Reihe, XXIV". Justus Liebigs Annalen der Chemie . 519 : 140-146. doi : 10.1002 / jlac.19355190112 .
- Diels, O .; Reese, J. (1935). "Synthesen in der hydroaromatischen Reihe, XXV". Justus Liebigs Annalen der Chemie . 519 : 147-157. doi : 10.1002 / jlac.19355190113 .
- Diels, O .; Harms, J. (1935). "Synthesen in der hydroaromatischen Reihe, XXVI". Justus Liebigs Annalen der Chemie . 525 : 73–94. doi : 10.1002 / jlac.19365250107 .
- Diels, O .; Schrum, H. (1937). "Synthesen in der hydroaromatischen Reihe, XXVII". Justus Liebigs Annalen der Chemie . 530 : 68–86. doi : 10.1002 / jlac.19375300106 .
- Diels, O .; Pistor, H. (1937). "Synthesen in der hydroaromatischen Reihe, XXVIII". Justus Liebigs Annalen der Chemie . 530 : 87–98. doi : 10.1002 / jlac.19375300107 .
- ^ "El Premio Nobel de Química 1950" . La Fundación Nobel . Consultado el 19 de febrero de 2016 .
- ^ Woodward, RB; Sondheimer, F .; Taub, D .; Heusler, K .; McLamore, WM (1952). "La síntesis total de esteroides". Revista de la Sociedad Química Estadounidense . 74 (17): 4223–4251. doi : 10.1021 / ja01137a001 .
- ^ Corey, EJ; Weinshenker, NM; Schaaf, TK; Huber, W. (1969). "Síntesis estéreo controlada de prostaglandinas F-2a y E-2 (dl)". Revista de la Sociedad Química Estadounidense . 91 (20): 5675–7. doi : 10.1021 / ja01048a062 . PMID 5808505 .
- ^ Nicolaou, KC; Sorensen, EJ (1996). Clásicos en síntesis total: objetivos, estrategias, métodos . Wiley VCH . ISBN 978-3-527-29231-8.
- ^ De Lucchi, O .; Pasquato, L. (1988). "El papel de las funcionalidades del azufre en la activación y dirección de olefinas en reacciones de cicloadición". Tetraedro . 44 (22): 6755–6794. doi : 10.1016 / S0040-4020 (01) 86204-9 .
- ^ Danishefsky, S .; Hirama, M .; Fritsch, N .; Clardy, J. (1979). "Síntesis de prefenato disódico y epiprefenato disódico. Estereoquímica del ácido prefénico y una observación sobre la reordenación catalizada por bases de ácido prefénico en ácido p-hidroxifeniláctico". Revista de la Sociedad Química Estadounidense . 101 (23): 7013–7018. doi : 10.1021 / ja00517a039 .
- ^ Wender, PA; Schaus, JM; White, AW (1980). "Metodología general para la síntesis de cis-hidroisoquinolina: Síntesis de reserpina". Revista de la Sociedad Química Estadounidense . 102 (19): 6157–6159. doi : 10.1021 / ja00539a038 .
- ^ Martin, SF; Rueger, H .; Williamson, SA; Grzejszczak, S. (1987). "Estrategias generales para la síntesis de alcaloides indol. Síntesis total de (±) -reserpina y (±) -α-yohimbina". Revista de la Sociedad Química Estadounidense . 109 (20): 6124–6134. doi : 10.1021 / ja00254a036 .
- ^ Nicolaou, KC; Yang, Z .; Liu, JJ; Ueno, H .; Nantermet, PG; Guy, RK; Claiborne, CF; Renaud, J .; Couladouros, EA; Paulvannan, K .; Sorensen, EJ (1994). "Síntesis total de taxol". Naturaleza . 367 (6464): 630–4. Código bibliográfico : 1994Natur.367..630N . doi : 10.1038 / 367630a0 . PMID 7906395 . S2CID 4371975 .
- ^ Narasaka, K .; Shimada, S .; Osoda, K .; Iwasawa, N. (1991). "Ácido fenilborónico como plantilla en la reacción de Diels-Alder". Síntesis . 1991 (12): 1171-1172. doi : 10.1055 / s-1991-28413 .
- ^ Smith, AB; Sestelo, JP; Dormer, PG (1995). "Síntesis total de (-) - Furaquinocina C". Revista de la Sociedad Química Estadounidense . 117 (43): 10755–10756. doi : 10.1021 / ja00148a023 .
- ^ Kozmin, SA; Rawal, VH (1998). "Una estrategia general para los alcaloides de Aspidosperma: síntesis eficiente, estereocontrolada de tabersonina". Revista de la Sociedad Química Estadounidense . 120 (51): 13523-13524. doi : 10.1021 / ja983198k .
- ^ Gibbs, RA; Okamura, WH (1988). "Una síntesis enantioselectiva corta de (+) - esterpureno: transferencia intramolecular completa de elementos quirales centrales a axiales a centrales". Revista de la Sociedad Química Estadounidense . 110 (12): 4062–4063. doi : 10.1021 / ja00220a069 .
- ^ Charest, MG; Siegel, DR; Myers, AG (2005). "Síntesis de (-) - tetraciclina". Revista de la Sociedad Química Estadounidense . 127 (23): 8292–3. doi : 10.1021 / ja052151d . PMID 15941256 .
- ^ Dauben, WG; Kessel, CR; Takemura, KH (1980). "Síntesis total simple y eficiente de cantaridina a través de una reacción de Diels-Alder de alta presión". Revista de la Sociedad Química Estadounidense . 102 (22): 6893–6894. doi : 10.1021 / ja00542a060 .
- ^ Holmes, HL (1948). "Dienófilos etilenicos y acetilénicos de la reacción de Diels-Alder". Reacciones orgánicas . 4 . págs. 60-173. doi : 10.1002 / 0471264180.or004.02 . ISBN 978-0471264187.
- ^ Butz, LW; Rytina, AW (1949). "Las quinonas de reacción de Diels-Alder y otras ciclononas". Reacciones orgánicas . 5 . págs. 136-192. doi : 10.1002 / 0471264180.or005.03 . ISBN 978-0471264187.
- ↑ Kloetzel, MC (1948). "La reacción de Diels-Alder con anhídrido maleico". Reacciones orgánicas . 4 . págs. 1-59. doi : 10.1002 / 0471264180.or004.01 . ISBN 978-0471264187.
- ^ Heintzelman, GR; Meigh, IR; Mahajan, YR; Weinreb, SW (2005). "Reacciones de Diels-Alder de Imino Dienophiles". Reacciones orgánicas . 65 . págs. 141–599. doi : 10.1002 / 0471264180.or065.02 . ISBN 978-0471264187.
- ^ Ciganek, E. (1984). "La reacción intramolecular Diels-Alder". Reacciones orgánicas . 32 . págs. 1-374. doi : 10.1002 / 0471264180. o032.01 . ISBN 978-0471264187.
Bibliografía
- Carey, Francis A .; Sundberg, Richard J. (2007). Química orgánica avanzada: Parte B: Reacciones y síntesis (5ª ed.). Nueva York: Springer. ISBN 978-0387683546.
enlaces externos
- [2] Traducción al inglés del seminal artículo alemán de 1928 de Diels y Alder que les valió el premio Nobel. Título en inglés: 'Síntesis de la serie hidroaromática'; Título alemán "Synthesen in der hydroaromatischen Reihe".
- Cicloadiciones
- Reacciones de nombres
- Reacciones de formación de enlaces carbono-carbono
- Reacciones de formación de anillos
- Inventos alemanes
- 1928 en ciencia
- 1928 en Alemania