Ácido arsénico
El ácido arsenioso (o ácido arsenioso ) es el compuesto inorgánico con la fórmula H 3 AsO 3 . Se sabe que se encuentra en soluciones acuosas , pero no se ha aislado como material puro, aunque este hecho no resta importancia al As(OH) 3 . [2]
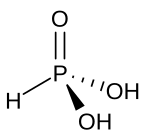
As(OH) 3 es una molécula piramidal que consta de tres grupos hidroxilo unidos al arsénico. El espectro de RMN de 1H de soluciones de ácido arsénico consta de una sola señal consistente con la alta simetría de la molécula. [3] Por el contrario, el ácido fosforoso nominalmente relacionado H 3 PO 3 adopta la estructura HPO(OH) 2 . El análogo estructural del ácido arsénico (P(OH) 3) es un componente de equilibrio muy pequeño de tales soluciones. Los diferentes comportamientos de los compuestos de As y P reflejan una tendencia en la que los estados de oxidación altos son más estables para los miembros más ligeros de los elementos del grupo principal que para sus congéneres más pesados. [4]
Un tautómero del ácido arsenoso es HAsO(OH) 2 , que se llama ácido arsónico . No ha sido aislado ni bien caracterizado.
La preparación de As(OH) 3 implica una hidrólisis lenta de trióxido de arsénico en agua. La adición de base convierte el ácido arsénico en los iones de arsenito [AsO(OH) 2 ] − , [AsO 2 (OH)] 2− y [AsO 3 ] 3− .
Siendo su primera p K a 9,2, el As(OH) 3 es un ácido débil. [4] Las reacciones atribuidas al trióxido de arsénico acuoso se deben al ácido arsénico y sus bases conjugadas.
Al igual que el trióxido de arsénico, el ácido arsénico a veces es anfótero . Por ejemplo, reacciona con los ácidos clorhídrico, bromhídrico y yodhídrico para producir tricloruro, tribromuro y triyoduro de arsénico.