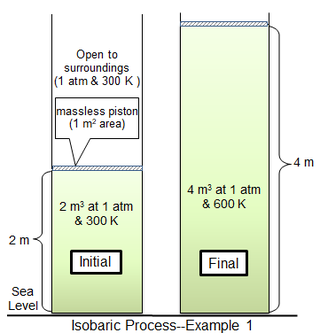
Proceso isobárico
En termodinámica , un proceso isobárico es un tipo de proceso termodinámico en el que la presión del sistema permanece constante: Δ P = 0. El calor transferido al sistema realiza trabajo , pero también cambia la energía interna ( U ) del sistema. Este artículo utiliza la convención de signos de la física para el trabajo, donde el trabajo positivo es el trabajo realizado por el sistema . Usando esta convención, por la primera ley de la termodinámica ,
donde W es trabajo, U es energía interna y Q es calor. [1] El trabajo de presión - volumen del sistema cerrado se define como:
donde Δ significa cambio durante todo el proceso, mientras que d denota un diferencial. Como la presión es constante, esto significa que
donde R representa la constante de los gases y n representa la cantidad de sustancia , que se supone que permanece constante (p. ej., no hay transición de fase durante una reacción química ). De acuerdo con el teorema de equipartición , [2] el cambio en la energía interna está relacionado con la temperatura del sistema por
Para encontrar la capacidad calorífica específica molar del gas involucrado, las siguientes ecuaciones se aplican a cualquier gas general que sea calóricamente perfecto. La propiedad γ se denomina índice adiabático o relación de capacidad calorífica . Algunas fuentes publicadas pueden usar k en lugar de γ .
Los valores de γ son γ = 7/5 para gases diatómicos como el aire y sus componentes principales , y γ = 5/3 para gases monoatómicos como los gases nobles . Las fórmulas para los calores específicos se reducirían en estos casos especiales: