Dióxido de plomo
El óxido de plomo (IV) es el compuesto inorgánico con la fórmula PbO 2 . Es un óxido donde el plomo se encuentra en un estado de oxidación de +4. [1] Es un sólido de color marrón oscuro que es insoluble en agua. [2] Existe en dos formas cristalinas. Tiene varias aplicaciones importantes en electroquímica , en particular como placa positiva de baterías de plomo ácido .
El dióxido de plomo tiene dos polimorfos principales, alfa y beta, que ocurren naturalmente como minerales raros escrutinyita y plattnerita , respectivamente. Mientras que la forma beta se identificó en 1845, [3] el α-PbO 2 se identificó por primera vez en 1946 y se encontró como un mineral natural en 1988. [4]
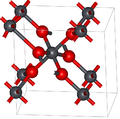
La forma alfa tiene simetría ortorrómbica , grupo espacial Pbcn (No. 60), símbolo de Pearson oP 12, constantes de red a = 0,497 nm, b = 0,596 nm, c = 0,544 nm, Z = 4 (cuatro unidades de fórmula por celda unitaria). [4] Los átomos de plomo tienen seis coordenadas.
La simetría de la forma beta es tetragonal , grupo espacial P4 2 /mnm (No. 136), símbolo de Pearson tP 6, constantes de red a = 0.491 nm, c = 0.3385 nm, Z = 2 [5] y relacionado con la estructura del rutilo y se puede considerar que contiene columnas de octaedros que comparten bordes opuestos y se unen a otras cadenas por esquinas. Esto contrasta con la forma alfa donde los octaedros están unidos por bordes adyacentes para dar cadenas en zigzag. [4]
La estequiometría del producto final se puede controlar cambiando la temperatura; por ejemplo, en la reacción anterior, el primer paso ocurre a 290 °C, el segundo a 350 °C, el tercero a 375 °C y el cuarto a 600 °C. Además, el Pb 2 O 3 se puede obtener descomponiendo el PbO 2 a 580–620 °C bajo una presión de oxígeno de 1400 atm (140 MPa). Por lo tanto, la descomposición térmica del dióxido de plomo es una forma común de producir varios óxidos de plomo. [6]
El dióxido de plomo es un compuesto anfótero con propiedades ácidas predominantes. Se disuelve en bases fuertes para formar el ion hidroxi plumbato , [Pb(OH) 6 ] 2− : [2]