Acetiluro
Acetiluro se refiere a compuestos químicos con las fórmulas químicas MC≡CH y MC≡CM, donde M es un metal. [1] El término se usa libremente y puede referirse a acetiluros sustituidos que tienen la estructura general RC≡CM (donde R es una cadena lateral orgánica ). Los acetiluros son reactivos en síntesis orgánica . El acetiluro de calcio comúnmente llamado carburo de calcio es un compuesto comercial importante.
Estructura y vinculación
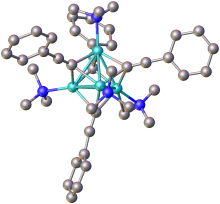
Los acetiluros de metales alcalinos y alcalinotérreos de fórmula general MC≡CM son compuestos de fase de Zintl similares a sal , que contienen C2−
2iones. La evidencia de este carácter iónico se puede ver en la rápida hidrólisis de estos compuestos para formar acetileno y óxidos metálicos, también hay alguna evidencia de la solubilidad de C2−
2iones en amoníaco líquido. [3] La C2−
2ion tiene un estado fundamental de capa cerrada de 1 Σ+
g, haciéndolo isoelectrónico a una molécula neutra N 2 , [4] lo que puede proporcionarle cierta estabilidad.
Los acetiluros análogos preparados a partir de otros metales, particularmente metales de transición , muestran un carácter covalente y están asociados invariablemente con sus centros metálicos. Esto se puede ver en su estabilidad general al agua (es decir , acetiluro de plata , acetiluro de cobre ) y aplicaciones químicas radicalmente diferentes.
Los acetiluros de fórmula general RC≡CM (donde R = H o alquilo) muestran generalmente propiedades similares a sus análogos doblemente sustituidos. En ausencia de ligandos adicionales, los acetiluros metálicos adoptan estructuras poliméricas en las que los grupos acetiluro son ligandos puente .
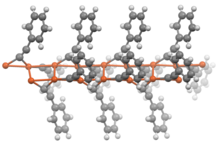
Preparación
Los alquinos terminales son ácidos débiles : [6]
- RC≡CH + R ″ M ⇌ R ″ H + RC≡CM
La generación de acetiluros a partir de acetileno y alquinos se basa en el uso de superbases organometálicas [7] o inorgánicas [8] en disolventes que son menos ácidos que el alquino terminal. En los primeros estudios se empleó amoníaco líquido , pero los disolventes etéreos son más comunes.
La amida de litio , [6] LiHMDS , [9] o reactivos de organolitio , como butillitio , [7] se utilizan con frecuencia para formar acetiluros de litio:
Los acetiluros de sodio o potasio se pueden preparar a partir de diversos reactivos inorgánicos (por ejemplo, amida de sodio ) [8] o de sus metales elementales, a menudo a temperatura ambiente y presión atmosférica. [6]
El acetiluro de cobre (I) se puede preparar pasando acetileno a través de una solución acuosa de cloruro de cobre (I) debido a un equilibrio de baja solubilidad . [6] De manera similar, los acetiluros de plata se pueden obtener a partir del nitrato de plata .
El carburo de calcio se prepara calentando carbón con cal CaO a aproximadamente 2000 ° C. Se utiliza un proceso similar para producir carburo de litio .
Reacciones
Los acetiluros del tipo RC 2 M se utilizan ampliamente en alquinilaciones en química orgánica . Son nucleófilos que se agregan a una variedad de sustratos electrófilos e insaturados. Una aplicación clásica es la reacción de Favorskii .
Es ilustrativa la secuencia que se muestra a continuación, el propiolato de etilo se desprotona con n- butillitio para dar el acetiluro correspondiente. Este acetiluro se suma al centro carbonilo de ciclopentanona . El tratamiento hidrolítico libera el alcohol alquinílico. [10]
Reacciones de acoplamiento
A veces, los acetiluros son productos intermedios en las reacciones de acoplamiento . Los ejemplos incluyen el acoplamiento Sonogashira , el acoplamiento Cadiot-Chodkiewicz , el acoplamiento Glaser y el acoplamiento Eglinton .
Riesgos
Algunos acetiluros son notoriamente explosivos. [11] La formación de acetiluros plantea un riesgo en la manipulación de acetileno gaseoso en presencia de metales como mercurio , plata o cobre , o aleaciones con su alto contenido ( latón , bronce , soldadura de plata ).
Ver también
- Etinilo
- Radical etinilo
- Carbono diatómico (C 2 neutro )
- Acetilendiol
Referencias
- ^ IUPAC , Compendio de terminología química , 2ª ed. (el "Libro de oro") (1997). Versión corregida en línea: (2006–) " acetylides ". doi : 10.1351 / goldbook.A00067
- ^ Schubert, Bernd; Weiss, Erwin (1983). "(PHCCLi) 4 (tmhda) 2 , un compuesto de organolitio polimérico con unidades estructurales cúbicas de Li 4 C 4 ". Angewandte Chemie International Edition en inglés . 22 (6): 496–497. doi : 10.1002 / anie.198304961 .
- ^ Hamberger, Markus; Liebig, Stefan; Friedrich, Ute; Korber, Nikolaus; Ruschewitz, Uwe (21 de diciembre de 2012). "Evidencia de solubilidad del ion acetiluro C2−
2: Síntesis y estructuras cristalinas de K 2 C 2 · 2 NH 3 , Rb 2 C 2 · 2 NH 3 y Cs 2 C 2 · 7 NH 3 ". Angewandte Chemie International Edition . 51 (52): 13006-13010. Doi : 10.1002 / anie.201206349 . PMID 23161511 . - ↑ Sommerfeld, T .; Riss, U .; Meyer, H.-D .; Cederbaum, L. (agosto de 1997). "Metaestable C2−
2Dianion ". Physical Review Letters . 79 (7): 1237-1240. Bibcode : 1997PhRvL..79.1237S . Doi : 10.1103 / PhysRevLett.79.1237 . - ^ Chui, Stephen SY; Ng, Miro FY; Che, Chi-Ming (2005). "Determinación de la estructura de polímeros de coordinación de Aril / Alquiletinilo Homoleptic AuI, AgI y CuI por Difracción de Polvo de Rayos X". Química: una revista europea . 11 (6): 1739-1749. doi : 10.1002 / quím.200400881 . PMID 15669067 .
- ↑ a b c d Viehe, Heinz Günter (1969). "Química de los acetilenos". Angewandte Chemie (1ª ed.). Nueva York: Marcel Dekker, inc. 84 (8): 170–179 y 225–241. doi : 10.1002 / ange.19720840843 .
- ^ a b Midland, MM; McLoughlin, JI; Werley, Ralph T., Jr. (1990). "Preparación y uso de acetiluro de litio: 1-metil-2-etinil- endo -3,3-dimetil-2-norbornanol". Síntesis orgánicas . 68 : 14. doi : 10.15227 / orgsyn.068.0014 .
- ↑ a b Coffman, Donald D. (1940). "Dimetiletilinilcarbinol". Síntesis orgánicas . 40 : 20. doi : 10.15227 / orgsyn.020.0040 .
- ^ Reich, Melanie (24 de agosto de 2001). "Adición de un acetiluro de litio a un aldehído; 1- (2-pentin-4-ol) -ciclopent-2-en-1-ol". Páginas sintéticas de ChemSpider (conjunto de datos): 137. doi : 10.1039 / SP137 .
- ^ Midland, M. Mark; Tramontano, Alfonso; Cable, John R. (1980). "Síntesis de 4-hidroxi-2-alquinoatos de alquilo". La Revista de Química Orgánica . 45 (1): 28-29. doi : 10.1021 / jo01289a006 .
- ^ Cataldo, Franco; Casari, Carlo S. (2007). "Síntesis, Estructura y Propiedades Térmicas de Polinuros y Acetiluros de Cobre y Plata". Revista de polímeros y materiales inorgánicos y organometálicos . 17 (4): 641–651. doi : 10.1007 / s10904-007-9150-3 . ISSN 1574-1443 . S2CID 96278932 .
- Aniones
- Grupos funcionales
- Acetiluros
![{\ displaystyle {\ ce {{HC \! {\ equiv} \! CH} + {\ overset {butil litio} {BuLi}} -> [{\ ce {THF}}] [- 78 ^ {\ circ} { \ ce {C}}] {Li - \! {\ equiv} \! - H} + BuH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ae261811e4519409e7516a7a6c4576ec44871845)