polaridad química
En química , la polaridad es una separación de la carga eléctrica que conduce a que una molécula o sus grupos químicos tengan un momento dipolar eléctrico , con un extremo con carga negativa y un extremo con carga positiva.
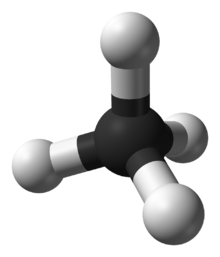
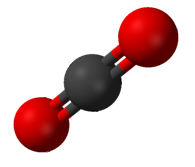
Las moléculas polares deben contener uno o más enlaces polares debido a la diferencia de electronegatividad entre los átomos enlazados. Las moléculas que contienen enlaces polares no tienen polaridad molecular si los dipolos de enlace se anulan entre sí por simetría.
Las moléculas polares interactúan a través de fuerzas intermoleculares dipolo-dipolo y enlaces de hidrógeno . La polaridad es la base de una serie de propiedades físicas, incluida la tensión superficial , la solubilidad y los puntos de fusión y ebullición.
No todos los átomos atraen electrones con la misma fuerza. La cantidad de "atracción" que un átomo ejerce sobre sus electrones se denomina electronegatividad . Los átomos con electronegatividades altas, como el flúor , el oxígeno y el nitrógeno , ejercen una mayor atracción sobre los electrones que los átomos con electronegatividades más bajas, como los metales alcalinos y los metales alcalinotérreos . En un enlace, esto conduce a una distribución desigual de electrones entre los átomos, ya que los electrones se acercarán al átomo con mayor electronegatividad.
Debido a que los electrones tienen una carga negativa, la distribución desigual de electrones dentro de un enlace conduce a la formación de un dipolo eléctrico : una separación de carga eléctrica positiva y negativa. Debido a que la cantidad de carga separada en tales dipolos suele ser menor que una carga fundamental , se denominan cargas parciales , indicadas como δ+ ( delta más) y δ− (delta menos). Estos símbolos fueron introducidos por Sir Christopher Ingold y la Dra. Edith Hilda (Usherwood) Ingold en 1926. [1] [2] El momento dipolar de enlace se calcula multiplicando la cantidad de carga separada y la distancia entre las cargas.
Estos dipolos dentro de las moléculas pueden interactuar con dipolos en otras moléculas, creando fuerzas intermoleculares dipolo-dipolo .