 | |
| Nombres | |
|---|---|
| Nombre IUPAC Cloruro de americio (III) | |
| Nombre IUPAC sistemático Cloruro de americio (3+) | |
| Otros nombres Cloruro de americio Tricloruro de americio | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Propiedades | |
| Soy Cl 3 | |
| Masa molar | 349 g · mol −1 |
| Apariencia | Cristales opacos de color rojo claro |
| Densidad | 5,87 g cm −3 [1] |
| Punto de fusion | 715 ° C (1319 ° F; 988 K) [2] |
| Punto de ebullición | 850 ° C (1.560 ° F; 1.120 K) [1] |
| Estructura | |
| hexagonal ( UCl 3 tipo ), HP8 | |
| P6 3 / m, No. 176 | |
| Prismático trigonal tricapado (nueve coordenadas) | |
| Compuestos relacionados | |
Otros cationes | Cloruro de europio (III) |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
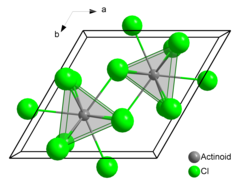
El cloruro de americio (III) o tricloruro de americio es el compuesto químico compuesto de americio y cloro con la fórmula AmCl 3 . Forma cristales hexagonales rosados . En el estado sólido, cada átomo de americio tiene nueve átomos de cloro como vecinos cercanos, aproximadamente a la misma distancia, en una configuración prismática trigonal tricapada. [3] [4]
El hexahidrato tiene una estructura cristalina de monoclina con: a = 970,2 pm, b = 656,7 pm yc = 800,9 pm; β = 93 ° 37 '; grupo espacial: P 2 / n . [5]
Reacciones [ editar ]
Se ha investigado un método de electrorrefinación con cloruro de americio (III) para separar mezclas de actínidos , ya que la energía libre de Gibbs estándar de formación de cloruro de americio (III) es muy diferente del resto de los cloruros de actínidos. [6] Esto se puede utilizar para eliminar el americio del plutonio fundiendo la mezcla cruda junto con sales como el cloruro de sodio . [7]
Referencias [ editar ]
- ^ a b "Química: tabla periódica: americio: datos compuestos (cloruro de americio (III))" . WebElements . Consultado el 24 de junio de 2008 .
- ^ Perry, Dale L .; Phillips, Sidney L. (1995), Manual de compuestos inorgánicos , CRC Press, pág. 15, ISBN 0-8493-8671-3, consultado el 25 de junio de 2008
- ^ LB Asprey, TK Keenan, FH Kruse: "Estructuras cristalinas de los trifluoruros, tricloruros, tribromuros y triyoduros de americio y curio", Inorg. Chem. 1965 , 4 (7) , 985–986; doi : 10.1021 / ic50029a013 .
- ^ AF Wells: Química inorgánica estructural quinta edición (1984) Publicaciones de la ciencia de Oxford, ISBN 0-19-855370-6 .
- ^ John H. Burns, Joseph Richard Peterson: "Las estructuras cristalinas de tricloruro de americio hexahidrato y tricloruro de berkelio hexahidrato", Inorg. Chem. 1971 , 10 (1) , 147-151; doi : 10.1021 / ic50095a029 .
- ^ Agencia de energía nuclear (2001), Actas del taller sobre separaciones piroquímicas , Aviñón, Francia: Publicaciones de la OCDE, págs. 276–277, ISBN 92-64-18443-0, consultado el 24 de junio de 2008
- ^ Procesamiento de plutonio en el complejo de armas nucleares , Diane Publishing, 1992, p. 21, ISBN 1-56806-568-X, consultado el 24 de junio de 2008