Anti-periplanar
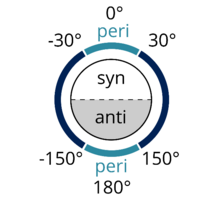
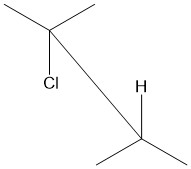
En química orgánica, anti-periplanar o antiperiplanar , describe el ángulo de enlace A–B–C–D en una molécula. En este confórmero, el ángulo diedro del enlace A–B y el enlace C–D es mayor a +150° o menor a −150° [1] (Figuras 1 y 2 ). Anti-periplanar se usa a menudo en los libros de texto para referirse estrictamente a anti-coplanar, [2] con un ángulo diedro AB CD de 180° (Figura 3). En una proyección de Newman, la molécula estará en una disposición escalonada con los grupos funcionales antiperiplanares apuntando hacia arriba y hacia abajo, separados 180° entre sí (ver Figura 4). La Figura 5 muestra 2-cloro-2,3-dimetilbutano en una proyección de caballete con cloro e hidrógeno anti-periplanar entre sí.
Syn- periplanar o synperiplanar es similar a anti-periplanar. En el confórmero sin-periplanar, A y D están en el mismo lado del plano del enlace, con el ángulo diedro de A–B y C–D entre +30° y −30° (ver Figura 2).
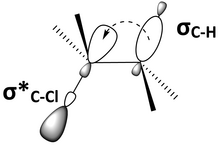
Un factor importante en el confórmero antiperiplanar es la interacción entre los orbitales moleculares. La geometría anti-periplanar pondrá un orbital de enlace y un orbital anti-enlazante aproximadamente paralelos entre sí, o syn-periplanar. La Figura 6 es otra representación del 2-cloro-2,3-dimetilbutano (Figura 5), que muestra el orbital de enlace C–H, σ C–H , y el orbital de antienlace C–Cl, σ* C–Cl , syn -periplanar. Los orbitales paralelos pueden superponerse y participar en la hiperconjugación.. Si el orbital enlazante es un donante de electrones y el orbital antienlazante es un aceptor de electrones, entonces el orbital enlazante podrá donar electronegatividad al orbital antienlazante. Esta interacción donante-aceptor lleno a vacío tiene un efecto estabilizador general sobre la molécula. Sin embargo, la donación de un orbital enlazante a un orbital antienlazante también resultará en el debilitamiento de ambos enlaces. En la Figura 6, el 2-cloro-2,3-dimetilbutano se estabiliza a través de la hiperconjugación de la donación de electrones de σ C-H a σ* C-Cl , pero los enlaces C-H y C-Cl están debilitados. Un diagrama de orbitales moleculares muestra que la mezcla de σ C–H y σ* C–Cl en 2-cloro-2,3-dimetilbutano reduce la energía de ambos orbitales (Figura 7).
Se producirá una reacción de eliminación bimolecular en una molécula en la que el enlace carbono-hidrógeno que se rompe y el grupo saliente son antiperiplanares [4] [5] [6] [7] (Figura 8). Se prefiere esta geometría porque alinea los orbitales σ C-H y σ* CX . [8] [9] La figura 9 muestra el orbital σ C-H y el orbital σ* CX paralelos entre sí, lo que permite que el orbital σ C-H se done al orbital antienlazante σ* CX a través de la hiperconjugación. Esto sirve para debilitar los enlaces CH y CX, los cuales se rompen en un E 2reacción. También configura la molécula para mover más fácilmente sus electrones σ C-H a un orbital π C-C (Figura 10).
En el reordenamiento de pinacol , un grupo metilo se encuentra anti-periplanar a un grupo funcional de alcohol activado. [10] [11] Esto coloca el orbital σ C–C del grupo metilo en paralelo con el orbital σ* C–O del alcohol activado. Antes de que el alcohol activado se vaya como H 2 O, el orbital de enlace metilo se dona al orbital de antienlace C–O, debilitando ambos enlaces. Esta hiperconjugación facilita el cambio de 1,2-metilo que se produce para eliminar el agua. Vea la Figura 11 para el mecanismo.
El término antiperiplanar fue acuñado por primera vez por Klyne y Prelog en su trabajo titulado "Descripción de relaciones estéricas a través de enlaces simples", publicado en 1960. [12] 'Anti' se refiere a los dos grupos funcionales que se encuentran en lados opuestos del plano de el vínculo. 'Peri' proviene de la palabra griega para 'cerca', por lo que periplanar significa "aproximadamente plano". [13] En su artículo “¿Periplanar o Coplanar?” Kane y Hersh señalan que muchos libros de texto orgánicos usan anti-periplanar para referirse a completamente anti-planar o anticoplanar, lo cual es técnicamente incorrecto. [14]