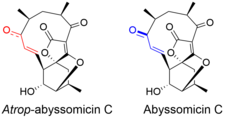
Atrop-abissomicina C
La atrop- abisomicina C es un producto natural de tipo policétido policíclico que es el atropisómero de la abisomicina C. Es un espirotetronato que pertenece a la clase de antibióticos tetronatos , que incluye compuestos como la tetronomicina , la aglomerina y la clorotricina . [1] En 2006, el grupo de Nicolaou descubrió atrop -abisomicin C mientras trabajaba en la síntesis total de abyssomicina C. [2] Luego, en 2007, Süssmuth y sus colaboradores aislaron atrop -abisomicin C de Verrucosispora marisAB-18-032, un actinomiceto marino encontrado en sedimentos del mar japonés. Descubrieron que la atrop- abisomicina C era el metabolito principal producido por esta cepa, mientras que la abisomicina C era un producto menor. La molécula muestra actividad antibacteriana al inhibir la enzima PabB ( 4-amino-4-desoxicorismato sintasa ), lo que agota la biosíntesis de p -aminobenzoato . [3] [4]
Atrop -abyssomicina C tiene una topografía estructural compleja pero intrigante. El compuesto contiene un sistema de oxabiciclo[2.2.2]octano fusionado con el resto tetronato. El anillo macrocíclico de 11 miembros lleva una cetona α, β-insaturada que se propuso como centro reactivo. [5] A pesar de ser un macrociclo tenso, existe un atropisómero , la abisomicina C. El atropisomerismo surge debido a una desviación estructural en la región de cetona α, β-insaturada de la molécula. La orientación del carbonilo en atrop -abismicina C es cisoide, mientras que la conformación en abisomicina C es transoide. [6] La fracción enona de atrop-abisomicin C tiene un mayor grado de conjugación, lo que lo convierte en un aceptor de Michael más activo. [7]
La biosíntesis de atrop- abisomicin C comienza con la síntesis de una cadena de policétido lineal en un sistema PKS I que consta de un módulo de carga y seis módulos de extensión. La cadena de policétido está formada por cinco acetatos, dos propionatos y el metabolito de la vía glucolítica. El D-1,3-bisfosfoglicerato, el metabolito glucolítico, es transferido a AbyA3 (una proteína transportadora de acilo) por AbyA2 para generar el gliceril-ACP. AbyA1 facilita la unión del gliceril-ACP a la cadena de policétido y la separación del policétido de la policétido sintasa para formar el intermediario 2 . [7] [8] [9]
Con base en la observación realizada para la biosíntesis de aglomerina, se ha propuesto que AbyA4 acetila el intermedio 2 y AbyA5 cataliza la eliminación de ácido acético para formar el doble enlace exocíclico en el intermedio 4 . [1] Se propuso que tuviera lugar un Diels-Alder intramolecular entre la olefina exocíclica y el dieno conjugado en el extremo de la cola del policétido para formar el anillo macrocíclico. [7] Se ha informado que el gen Abycyc previamente no identificado podría codificar una enzima que lleva a cabo la cicloadición de Diels-Alder. [10] Después de la reacción de Diels-Alder, se forma un anillo de epóxido y luego se abre por el grupo hidroxilo de tetronato para formar atrop-abisomicin C. Se ha postulado que la monooxigenasa AbyE cataliza la formación de epóxido. [8]