Anhídrido carbónico
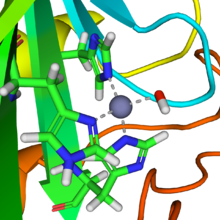
Las anhidrasas carbónicas (o carbonato deshidratasas ) forman una familia de enzimas que catalizan la interconversión entre el dióxido de carbono y el agua y los iones disociados de ácido carbónico (es decir, iones bicarbonato e hidrógeno ). [1] El sitio activo de la mayoría de las anhidrasas carbónicas contiene un ion zinc . Por tanto, se clasifican como metaloenzimas . La enzima mantiene el equilibrio ácido-base y ayuda a transportar el dióxido de carbono. [2]
La anhidrasa carbónica ayuda a mantener la homeostasis ácido-base , regula el pH y el equilibrio de líquidos. Dependiendo de su ubicación, la función de la enzima cambia ligeramente. Por ejemplo, la anhidrasa carbónica produce ácido en el revestimiento del estómago. En el riñón, el control de los iones de bicarbonato influye en el contenido de agua de la célula. El control de los iones de bicarbonato también influye en el contenido de agua en los ojos. Los inhibidores de la anhidrasa carbónica se utilizan para tratar el glaucoma, la acumulación excesiva de agua en los ojos. El bloqueo de esta enzima cambia el equilibrio de líquidos en los ojos del paciente para reducir la acumulación de líquido, aliviando así la presión. [2] [3]
El efecto Bohr es una forma de describir la afinidad de unión al oxígeno de la hemoglobina. El efecto Bohr fue descrito por Christian Bohr en el año 1904, y se refiere a un cambio en una curva de disociación del oxígeno que es causado por un cambio en la concentración de dióxido de carbono o un cambio en el pH. Esencialmente, un aumento en el dióxido de carbono da como resultado un pH sanguíneo más bajo, lo que reduce la unión de oxígeno-hemoglobina. [4] Lo contrario es cierto cuando una disminución en la concentración de dióxido de carbono aumenta el pH de la sangre, lo que aumenta la tasa de unión de oxígeno-hemoglobina. Relacionar el efecto Bohr con la anhidrasa carbónica es simple: la anhidrasa carbónica acelera la reacción del dióxido de carbono que reacciona con el agua para producir iones de hidrógeno (protones) e iones de bicarbonato.
Para describir el equilibrio en la reacción de la anhidrasa carbónica, se utiliza el principio de Le Chatelier. Los tejidos son más ácidos que los pulmones porque el dióxido de carbono se produce por la respiración celular y reacciona con el agua en los tejidos para producir los protones de hidrógeno. Debido a que la concentración de dióxido de carbono es mayor, el equilibrio se desplaza hacia la derecha, hacia el lado del bicarbonato. Lo contrario se ve en los pulmones donde se libera dióxido de carbono, por lo que su concentración es menor, por lo que el equilibrio se desplaza hacia la izquierda hacia el dióxido de carbono para intentar aumentar su concentración. [5]
Una enzima es una sustancia que actúa como catalizador en los organismos vivos y ayuda a acelerar las reacciones químicas. [6] La anhidrasa carbónica es una enzima importante que se encuentra en los glóbulos rojos, la mucosa gástrica, las células pancreáticas e incluso los túbulos renales. Fue descubierto en el año 1932 y se ha categorizado en tres clases generales. [7] La clase uno es la anhidrasa carbónica alfa que se encuentra en los mamíferos, la clase dos es la anhidrasa carbónica beta que se encuentra en bacterias y plantas y, por último, la clase tres es la anhidrasa carbónica gamma que se encuentra en las bacterias metanógenas en las aguas termales. [8]Las tres clases de anhidrasa carbónica tienen todas el mismo sitio activo con un centro de metal Zn; sin embargo, no son estructuralmente similares entre sí. El papel principal de la anhidrasa carbónica en los seres humanos es catalizar la conversión de dióxido de carbono en ácido carbónico y viceversa. Sin embargo, también puede ayudar con el transporte de CO 2 en la sangre, lo que a su vez ayuda a la respiración. Incluso puede funcionar en la formación de ácido clorhídrico por el estómago. [6] Por lo tanto, el papel de la anhidrasa carbónica depende de dónde se encuentre en el cuerpo.