Catalizador de Grubbs
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC Benciliden-bis (triciclohexilfosfino) -diclororutenio | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| |
| Propiedades | |
| C 43 H 72 Cl 2 P 2 Ru | |
| Masa molar | 822,97 g · mol −1 |
| Apariencia | Sólido púrpura |
| Punto de fusion | 153 ° C (307 ° F; 426 K) (descomposición) |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC [1,3-bis- (2,4,6-trimetilfenil) -2-imidazolidiniliden] dicloro (fenilmetileno) (triciclohexilfosfino) rutenio | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Propiedades | |
| C 46 H 65 Cl 2 N 2 P Ru | |
| Masa molar | 848,98 g · mol −1 |
| Apariencia | Sólido marrón rosáceo |
| Punto de fusion | 143,5 a 148,5 ° C (290,3 a 299,3 ° F; 416,6 a 421,6 K) |
| Riesgos | |
| Pictogramas GHS |  |
| Palabra de señal GHS | Advertencia |
| H228 | |
| P210 , P240 , P241 , P280 , P378 | |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
 | |
 | |
| Nombres | |
|---|---|
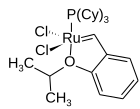
| Nombre IUPAC Dicloro ( o -isopropoxifenilmetileno) (triciclohexilfosfina) rutenio (II) | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) |
|
| ChemSpider |
|
PubChem CID |
|
InChI
| |
Sonrisas
| |
| Propiedades | |
Fórmula química | C 28 H 45 Cl 2 O P Ru |
| Masa molar | 600,61 g · mol −1 |
| Apariencia | Sólido marrón |
| Punto de fusion | 195 a 197 ° C (383 a 387 ° F; 468 a 470 K) |
| Riesgos | |
| Pictogramas GHS | |
| Palabra de señal GHS | Advertencia |
Declaraciones de peligro GHS | H228 |
Consejos de prudencia del SGA | P210 , P240 , P241 , P280 , P378 |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
| Nombres | |
|---|---|
| Nombre IUPAC [1,3-Bis- (2,4,6-trimetilfenil) -2-imidazolidiniliden] dicloro ( o -isopropoxifenilmetilen) rutenio | |
| Identificadores | |
Número CAS |
|
Modelo 3D ( JSmol ) |
|
| ChemSpider |
|
| Número CE |
|
PubChem CID |
|
InChI
| |
Sonrisas
| |
| Propiedades | |
Fórmula química | C 31 H 38 Cl 2 N 2 O Ru |
| Masa molar | 626,63 g · mol −1 |
| Apariencia | Verde sólido |
| Punto de fusion | 216 a 220 ° C (421 a 428 ° F; 489 a 493 K) |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
Los catalizadores de Grubbs son una serie de complejos de carbeno de metales de transición utilizados como catalizadores para la metátesis de olefinas . Llevan el nombre de Robert H. Grubbs , el químico que supervisó su síntesis. Se han desarrollado varias generaciones del catalizador . [1] [2] Los catalizadores de Grubbs toleran muchos grupos funcionales en los sustratos de alqueno , son tolerantes al aire y son compatibles con una amplia gama de disolventes. [3] [4] Por estas razones, los catalizadores de Grubbs se han vuelto populares en la química orgánica sintética . [5] Grubbs, junto conRichard R. Schrock e Yves Chauvin , ganaron el Premio Nobel de Química en reconocimiento a sus contribuciones al desarrollo de la metátesis de olefinas.
Catalizador de primera generación
En la década de 1960, se descubrió que el tricloruro de rutenio catalizaba la metátesis de olefinas. Los procesos se comercializaron en base a estos descubrimientos. Estos catalizadores homogéneos mal definidos pero altamente activos permanecen en uso industrial. [6] El primer catalizador de rutenio bien definido se informó en 1992. [7] Se preparó a partir de RuCl 2 (PPh 3 ) 4 y difenilciclopropeno.
Este catalizador de rutenio inicial fue seguido en 1995 por lo que ahora se conoce como el catalizador de Grubbs de primera generación. Se sintetiza a partir de RuCl 2 (PPh 3 ) 3 , fenildiazometano y triciclohexilfosfina en una síntesis de un solo recipiente . [8] [9]
El catalizador de Grubbs de primera generación fue el primer catalizador basado en Ru bien definido. También es importante como precursor de todos los demás catalizadores de tipo Grubbs.
Catalizador de segunda generación
El catalizador de segunda generación tiene los mismos usos en síntesis orgánica que el catalizador de primera generación, pero generalmente con mayor actividad. Este catalizador es estable frente a la humedad y el aire , por lo que es más fácil de manipular en el laboratorio.
Poco antes del descubrimiento del catalizador de Grubbs de segunda generación, un catalizador muy similar basado en una insaturado N se informó de carbeno heterocíclico (1,3-bis (2,4,6-trimetilfenil) imidazol) independientemente por Nolan [10] y Grubbs [11] en marzo de 1999 y por Fürstner [12] en junio del mismo año. Poco después, en agosto de 1999, Grubbs informó sobre el catalizador de segunda generación, basado en un carbeno N- heterocíclico saturado ( 1,3-bis (2,4,6-trimetilfenil) dihidroimidazol ): [13]
Tanto en los casos saturados como insaturados, un ligando de fosfina se reemplaza con un carbeno N -heterocíclico (NHC), que es característico de todos los catalizadores de tipo de segunda generación. [3]
Tanto los catalizadores de primera como de segunda generación están disponibles comercialmente, junto con muchos derivados del catalizador de segunda generación.
Catalizadores Hoveyda-Grubbs
En los catalizadores Hoveyda-Grubbs , los ligandos de bencilideno tienen un grupo orto- isopropoxi quelante unido a los anillos de benceno. El resto de orto- isopropoxibencilideno se denomina a veces quelato de Hoveyda. El átomo de oxígeno quelante reemplaza a un ligando de fosfina , que en el caso del catalizador de segunda generación, da una estructura completamente libre de fosfina. El catalizador Hoveyda-Grubbs de primera generación fue informado en 1999 por el grupo de Amir H. Hoveyda , [14] y al año siguiente, el catalizador Hoveyda-Grubbs de segunda generación fue descrito en publicaciones casi simultáneas por Blechert [15] y Laboratorios Hoveyda [16] .El nombre de Siegfried Blechert no se incluye comúnmente en el nombre del catalizador epónimo. Los catalizadores de Hoveyda-Grubbs, aunque son más caros y más lentos de iniciar que el catalizador de Grubbs del que se derivan, son populares debido a su estabilidad mejorada. [3] Al cambiar las propiedades estéricas y electrónicas del quelato, se puede modular la velocidad de iniciación del catalizador, [17] [18] como en los catalizadores Zhan . Los catalizadores Hoveyda-Grubbs se forman fácilmente a partir del catalizador de Grubbs correspondiente mediante la adición del ligando quelante y el uso de un eliminador de fosfina como el cloruro de cobre (I) : [16]
Los catalizadores Hoveyda-Grubbs de segunda generación también se pueden preparar a partir del catalizador Hoveyda-Grubbs de primera generación mediante la adición del NHC: [15]
En un estudio, se prepara un catalizador de Grubbs soluble en agua uniendo una cadena de polietilenglicol al grupo imidazolidina . [19] Este catalizador se usa en la reacción de metátesis de cierre de anillo en agua de un dieno que lleva un grupo de sal de amonio que lo hace soluble en agua también.
Catalizador Grubbs de tercera generación (catalizadores de inicio rápido)
La velocidad del catalizador de Grubbs se puede alterar reemplazando el ligando de fosfina con ligandos de piridina más lábiles . Al usar 3-bromopiridina, la tasa de iniciación aumenta más de un millón de veces. [20] Tanto la piridina como la 3-bromopiridina se utilizan comúnmente, y la versión de bromo es 4,8 veces más lábil, lo que da como resultado tasas aún más rápidas. [21] El catalizador se aísla tradicionalmente como un complejo de dos piridinas, sin embargo, una piridina se pierde al disolverse e inhibe reversiblemente el centro de rutenio a lo largo de cualquier reacción química.
La aplicación principal de los catalizadores de iniciación rápida es como iniciadores para la polimerización por metátesis por apertura de anillo (ROMP). Debido a su utilidad en ROMP, estos catalizadores a veces se denominan catalizadores de Grubbs de tercera generación. [22] La alta relación entre la tasa de iniciación y la tasa de propagación hace que estos catalizadores sean útiles en la polimerización viva , produciendo polímeros con baja polidispersidad . [23]
Aplicaciones
Los catalizadores de Grubbs son de interés para la metátesis de olefinas . Se aplica principalmente a la síntesis química fina. Las aplicaciones comerciales a gran escala de la metátesis de olefinas casi siempre emplean catalizadores heterogéneos o sistemas mal definidos basados en tricloruro de rutenio. [6]
Referencias
- ^ Grubbs, Robert H. (2003). Manual de metátesis (1ª ed.). Weinheim: Wiley-VCH. ISBN 978-3-527-30616-9.
- ^ Grubbs, RH; Trnka, TM (2004). "Metátesis de olefinas catalizadas por rutenio". En Murahashi, S. (ed.). Rutenio en síntesis orgánica . Weinheim: Wiley-VCH. págs. 153-177. doi : 10.1002 / 3527603832.ch6 . ISBN 9783527603831.
- ^ a b c Vougioukalakis, GC; Grubbs, RH (2010). "Catalizadores de metátesis de olefinas coordinadas por carbeno heterocíclico basado en rutenio". Revisiones químicas . 110 (3): 1746-1787. doi : 10.1021 / cr9002424 . PMID 20000700 .
- ^ Trnka, TM; Grubbs, RH (2001). "El desarrollo de catalizadores de metátesis de olefinas L 2 X 2 Ru = CHR: una historia de éxito organometálica". Cuentas de Investigación Química . 34 (1): 18-29. doi : 10.1021 / ar000114f . PMID 11170353 .
- ^ Cossy, Janine; Arseniyadis, Stellios; Meyer, Christophe (2010). Metátesis en la síntesis de productos naturales: estrategias, sustratos y catalizadores (1ª ed.). Weinheim: Wiley-VCH. ISBN 978-3-527-32440-8.
- ↑ a b Lionel Delaude, Alfred F. Noels (2005). "Metátesis". Enciclopedia Kirk-Othmer de tecnología química . Weinheim: Wiley-VCH. doi : 10.1002 / 0471238961.metanoel.a01 . ISBN 978-0471238966.Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )
- ^ Nguyen, ST; Johnson, LK; Grubbs, RH; Ziller, JW (1992). "Polimerización por metátesis de apertura de anillo (ROMP) de norborneno por un complejo de carbeno del Grupo VIII en medios próticos" (PDF) . Revista de la Sociedad Química Estadounidense . 114 (10): 3974–3975. doi : 10.1021 / ja00036a053 .
- ^ Schwab, P .; Francia, MB; Ziller, JW; Grubbs, RH (1995). "Una serie de catalizadores de metátesis bien definidos - Síntesis de [RuCl 2 (= CHR ′) (PR 3 ) 2 ] y sus reacciones". Angew. Chem. En t. Ed. 34 (18): 2039–2041. doi : 10.1002 / anie.199520391 .
- ^ Schwab, P .; Grubbs, RH; Ziller, JW (1996). "Síntesis y aplicaciones de RuCl 2 (= CHR ') (PR 3 ) 2 : la influencia del resto alquilideno en la actividad de metátesis". Mermelada. Chem. Soc . 118 (1): 100-110. doi : 10.1021 / ja952676d .
- ^ Huang, J.-K .; Stevens, ED; Nolan, SP; Petersen, JL (1999). "Complejos de rutenio activos de metátesis de olefinas que llevan un ligando de carbeno nucleofílico". Mermelada. Chem. Soc . 121 (12): 2674–2678. doi : 10.1021 / ja9831352 .
- ^ Scholl, M .; Trnka, TM; Morgan, JP; Grubbs, RH (1999). "Aumento de la actividad de metátesis de cierre de anillo de catalizadores de metátesis de olefinas basados en rutenio coordinados con ligandos de imidazolin-2-ilideno". Letras de tetraedro . 40 (12): 2247–2250. doi : 10.1016 / S0040-4039 (99) 00217-8 .
- ↑ Ackermann, L .; Fürstner, A .; Weskamp, T .; Kohl, FJ; Herrmann, WA (1999). "Los complejos de carbeno de rutenio con ligandos de imidazolin-2-ilideno permiten la formación de cicloalquenos tetrasustituidos por RCM". Tetrahedron Lett . 40 (26): 4787–4790. doi : 10.1016 / S0040-4039 (99) 00919-3 .
- ^ Scholl, M .; Ding, S .; Lee, CW; Grubbs, RH (1999). "Síntesis y actividad de una nueva generación de catalizadores de metátesis de olefinas a base de rutenio coordinados con ligandos de 1,3-Dimesitil-4,5-dihidroimidazol-2-ilideno". Org. Letón. 1 (6): 953–956. doi : 10.1021 / ol990909q . PMID 10823227 .
- ^ Kingsbury, Jason S .; Harrity, Joseph PA; Bonitatebus, Peter J .; Hoveyda, Amir H. (1999). "Un catalizador de metátesis basado en Ru reciclable". Revista de la Sociedad Química Estadounidense . 121 (4): 791–799. doi : 10.1021 / ja983222u .
- ^ a b Gessler, S .; Randl, S .; Blechert, S. (2000). "Reacciones de síntesis y metátesis del complejo dihidroimidazol carbeno rutenio libre de fosfina". Letras de tetraedro . 41 (51): 9973–9976. doi : 10.1016 / S0040-4039 (00) 01808-6 .
- ^ a b Garber, SB; Kingsbury, JS; Gris, BL; Hoveyda, AH (2000). "Catalizadores de metátesis basados en Ru monoméricos y dendríticos eficientes y reciclables". Revista de la Sociedad Química Estadounidense . 122 (34): 8168–8179. doi : 10.1021 / ja001179g .
- ^ Engle, Keary M .; Lu, Gang; Luo, Shao-Xiong; Henling, Lawrence M .; Takase, Michael K .; Liu, Peng; Houk, KN; Grubbs, Robert H. (2015). "Orígenes de las diferencias en la tasa de iniciación en los catalizadores de metátesis de olefinas de rutenio que contienen bencilidenos quelantes". Revista de la Sociedad Química Estadounidense . 137 (17): 5782–5792. doi : 10.1021 / jacs.5b01144 . PMID 25897653 .
- ^ Luo, Shao-Xiong; Engle, Keary M .; Deng, Xiaofei; Hejl, Andrew; Takase, Michael K .; Henling, Lawrence M .; Liu, Peng; Houk, KN; Grubbs, Robert H. (2018). "Un modelo de predicción de cinética de iniciación permite el diseño racional de catalizadores de metátesis de olefinas de rutenio que llevan bencilidenos quelantes modificados" . Catálisis ACS . 8 (5): 4600–4611. doi : 10.1021 / acscatal.8b00843 . PMC 7289044 .
- ↑ Hong, Soon Hyeok; Grubbs, Robert H. (2006). "Catalizador de metátesis de olefinas altamente activo soluble en agua" (PDF) . Revista de la Sociedad Química Estadounidense . 128 (11): 3508–3509. doi : 10.1021 / ja058451c . PMID 16536510 .
- ^ Amor, JA; Morgan, JP; Trnka, TM; Grubbs, RH (2002). "Un catalizador a base de rutenio práctico y altamente activo que afecta la metátesis cruzada de acrilonitrilo". Angew. Chem. En t. Ed. Engl. 41 (21): 4035–4037. doi : 10.1002 / 1521-3773 (20021104) 41:21 <4035 :: AID-ANIE4035> 3.0.CO; 2-I . PMID 12412073 .
- ^ Walsh, Dylan J .; Lau, Sii Hong; Hyatt, Michael G .; Guironnet, Damien (25 de septiembre de 2017). "Estudio cinético de polimerización de metátesis de apertura de anillo vivo con catalizadores de Grubbs de tercera generación". Revista de la Sociedad Química Estadounidense . 139 (39): 13644-13647. doi : 10.1021 / jacs.7b08010 . ISSN 0002-7863 . PMID 28944665 .
- ^ Leitgeb, Anita; Wappel, Julia; Slugovc, Christian (2010). "La caja de herramientas ROMP actualizada" . Polímero . 51 (14): 2927-2946. doi : 10.1016 / j.polymer.2010.05.002 .
- ↑ Choi, T.-L .; Grubbs, RH (2003). "Polimerización de metátesis de apertura de anillo vivo controlada por un catalizador de rutenio de inicio rápido". Angewandte Chemie International Edition . 42 (15): 1743-1746. doi : 10.1002 / anie.200250632 . PMID 12707895 .
- Compuestos de organorutenio
- Catalizadores
- Complejos de fosfina
- Complejos de cloro