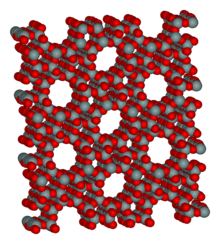
Catálisis heterogénea
En química, la catálisis heterogénea es una catálisis en la que la fase de los catalizadores difiere de la de los reactivos o productos . [1] El proceso contrasta con la catálisis homogénea donde los reactivos, productos y catalizador existen en la misma fase. La fase distingue no solo entre componentes sólidos , líquidos y gaseosos , sino también entre mezclas inmiscibles (p. ej. , aceite y agua ), o en cualquier lugar donde esté presente una interfaz.
La catálisis heterogénea típicamente involucra catalizadores en fase sólida y reactivos en fase gaseosa. [2] En este caso, hay un ciclo de adsorción molecular, reacción y desorción que ocurre en la superficie del catalizador. La termodinámica, la transferencia de masa y la transferencia de calor influyen en la velocidad (cinética) de la reacción .
La catálisis heterogénea es muy importante porque permite una producción más rápida a gran escala y la formación selectiva de productos. [3] Aproximadamente el 35% del PIB mundial está influenciado por la catálisis. [4] La producción del 90 % de los productos químicos (por volumen) está asistida por catalizadores sólidos. [2] Las industrias química y energética dependen en gran medida de la catálisis heterogénea. Por ejemplo, el proceso Haber-Bosch utiliza catalizadores a base de metales en la síntesis de amoníaco , un componente importante de los fertilizantes; En 2016 se produjeron 144 millones de toneladas de amoníaco. [5]
La adsorción es un paso esencial en la catálisis heterogénea. La adsorción es el proceso por el cual una molécula en fase gaseosa (o solución) (el adsorbato) se une a átomos de superficie sólidos (o líquidos) (el adsorbente). Lo contrario de la adsorción es la desorción , el adsorbato se separa del adsorbente. En una reacción facilitada por catálisis heterogénea, el catalizador es el adsorbente y los reactivos son el adsorbato.
Se reconocen dos tipos de adsorción: fisisorción , adsorción débilmente ligada, y quimisorción , adsorción fuertemente ligada. Muchos procesos en catálisis heterogénea se encuentran entre los dos extremos. El modelo de Lennard-Jones proporciona un marco básico para predecir las interacciones moleculares en función de la separación atómica. [6]
En la fisisorción, una molécula se siente atraída por los átomos de la superficie a través de las fuerzas de van der Waals . Estos incluyen interacciones dipolo-dipolo, interacciones dipolo inducidas y fuerzas de dispersión de London. Tenga en cuenta que no se forman enlaces químicos entre el adsorbato y el adsorbente, y sus estados electrónicos permanecen relativamente imperturbables. Las energías típicas para la fisisorción son de 3 a 10 kcal/mol. [2] En la catálisis heterogénea, cuando una molécula de reactivo fisisorbe a un catalizador, comúnmente se dice que está en un estado precursor, un estado de energía intermedia antes de la quimisorción, una adsorción más fuertemente unida. [6] Desde el estado precursor, una molécula puede sufrir quimisorción, desorción o migración a través de la superficie. [7]La naturaleza del estado precursor puede influir en la cinética de la reacción. [7]