Proceso de Castner-Kellner
El proceso Castner-Kellner es un método de electrólisis en una solución acuosa de cloruro alcalino (generalmente solución de cloruro de sodio ) para producir el correspondiente hidróxido alcalino , [1] inventado por el estadounidense Hamilton Castner y el austriaco [2] Karl Kellner en la década de 1890. [3]
La primera patente para electrolizar salmuera se concedió en Inglaterra en 1851 a Charles Watt . Sin embargo, su proceso no era un método económicamente factible para producir hidróxido de sodio porque no podía evitar que el cloro que se formaba en la solución de salmuera reaccionara con sus otros componentes. El químico e ingeniero estadounidense, Hamilton Castner , resolvió el problema de la mezcla con la invención de la celda de mercurio y se le otorgó una patente estadounidense en 1892 ( [1] ). químico austríaco, Carl Kellnerllegó a una solución similar casi al mismo tiempo. Para evitar una batalla legal, se convirtieron en socios en 1895 y fundaron la Castner-Kellner Alkali Company, que construyó plantas que empleaban el proceso en toda Europa. El proceso de celda de mercurio continúa en uso hasta el día de hoy. [4] Las operaciones actuales de la planta de celdas de mercurio son criticadas por la liberación ambiental de mercurio [5] que en algunos casos conduce a una intoxicación grave por mercurio ( como ocurrió en Japón ). Debido a estas preocupaciones, las plantas de celdas de mercurio se están eliminando gradualmente y se está realizando un esfuerzo sostenido para reducir las emisiones de mercurio de las plantas existentes. [6]
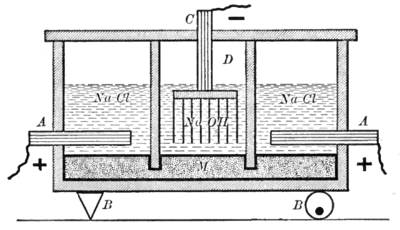
El aparato mostrado está dividido en dos tipos de celdas separadas por paredes de pizarra . El primer tipo, que se muestra a la derecha ya la izquierda del diagrama, usa un electrolito de solución de cloruro de sodio, un ánodo de grafito (A) y un cátodo de mercurio (M). El otro tipo de celda, que se muestra en el centro del diagrama, usa un electrolito de solución de hidróxido de sodio , un ánodo de mercurio (M) y un cátodo de hierro (D). El electrodo de mercurio es común entre las dos celdas. Esto se logra haciendo que las paredes que separan las celdas se sumerjan por debajo del nivel de los electrolitos, pero aún así permiten que el mercurio fluya por debajo de ellas. [7]
El gas de cloro resultante se ventila en la parte superior de las celdas exteriores donde se recolecta como un subproducto del proceso. La reacción en el cátodo de mercurio en las celdas exteriores es
El sodio metálico formado por esta reacción se disuelve en el mercurio para formar una amalgama . El mercurio conduce la corriente desde las celdas exteriores a la celda central. Además, un mecanismo oscilante (B mostrado por el fulcro a la izquierda y la rotación excéntrica a la derecha) agita el mercurio para transportar el sodio metálico disuelto desde las celdas exteriores a la celda central.
La reacción del ánodo en la celda central tiene lugar en la interfaz entre el mercurio y la solución de hidróxido de sodio.