Ozono
Ozono ( / oʊ z oʊ n / ), o trioxygen , es una inorgánico molécula con la fórmula química O
3. Es un gas azul pálido con un olor acre distintivo . Es un alótropo de oxígeno que es mucho menos estable que el alótropo diatómico O
2, descomponiéndose en la atmósfera inferior a O
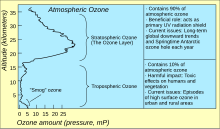
2( dioxígeno ). El ozono se forma a partir de dioxígeno por la acción de la luz ultravioleta (UV) y las descargas eléctricas dentro de la atmósfera terrestre . Está presente en concentraciones muy bajas a lo largo de este último, con su alta concentración más alta de la capa de ozono de la estratosfera , que absorbe la mayor parte de la Sun radiación ultravioleta 's (UV).
El olor del ozono recuerda al cloro y es detectable por muchas personas en concentraciones tan pequeñas como0,1 ppm en aire. La estructura del O 3 del ozono se determinó en 1865. Más tarde se demostró que la molécula tenía una estructura doblada y era débilmente paramagnética . En condiciones estándar , el ozono es un gas azul pálido que se condensa a temperaturas criogénicas a un líquido azul oscuro y finalmente a un sólido violeta-negro . La inestabilidad del ozono con respecto al dioxígeno más común es tal que tanto el gas concentrado como el ozono líquido pueden descomponerse explosivamente a temperaturas elevadas, golpes físicos o calentamiento rápido hasta el punto de ebullición. [5] Por lo tanto, se utiliza comercialmente solo en concentraciones bajas.
El ozono es un oxidante poderoso (mucho más que el dioxígeno ) y tiene muchas aplicaciones industriales y de consumo relacionadas con la oxidación. Este mismo alto potencial oxidante, sin embargo, hace que el ozono dañe las mucosas y los tejidos respiratorios de los animales, y también los tejidos de las plantas, en concentraciones superiores a aproximadamente0,1 ppm . Si bien esto hace que el ozono sea un potente peligro respiratorio y contaminante cerca del nivel del suelo, una concentración más alta en la capa de ozono (de dos a ocho ppm) es beneficiosa, ya que evita que la luz ultravioleta dañina llegue a la superficie de la Tierra.
El nombre trivial ozono es el nombre IUPAC más utilizado y preferido . Los nombres sistemáticos 2? 4 -trioxidiene [ dudoso ] y catena-trioxygen , válidos IUPAC nombres, se construyen de acuerdo con el sustitutivo y nomenclaturas aditivos, respectivamente. El nombre ozono deriva de ozein (ὄζειν), el verbo griego para olfato, que se refiere al olor distintivo del ozono.
En contextos apropiados, el ozono puede verse como un trioxidano con dos átomos de hidrógeno eliminados y, como tal, el trioxidanilideno puede usarse como un nombre sistemático, de acuerdo con la nomenclatura sustitutiva. Por defecto, estos nombres no tienen en cuenta la radicalidad de la molécula de ozono. En un contexto aún más específico, esto también puede nombrar el estado fundamental del singlete no radical, mientras que el estado dirradical se denomina trioxidandiilo .
Trioxidanediyl (u ozonide ) se usa, no sistemáticamente, para referirse al grupo sustituyente (-OOO-). Se debe tener cuidado para evitar confundir el nombre del grupo con el nombre específico del contexto para el ozono dado anteriormente.


.jpg/440px-Smyths_revised_ozonometer,_1865._(9660571191).jpg)