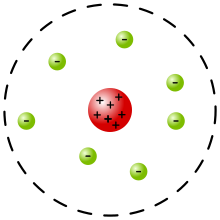
modelo rutherford
El modelo de Rutherford fue ideado por el físico nacido en Nueva Zelanda Ernest Rutherford para describir un átomo . Rutherford dirigió el experimento Geiger-Marsden en 1909, que sugirió, según el análisis de Rutherford de 1911, que el modelo del átomo de pudín de ciruelas de JJ Thomson era incorrecto. El nuevo modelo de Rutherford [1] para el átomo, basado en los resultados experimentales, contenía nuevas características de una carga central relativamente alta concentrada en un volumen muy pequeño en comparación con el resto del átomo y con este volumen central que también contenía la mayor parte del masa atómica del átomo. Esta región sería conocida como el " núcleo"del átomo.
Rutherford anuló el modelo de Thomson en 1911 con su conocido experimento de lámina de oro en el que demostró que el átomo tiene un núcleo diminuto y pesado. Rutherford diseñó un experimento para utilizar las partículas alfa emitidas por un elemento radiactivo como sondas para el mundo invisible de la estructura atómica. Si Thomson estaba en lo cierto, el rayo atravesaría directamente la lámina de oro. La mayoría de los rayos atravesaron la lámina, pero algunos fueron desviados.
Rutherford presentó su propio modelo físico para la estructura subatómica, como una interpretación de los inesperados resultados experimentales. En él, el átomo está formado por una carga central (este es el núcleo atómico moderno , aunque Rutherford no usó el término "núcleo" en su artículo) rodeado por una nube de (presuntamente) electrones en órbita . En este artículo de mayo de 1911, Rutherford solo se comprometió con una pequeña región central de carga positiva o negativa muy alta en el átomo.
Para concretar, considere el paso de una partícula α de alta velocidad a través de un átomo que tiene una carga central positiva N e y está rodeada por una carga compensatoria de N electrones. [2]
A partir de consideraciones puramente energéticas de hasta dónde podrían penetrar las partículas de velocidad conocida hacia una carga central de 100 e, Rutherford pudo calcular que el radio de su carga central de oro tendría que ser menor (no se puede decir cuánto menos). ) que 3,4 × 10 −14 metros. Esto fue en un átomo de oro que se sabe que tiene un radio de 10 a 10 metros, un hallazgo muy sorprendente, ya que implica una fuerte carga central de menos de 1/3000 del diámetro del átomo.
El modelo de Rutherford sirvió para concentrar gran parte de la carga y la masa del átomo en un núcleo muy pequeño, pero no atribuyó ninguna estructura a los electrones restantes ni a la masa atómica restante. Sí mencionó el modelo atómico de Hantaro Nagaoka , en el que los electrones están dispuestos en uno o más anillos, con la estructura metafórica específica de los anillos estables de Saturno. El modelo de budín de ciruelas de JJ Thomson también tenía anillos de electrones en órbita. Jean Baptiste Perrin afirmó en su conferencia Nobel [3] que él fue el primero en sugerir el modelo en su artículo de 1901. Pero en realidad, el físico Joseph Larmor creó el primer modelo del sistema solar del átomo en 1897. [4 ]