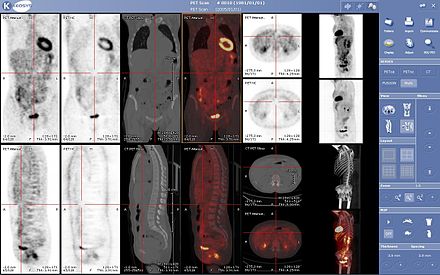
Medicina Nuclear
| Medicina Nuclear | |
|---|---|
| ICD-10-PCS | C |
| CIE-9 | 92 |
| Malla | D009683 |
| Código OPS-301 | 3-70 - 3-72 , 8-53 |
La medicina nuclear es una especialidad médica que implica la aplicación de sustancias radiactivas en el diagnóstico y tratamiento de enfermedades . Imágenes de medicina nuclear, en un sentido, es " radiología hecho de adentro hacia afuera" o "endoradiology" debido a que registra la emisión de radiación desde el interior del cuerpo en lugar de la radiación que es generada por fuentes externas como los rayos X . Además, las exploraciones de medicina nuclear difieren de la radiología, ya que el énfasis no está en la anatomía de la imagen, sino en la función. Por tal razón, se denomina modalidad de imagen fisiológica . Tomografía computarizada por emisión de fotón único (SPECT) yLa tomografía por emisión de positrones (PET) son las dos modalidades de imagen más comunes en medicina nuclear. [1]
Diagnóstico por imágenes médicas
Diagnóstico
En las imágenes de medicina nuclear, los radiofármacos se toman internamente, por ejemplo, por inhalación, por vía intravenosa u oral. Luego, los detectores externos ( cámaras gamma ) capturan y forman imágenes a partir de la radiación emitida por los radiofármacos. Este proceso es diferente a una radiografía de diagnóstico, donde la radiación externa pasa a través del cuerpo para formar una imagen.
Existen varias técnicas de medicina nuclear diagnóstica.
- 2D: La gammagrafía ("scint") es el uso de radionucleidos internos para crear imágenes bidimensionales. [2]
Una gammagrafía ósea de cuerpo entero de medicina nuclear. La gammagrafía ósea de cuerpo entero de medicina nuclear se usa generalmente en evaluaciones de diversas patologías relacionadas con los huesos, como dolor óseo, fractura por estrés, lesiones óseas no malignas, infecciones óseas o la diseminación del cáncer al hueso.
Escáner de perfusión miocárdica de medicina nuclear con talio-201 para las imágenes restantes (filas inferiores) y Tc-Sestamibi para las imágenes de estrés (filas superiores). La gammagrafía de perfusión miocárdica de medicina nuclear juega un papel fundamental en la evaluación no invasiva de la enfermedad de las arterias coronarias. El estudio no solo identifica a pacientes con enfermedad de las arterias coronarias; también proporciona información de pronóstico general o riesgo general de eventos cardíacos adversos para el paciente.
Una gammagrafía de paratiroides de medicina nuclear demuestra un adenoma paratiroideo adyacente al polo inferior izquierdo de la glándula tiroides. El estudio anterior se realizó con tecnecio-sestamibi (1ª columna) y yodo-123 (2ª columna) de imagen simultánea y la técnica de sustracción (3ª columna).
Exploración normal de ventilación y perfusión pulmonar (V / Q). La exploración V / Q de medicina nuclear es útil en la evaluación de la embolia pulmonar.
Gammagrafía de tiroides con yodo-123 para evaluación de hipertiroidismo.
- 3D: SPECT es una técnica tomográfica 3D que utiliza datos de cámaras gamma de muchas proyecciones y se puede reconstruir en diferentes planos. La tomografía por emisión de positrones (PET) utiliza la detección de coincidencia para obtener imágenes de los procesos funcionales.
Una exploración hepática SPECT de medicina nuclear con glóbulos rojos autólogos marcados con tecnecio-99m. Un foco de alta captación (flecha) en el hígado es compatible con un hemangioma.
Proyección de intensidad máxima (MIP) de una tomografía por emisión de positrones (PET) de cuerpo entero de una mujer de 79 kg después de la inyección intravenosa de 371 MBq de 18F-FDG (una hora antes de la medición).
Las pruebas de medicina nuclear difieren de la mayoría de las otras modalidades de imágenes en que las pruebas de diagnóstico muestran principalmente la función fisiológica del sistema que se investiga en contraposición a las imágenes anatómicas tradicionales como la TC o la RMN. Los estudios de imágenes de medicina nuclear son generalmente más específicos de órganos, tejidos o enfermedades (p. Ej., Gammagrafía pulmonar, gammagrafía cardíaca, gammagrafía ósea, gammagrafía cerebral, tumor, infección, Parkinson, etc.) que los de las imágenes radiológicas convencionales, que se centran en un sección particular del cuerpo (por ejemplo: radiografía de tórax, tomografía computarizada del abdomen / pelvis, tomografía computarizada de la cabeza, etc.). Además, existen estudios de medicina nuclear que permiten obtener imágenes de todo el cuerpo basándose en determinados receptores o funciones celulares. Algunos ejemplos son las exploraciones PET de cuerpo entero o las exploraciones PET / CT , exploraciones con galio ,exploraciones de glóbulos blancos con indio , exploraciones con MIBG y octreótido .
Si bien la capacidad del metabolismo nuclear para obtener imágenes de los procesos patológicos a partir de las diferencias en el metabolismo es insuperable, no es única. Ciertas técnicas como la imagen de resonancia magnética funcional de los tejidos (en particular los tejidos cerebrales) por el flujo sanguíneo y por lo tanto muestran el metabolismo. Además, las técnicas de mejora del contraste tanto en CT como en MRI muestran regiones de tejido que manejan los productos farmacéuticos de manera diferente, debido a un proceso inflamatorio.
Las pruebas de diagnóstico en medicina nuclear aprovechan la forma en que el cuerpo maneja las sustancias de manera diferente cuando hay una enfermedad o patología presente. El radionúclido introducido en el cuerpo a menudo se une químicamente a un complejo que actúa de manera característica dentro del cuerpo; esto se conoce comúnmente como trazador . En presencia de una enfermedad, un marcador a menudo se distribuirá por el cuerpo y / o se procesará de manera diferente. Por ejemplo, el ligando metilen-difosfonato ( MDP ) puede ser absorbido preferentemente por el hueso. Al unir químicamente tecnecio-99ma MDP, la radiactividad se puede transportar y unir al hueso a través de la hidroxiapatita para la obtención de imágenes. Cualquier función fisiológica aumentada, como la debida a una fractura en el hueso, generalmente significará una mayor concentración del marcador. Esto a menudo da como resultado la aparición de un "punto caliente", que es un aumento focal de la acumulación de radio o un aumento general de la acumulación de radio en todo el sistema fisiológico. Algunos procesos patológicos dan como resultado la exclusión de un marcador, lo que da como resultado la aparición de un "punto frío". Se han desarrollado muchos complejos trazadores para obtener imágenes o tratar muchos órganos, glándulas y procesos fisiológicos diferentes.
Técnicas de escaneo híbrido
En algunos centros, las exploraciones de medicina nuclear se pueden superponer, mediante software o cámaras híbridas, a imágenes de modalidades como la TC o la RM para resaltar la parte del cuerpo en la que se concentra el radiofármaco. Esta práctica a menudo se denomina fusión de imágenes o co-registro, por ejemplo, SPECT / CT y PET / CT. La técnica de imagen por fusión en medicina nuclear proporciona información sobre la anatomía y la función, que de otro modo no estaría disponible o requeriría un procedimiento o cirugía más invasivos.
Tomografía por emisión de positrones / TC de cuerpo entero normal con FDG -18. La exploración por TEP / TC de cuerpo entero se utiliza comúnmente en la detección, estadificación y seguimiento de varios cánceres.
PET / CT de cuerpo entero anormal con múltiples metástasis de un cáncer. La exploración por TEP / TC de cuerpo entero se ha convertido en una herramienta importante en la evaluación del cáncer.
Preocupaciones prácticas en las imágenes nucleares
Aunque no se comprenden bien los riesgos de las exposiciones a radiación de bajo nivel, se ha adoptado universalmente un enfoque cauteloso de que todas las exposiciones a la radiación humana deben mantenerse tan bajas como sea razonablemente posible, "ALARP". (Originalmente, esto se conocía como "Tan bajo como sea razonablemente posible" (ALARA), pero esto ha cambiado en los borradores modernos de la legislación para agregar más énfasis en lo "Razonablemente" y menos en lo "Alcanzable").
Trabajando con el principio ALARP, antes de que un paciente sea expuesto a un examen de medicina nuclear, se debe identificar el beneficio del examen. Esto debe tener en cuenta las circunstancias particulares del paciente en cuestión, cuando corresponda. Por ejemplo, si es poco probable que un paciente pueda tolerar una cantidad suficiente del procedimiento para lograr un diagnóstico, entonces sería inapropiado proceder a inyectar al paciente con el marcador radiactivo.
Cuando el beneficio justifique el procedimiento, la exposición a la radiación (la cantidad de radiación administrada al paciente) también debe mantenerse tan baja como sea razonablemente posible. Esto significa que las imágenes producidas en medicina nuclear nunca deberían ser mejores que las requeridas para un diagnóstico confiable. Dar mayores exposiciones a la radiación puede reducir el ruido en una imagen y hacerla más atractiva desde el punto de vista fotográfico, pero si la pregunta clínica puede responderse sin este nivel de detalle, entonces esto es inapropiado.
Como resultado, la dosis de radiación de las imágenes de medicina nuclear varía mucho según el tipo de estudio. La dosis de radiación eficaz puede ser inferior o comparable o puede superar con creces la dosis de radiación de fondo anual ambiental diaria general . Asimismo, también puede ser menor, en el rango o mayor que la dosis de radiación de una tomografía computarizada de abdomen / pelvis.
Algunos procedimientos de medicina nuclear requieren una preparación especial del paciente antes del estudio para obtener el resultado más preciso. Las preparaciones previas a la obtención de imágenes pueden incluir la preparación dietética o la suspensión de ciertos medicamentos. Se anima a los pacientes a consultar con el departamento de medicina nuclear antes de una exploración.
Análisis
El resultado final del proceso de obtención de imágenes de medicina nuclear es un "conjunto de datos" que comprende una o más imágenes. En conjuntos de datos de múltiples imágenes, la matriz de imágenes puede representar una secuencia de tiempo (es decir, cine o película) a menudo llamada un conjunto de datos "dinámico", una secuencia de tiempo cardíaca activada o una secuencia espacial donde la cámara gamma se mueve en relación con el paciente. SPECT (tomografía computarizada por emisión de fotón único) es el proceso mediante el cual las imágenes adquiridas de una cámara gamma giratoria se reconstruyen para producir una imagen de un "corte" a través del paciente en una posición particular. Una colección de cortes paralelos forma una pila de cortes, una representación tridimensional de la distribución de radionucleidos en el paciente.
La computadora de medicina nuclear puede requerir millones de líneas de código fuente para proporcionar paquetes de análisis cuantitativos para cada una de las técnicas de imágenes específicas disponibles en medicina nuclear. [ cita requerida ]
Las secuencias de tiempo se pueden analizar más a fondo utilizando modelos cinéticos como modelos multicompartimentales o un diagrama de Patlak .
Medicina nuclear intervencionista
La terapia con radionúclidos se puede usar para tratar afecciones como hipertiroidismo , cáncer de tiroides , cáncer de piel y trastornos sanguíneos.
En la terapia de medicina nuclear, la dosis de tratamiento con radiación se administra internamente (por ejemplo, vías intravenosa u oral) o externamente directamente sobre el área a tratar en forma de un compuesto (por ejemplo, en el caso de cáncer de piel).
Los radiofármacos utilizados en la terapia de medicina nuclear emiten radiación ionizante que viaja solo una corta distancia, lo que minimiza los efectos secundarios no deseados y el daño a órganos no afectados o estructuras cercanas. La mayoría de las terapias de medicina nuclear se pueden realizar como procedimientos ambulatorios, ya que el tratamiento tiene pocos efectos secundarios y la exposición del público en general a la radiación puede mantenerse dentro de un límite seguro.
Terapias comunes de medicina nuclear (fuente no sellada)
| Sustancia | Condición |
|---|---|
| Yoduro de yodo-131- sodio | hipertiroidismo y cáncer de tiroides |
| Itrio-90- ibritumomab tiuxetan (Zevalin) y yodo-131- tositumomab (Bexxar) | linfoma refractario |
| 131 I-MIBG ( metayodobencilguanidina ) | tumores neuroendocrinos |
| Samario-153 o estroncio-89 | tratamiento paliativo del dolor óseo |
| Renio -188 | carcinoma de células escamosas o carcinoma de células basales de la piel |
En algunos centros, el departamento de medicina nuclear también puede utilizar cápsulas de isótopos implantadas ( braquiterapia ) para tratar el cáncer.
Fuentes de radiación de uso común (radionúclidos) para braquiterapia [3]
| Radionúclido | Escribe | Media vida | Energía |
|---|---|---|---|
| Cesio-137 ( 137 Cs) | rayos γ | 30,17 años | 0,662 MeV |
| Cobalto-60 ( 60 Co) | rayos γ | 5,26 años | 1,17, 1,33 MeV |
| Iridio-192 ( 192 Ir) | β - -particles | 73,8 días | 0,38 MeV (media) |
| Yodo-125 ( 125 I) | rayos γ | 59,6 días | 27,4, 31,4 y 35,5 keV |
| Paladio-103 ( 103 Pd) | rayos γ | 17,0 días | 21 keV (media) |
| Rutenio-106 ( 106 Ru) | β - -particles | 1,02 años | 3,54 MeV |
Historia
La historia de la medicina nuclear contiene contribuciones de científicos de diferentes disciplinas en física, química, ingeniería y medicina. La naturaleza multidisciplinaria de la medicina nuclear dificulta a los historiadores médicos determinar la fecha de nacimiento de la medicina nuclear. Probablemente, esto puede ubicarse mejor entre el descubrimiento de la radiactividad artificial en 1934 y la producción de radionúclidos por el Laboratorio Nacional de Oak Ridge para uso relacionado con la medicina, en 1946. [4]
Los orígenes de esta idea médica se remontan a mediados de la década de 1920 en Friburgo , Alemania, cuando George de Hevesy realizó experimentos con radionucleidos administrados a ratas, mostrando así las vías metabólicas de estas sustancias y estableciendo el principio del trazador . Posiblemente, la génesis de este campo de la medicina tuvo lugar en 1936, cuando John Lawrence , conocido como "el padre de la medicina nuclear", se ausentó de su puesto de profesor en la Facultad de Medicina de Yale , para visitar a su hermano Ernest Lawrence en su nueva residencia. laboratorio de radiación (ahora conocido como Laboratorio Nacional Lawrence Berkeley ) en Berkeley , California. Más tarde, John Lawrence hizo la primera aplicación en pacientes de un radionúclido artificial cuando utilizó fósforo-32 para tratar la leucemia . [5] [6]
Muchos historiadores consideran el descubrimiento de radionúclidos producidos artificialmente por Frédéric Joliot-Curie e Irène Joliot-Curie en 1934 como el hito más significativo de la medicina nuclear. [4] En febrero de 1934, informaron sobre la primera producción artificial de material radiactivo en la revista Nature , después de descubrir radiactividad en papel de aluminio irradiado con una preparación de polonio. Su trabajo se basó en descubrimientos anteriores de Wilhelm Konrad Roentgen para rayos X, Henri Becquerel para sales de uranio radiactivo y Marie Curie (madre de Irène Curie) para torio radiactivo, polonio y acuñando el término "radiactividad". Taro Takemiestudió la aplicación de la física nuclear a la medicina en la década de 1930. La historia de la medicina nuclear no estará completa sin mencionar a estos pioneros.
La medicina nuclear ganó reconocimiento público como una especialidad potencial cuando el 11 de mayo de 1946 un artículo en el Journal of the American Medical Association (JAMA) del Dr. Saul Hertz del Massachusetts General Hospital y el Dr. Arthur Roberts del Massachusetts Institute of Technology, describió el uso exitoso sobre el tratamiento de la enfermedad de Graves con yodo radiactivo (RAI). [7] Además, Sam Seidlin . [8] trajo un mayor desarrollo en el campo que describe un tratamiento exitoso de un paciente con metástasis de cáncer de tiroides utilizando yodo radiactivo ( I-131 ). Estos artículos son considerados por muchos historiadores como los artículos más importantes jamás publicados en medicina nuclear. [9]Aunque el uso más temprano de I-131 se dedicó a la terapia del cáncer de tiroides, su uso se expandió más tarde para incluir imágenes de la glándula tiroides, cuantificación de la función tiroidea y terapia para el hipertiroidismo. Entre los muchos radionucleidos que se descubrieron para uso médico, ninguno fue tan importante como el descubrimiento y desarrollo del tecnecio-99m . Fue descubierto por primera vez en 1937 por C. Perrier y E. Segre como un elemento artificial para llenar el espacio número 43 en la Tabla Periódica. El desarrollo de un sistema generador para producir tecnecio-99m en la década de 1960 se convirtió en un método práctico para uso médico. Hoy en día, el tecnecio-99m es el elemento más utilizado en medicina nuclear y se emplea en una amplia variedad de estudios de imágenes de medicina nuclear.
El uso clínico generalizado de la medicina nuclear comenzó a principios de la década de 1950, cuando se expandieron los conocimientos sobre los radionucleidos, la detección de radiactividad y el uso de ciertos radionucleidos para rastrear procesos bioquímicos. Los trabajos pioneros de Benedict Cassen en el desarrollo del primer escáner rectilíneo y la cámara de centelleo de Hal O. Anger ( cámara Anger ) ampliaron la joven disciplina de la medicina nuclear hasta convertirla en una especialidad de imágenes médicas en toda regla.
A principios de la década de 1960, en el sur de Escandinavia , Niels A. Lassen , David H. Ingvar y Erik Skinhøj desarrollaron técnicas que proporcionaron los primeros mapas de flujo sanguíneo del cerebro, que inicialmente incluían la inhalación de xenón-133 ; [10] poco después se desarrolló un equivalente intraarterial, que permite medir la distribución local de la actividad cerebral en pacientes con trastornos neuropsiquiátricos como la esquizofrenia. [11] Las versiones posteriores tendrían 254 centelleadores.por lo que podría producirse una imagen bidimensional en un monitor a color. Les permitió construir imágenes que reflejan la activación cerebral a partir del habla, la lectura, la percepción visual o auditiva y el movimiento voluntario. [12] La técnica también se utilizó para investigar, por ejemplo, movimientos secuenciales imaginados, cálculo mental y navegación espacial mental. [13] [14]
En la década de 1970, la mayoría de los órganos del cuerpo podían visualizarse mediante procedimientos de medicina nuclear. En 1971, la Asociación Médica Estadounidense reconoció oficialmente la medicina nuclear como especialidad médica. [15] En 1972, se estableció la Junta Estadounidense de Medicina Nuclear , y en 1974, se estableció la Junta Osteopática Estadounidense de Medicina Nuclear , consolidando la medicina nuclear como una especialidad médica independiente.
En la década de 1980, se diseñaron radiofármacos para su uso en el diagnóstico de enfermedades cardíacas. El desarrollo de la tomografía computarizada por emisión de fotón único (SPECT), aproximadamente al mismo tiempo, condujo a la reconstrucción tridimensional del corazón y al establecimiento del campo de la cardiología nuclear.
Los desarrollos más recientes en medicina nuclear incluyen la invención del primer escáner de tomografía por emisión de positrones ( PET ). El concepto de tomografía de emisión y transmisión, más tarde desarrollado en tomografía computarizada por emisión de fotón único (SPECT), fue introducido por David E. Kuhl y Roy Edwards a fines de la década de 1950. [ cita requerida ]Su trabajo condujo al diseño y construcción de varios instrumentos tomográficos en la Universidad de Pennsylvania. Las técnicas de imágenes tomográficas se desarrollaron aún más en la Facultad de Medicina de la Universidad de Washington. Estas innovaciones llevaron a la obtención de imágenes de fusión con SPECT y CT de Bruce Hasegawa de la Universidad de California en San Francisco (UCSF), y el primer prototipo de PET / CT de DW Townsend de la Universidad de Pittsburgh en 1998. [ cita requerida ]
Las imágenes de PET y PET / CT experimentaron un crecimiento más lento en sus primeros años debido al costo de la modalidad y al requerimiento de un ciclotrón in situ o cercano. Sin embargo, una decisión administrativa para aprobar el reembolso médico de aplicaciones limitadas de PET y PET / CT en oncología ha dado lugar a un crecimiento fenomenal y una aceptación generalizada en los últimos años, lo que también se vio facilitado por el establecimiento de trazadores etiquetados con 18F para procedimientos estándar, lo que permitió trabajar en sitios no equipados con ciclotrón. Las imágenes PET / CT son ahora una parte integral de la oncología para el diagnóstico, la estadificación y la monitorización del tratamiento. Un escáner de MRI / PET totalmente integrado está en el mercado desde principios de 2011. [ cita requerida ]
Fuentes de radionucleidos
El 99m Tc se suministra normalmente a los hospitales a través de un generador de radionúclidos que contiene el radionúclido molibdeno-99 original . El 99 Mo se obtiene típicamente como un producto de fisión de 235 U en reactores nucleares, sin embargo, la escasez de suministro global ha llevado a la exploración de otros métodos de producción . Aproximadamente un tercio del suministro mundial, y la mayor parte del suministro europeo, de isótopos médicos se produce en el reactor nuclear de Petten en los Países Bajos . Otro tercio del suministro mundial, y la mayor parte del suministro de América del Norte, se produjo en los Laboratorios Chalk River en Chalk River., Ontario , Canadá hasta su cierre permanente en 2018. [16]
El radioisótopo más comúnmente utilizado en PET 18 F , no se produce en ningún reactor nuclear, sino en un acelerador circular llamado ciclotrón . El ciclotrón se utiliza para acelerar los protones para bombardear el isótopo pesado estable de oxígeno 18 O . El 18 O constituye aproximadamente el 0,20% del oxígeno ordinario (principalmente oxígeno-16 ), del cual se extrae. El 18 F es entonces típicamente utiliza para hacer FDG .
| isótopo | símbolo | Z | T 1/2 | decaer | gamma (keV) | Energía beta (keV) |
|---|---|---|---|---|---|---|
| Imágenes: | ||||||
| flúor-18 | 18 F | 9 | 109,77 metros | β + | 511 (193%) | 249,8 (97%) [20] |
| galio-67 | 67 Ga | 31 | 3,26 días | CE | 93 (39%), 185 (21%), 300 (17%) | - |
| criptón-81m | 81 millones Kr | 36 | 13,1 s | ESO | 190 (68%) | - |
| rubidio-82 | 82 Rb | 37 | 1,27 metros | β + | 511 (191%) | 3.379 (95%) |
| nitrógeno-13 | 13 N | 7 | 9,97 metros | β + | 511 (200%) | 1190 (100%) [21] |
| tecnecio-99m | 99m Tc | 43 | 6,01 horas | ESO | 140 (89%) | - |
| indio-111 | 111 en | 49 | 2,80 días | CE | 171 (90%), 245 (94%) | - |
| yodo-123 | 123 yo | 53 | 13,3 h | CE | 159 (83%) | - |
| xenón-133 | 133 Xe | 54 | 5,24 días | β - | 81 (31%) | 0,364 (99%) |
| talio-201 | 201 Tl | 81 | 3,04 días | CE | 69–83 * (94%), 167 (10%) | - |
| Terapia: | ||||||
| itrio-90 | 90 Y | 39 | 2,67 días | β - | - | 2.280 (100%) |
| yodo-131 | 131 Yo | 53 | 8.02 días | β - | 364 (81%) | 0,807 (100%) |
| lutecio-177 | 177 Lu | 71 | 6,65 días | β - | 113 (6,6%), 208 (11%) | 497 (78,6%), 384 (9,1%), 176 (12,2%) |
Z = número atómico, el número de protones; T 1/2 = vida media; decaimiento = modo de decaimiento | ||||||
Un estudio típico de medicina nuclear implica la administración de un radionúclido en el cuerpo mediante inyección intravenosa en forma líquida o agregada, la ingestión combinada con alimentos, la inhalación como gas o aerosol o, en raras ocasiones, la inyección de un radionúclido que se ha sometido a microencapsulación . Algunos estudios requieren el etiquetado de los propios glóbulos del paciente con un radionúclido ( gammagrafía de leucocitos y gammagrafía de glóbulos rojos ). La mayoría de los radionúclidos de diagnóstico emiten rayos gamma directamente de su desintegración o indirectamente a través de la aniquilación de electrones y positrones , mientras que las propiedades dañinas para las células de las partículas betase utilizan en aplicaciones terapéuticas. Los radionucleidos refinados para su uso en medicina nuclear se derivan de procesos de fisión o fusión en reactores nucleares , que producen radionucleidos con vidas medias más largas, o ciclotrones , que producen radionucleidos con vidas medias más cortas, o aprovechan los procesos de desintegración natural en generadores específicos. es decir, molibdeno / tecnecio o estroncio / rubidio.
Los radionúclidos intravenosos más comúnmente usados son tecnecio-99m, yodo-123, yodo-131, talio-201, galio-67, flúor-18 fluorodesoxiglucosa y leucocitos marcados con indio-111 . [ cita requerida ] Los radionúclidos gaseosos / en aerosol más comúnmente usados son xenón-133, criptón-81m, tecnecio-99m ( aerosolizado ). [22]
Policias y procedimientos
Dosis de radiación
Un paciente que se somete a un procedimiento de medicina nuclear recibirá una dosis de radiación. Según las directrices internacionales actuales, se asume que cualquier dosis de radiación, por pequeña que sea, presenta un riesgo. En general, se acepta que la dosis de radiación administrada a un paciente en una investigación de medicina nuclear, aunque no probada, presenta un riesgo muy pequeño de inducir cáncer. A este respecto, es similar al riesgo de las investigaciones de rayos X, excepto que la dosis se administra internamente en lugar de una fuente externa, como una máquina de rayos X, y las cantidades de dosificación son típicamente significativamente más altas que las de los rayos X.
La dosis de radiación de una investigación de medicina nuclear se expresa como una dosis efectiva con unidades de sieverts (generalmente administradas en milisieverts, mSv). La dosis efectiva resultante de una investigación está influenciada por la cantidad de radioactividad administrada en megabequerelios (MBq), las propiedades físicas del radiofármaco utilizado, su distribución en el cuerpo y su tasa de eliminación del cuerpo.
Las dosis efectivas pueden variar desde 6 μSv (0.006 mSv) para una medición de 3 MBq de cromo -51 EDTA de la tasa de filtración glomerular hasta 11.2 mSv (11.200 μSv) para un procedimiento de imágenes de miocardio con 80 MBq de talio -201 . La gammagrafía ósea común con 600 MBq de tecnecio-99m MDP tiene una dosis efectiva de aproximadamente 2,9 mSv (2900 μSv). [23]
Antiguamente, las unidades de medida eran el curie (Ci), siendo 3.7E10 Bq, y también 1.0 gramos de Radio ( Ra-226 ); el rad (dosis de radiación absorbida), ahora reemplazada por el gris ; y el rem ( hombre equivalente de Röntgen ), ahora reemplazado por el sievert . [24] El rad y el rem son esencialmente equivalentes para casi todos los procedimientos de medicina nuclear, y solo la radiación alfa producirá un valor Rem o Sv más alto, debido a su efectividad biológica relativa mucho más alta.(RBE). En la actualidad, los emisores alfa rara vez se utilizan en medicina nuclear, pero se utilizaron ampliamente antes de la llegada de los radionucleidos producidos por reactores nucleares y aceleradores. Los conceptos relacionados con la exposición de los seres humanos a las radiaciones están cubiertos por el campo de la Física de la Salud ; el desarrollo y la práctica de técnicas de medicina nuclear seguras y eficaces es un enfoque clave de la Física Médica .
Marcos regulatorios y directrices
Diferentes países de todo el mundo mantienen marcos regulatorios que son responsables de la gestión y el uso de radionucleidos en diferentes entornos médicos. Por ejemplo, en los EE. UU., La Comisión Reguladora Nuclear (NRC) y la Administración de Alimentos y Medicamentos (FDA) tienen pautas establecidas para que las sigan los hospitales. [25] Con la NRC, si los materiales radiactivos no están involucrados, como los rayos X, por ejemplo, no están regulados por la agencia y, en cambio, están regulados por los estados individuales. [26] Organizaciones internacionales, como el Organismo Internacional de Energía Atómica.(OIEA), han publicado periódicamente diferentes artículos y directrices sobre las mejores prácticas en medicina nuclear, así como informes sobre tecnologías emergentes en medicina nuclear. [27] [28] Otros factores que se consideran en la medicina nuclear incluyen el historial médico del paciente y el manejo posterior al tratamiento. Grupos como la Comisión Internacional de Protección Radiológica han publicado información sobre cómo gestionar el alta de pacientes de un hospital con radionucleidos no sellados. [29]
Ver también
- Investigación con sujetos humanos
- Lista de sociedades de medicina nuclear
- Médico de medicina nuclear
- Tecnología nuclear
- Radiógrafo
Referencias
- ^ "Medicina nuclear" . Archivado desde el original el 27 de febrero de 2015 . Consultado el 20 de agosto de 2015 .
- ^ Citación de gammagrafía : Diccionario médico de Dorland para consumidores de salud, 2007 por Saunders; Saunders Comprehensive Veterinary Dictionary, 3 ed. 2007; McGraw-Hill Concise Dictionary of Modern Medicine, 2002 por The McGraw-Hill Companies
- ^ "Tarjetas de cartera nuclear" . Consultado el 20 de agosto de 2015 .
- ↑ a b Edwards, CL (1979). "Radionúclidos de localización de tumores en retrospectiva y perspectiva". Seminarios de Medicina Nuclear . 9 (3): 186–9. doi : 10.1016 / s0001-2998 (79) 80030-6 . PMID 388628 .
- ^ Laboratorio Donner: el lugar de nacimiento de. Medicina Nuclear
- ^ Momentos importantes en la historia de la medicina nuclear
- ^ Hertz S, Roberts A (mayo de 1946). "Yodo radiactivo en el estudio de la fisiología tiroidea; el uso de la terapia con yodo radiactivo en el hipertiroidismo". Revista de la Asociación Médica Estadounidense . 131 : 81–6. doi : 10.1001 / jama.1946.02870190005002 . PMID 21025609 .
- ^ Seidlin SM, Marinelli LD, Oshry E (diciembre de 1946). "Terapia con yodo radiactivo; efecto sobre las metástasis funcionales del adenocarcinoma de tiroides". Revista de la Asociación Médica Estadounidense . 132 (14): 838–47. doi : 10.1001 / jama.1946.02870490016004 . PMID 20274882 .
- ^ Henkin R, et al. (1996). Medicina nuclear (Primera ed.). ISBN 978-0-8016-7701-4.
- ^ Lassen NA , Ingvar DH (1961). "Determinación cuantitativa del flujo sanguíneo cerebral regional en el hombre". The Lancet . 278 (7206): 806–807. doi : 10.1016 / s0140-6736 (61) 91092-3 .
- ^ Ingvar DH , Franzén G (diciembre de 1974). "Distribución de la actividad cerebral en la esquizofrenia crónica" . Lancet . 2 (7895): 1484–6. doi : 10.1016 / s0140-6736 (74) 90221-9 . PMID 4140398 .
- ^ Lassen NA , Ingvar DH , Skinhøj E (octubre de 1978). "Función cerebral y flujo sanguíneo". Scientific American . 239 (4): 62–71. Código Bibliográfico : 1978SciAm.239d..62L . doi : 10.1038 / scientificamerican1078-62 . PMID 705327 .
- ^ Roland PE , Larsen B, Lassen NA , Skinhøj E (enero de 1980). "Área motora suplementaria y otras áreas corticales en la organización de los movimientos voluntarios en el hombre". Revista de neurofisiología . 43 (1): 118–36. doi : 10.1152 / jn.1980.43.1.118 . PMID 7351547 .
- ^ Roland PE , Friberg L (1985). "Localización de áreas corticales activadas por el pensamiento" . Revista de neurofisiología . 53 (5). págs. 1219-1243.
- ^ "¿Qué es la medicina nuclear" (PDF) . Sociedad de Medicina Nuclear .
- ^ "Canadá cierra permanentemente el reactor de investigación NRU" . Internacional de Ingeniería Nuclear . 6 de abril de 2018.
- ^ Eckerman KF, Endo A: MIRD: Esquemas de desintegración y datos de radionúclidos. Sociedad de Medicina Nuclear, 2008. ISBN 978-0-932004-80-2
- ^ Tabla de isótopos radiactivos Archivado el 4 de diciembre de 2004 en la Wayback Machine.
- ^ Dash A, Pillai MR, Knapp FF (junio de 2015). "Producción de (177) Lu para terapia con radionúclidos dirigida: opciones disponibles" . Medicina nuclear e imagenología molecular . 49 (2): 85-107. doi : 10.1007 / s13139-014-0315-z . PMC 4463871 . PMID 26085854 .
- ^ "Inyección de fluoruro de sodio F 18" . Consultado el 20 de agosto de 2015 .
- ^ "Amoníaco N-13" . Consultado el 20 de agosto de 2015 .
- ^ Technegas un radioaerosol inventado en Australia por el Dr. Bill Burch y el Dr. Richard Fawdry
- ^ Comité Asesor de Administración de Sustancias Radiactivas (19 de febrero de 2021). "Notas de la ARSAC para orientación" (pdf) . GOV.UK . Salud Pública de Inglaterra .
- ↑ Chandler, David (28 de marzo de 2011). "Explicado: rad, rem, sieverts, becquerels" . Noticias del MIT | Instituto de Tecnología de Massachusetts . Consultado el 25 de abril de 2021 .
- ^ Le, Dao (2021), Wong, Franklin CL (ed.), "Una descripción general de las regulaciones de los radiofármacos" , Terapia del cáncer con radionúclidos locorregionales: aspectos clínicos y científicos , Cham: Springer International Publishing, págs. 225–247, doi : 10.1007 / 978-3-030-56267-0_10 , ISBN 978-3-030-56267-0, consultado el 25 de abril de 2021
- ^ "Medicina nuclear: qué es y qué no es" . NRC Web . 2020-06-08 . Consultado el 25 de abril de 2021 .
- ^ "Normas de seguridad del OIEA y exposición médica" . www.iaea.org . 2017-10-30 . Consultado el 25 de abril de 2021 .
- ^ "Campus de salud humana - Medicina nuclear" . humanhealth.iaea.org . Consultado el 25 de abril de 2021 .
- ^ "Liberación de pacientes después de la terapia con radionucleidos no sellados" . Anales de la ICRP . 34 (2): v – vi. Junio de 2004. doi : 10.1016 / j.icrp.2004.08.001 . ISSN 0146-6453 .
Otras lecturas
- Mas JC (2008). Una guía para el paciente sobre procedimientos de medicina nuclear: inglés-español . Sociedad de Medicina Nuclear. ISBN 978-0-9726478-9-2.
- Taylor A, Schuster DM, Naomi Alazraki N (2000). Una guía para médicos de medicina nuclear (2ª ed.). Sociedad de Medicina Nuclear. ISBN 978-0-932004-72-7.
- Shumate MJ, Kooby DA, Alazraki NP (enero de 2007). Guía para médicos de oncología nuclear: terapias prácticas de imágenes moleculares y radionúclidos . Sociedad de Medicina Nuclear. ISBN 978-0-9726478-8-5.
- Ell P, Gambhir S (2004). Medicina nuclear en el diagnóstico y tratamiento clínico . Churchill Livingstone. pag. 1950. ISBN 978-0-443-07312-0.
- Jones DW, Hogg P, Seeram E (marzo de 2013). SPECT / TC práctica en medicina nuclear . ISBN 978-1447147022.
enlaces externos
| Wikimedia Commons tiene medios relacionados con la medicina nuclear . |
| Wikilibros tiene un libro sobre el tema: Física básica de la medicina nuclear |
Wikinews tiene noticias relacionadas:
|
- Medicina nuclear en Curlie
- Audiencia sobre la resolución de la crisis de isótopos médicos ante el Subcomité de Energía y Medio Ambiente del Comité de Energía y Comercio, Cámara de Representantes, Ciento Undécimo Congreso, Primera Sesión, 9 de septiembre de 2009
| Recursos de la biblioteca sobre medicina nuclear |
|
- Medicina Nuclear
- Radiología
- Radioquímica medicinal