Dióxido de silicio
El dióxido de silicio , también conocido como sílice , es un óxido de silicio con la fórmula química SiO 2 , que se encuentra más comúnmente en la naturaleza como cuarzo y en varios organismos vivos. [5] [6] En muchas partes del mundo, la sílice es el componente principal de la arena . La sílice es una de las familias de materiales más complejas y abundantes, que existe como compuesto de varios minerales y como producto sintético. Ejemplos notables incluyen cuarzo fundido , sílice ahumada , gel de sílice y aerogeles.. Se utiliza en materiales estructurales, microelectrónica (como aislante eléctrico ) y como componentes en las industrias alimentaria y farmacéutica.
En la mayoría de los silicatos , el átomo de silicio muestra una coordinación tetraédrica , con cuatro átomos de oxígeno rodeando un átomo de Si central ( ver Celda unitaria 3-D ). Por tanto, el SiO 2 forma sólidos de red tridimensionales en los que cada átomo de silicio está unido covalentemente de forma tetraédrica a 4 átomos de oxígeno. Por el contrario, el CO 2 es una molécula lineal. Las estructuras marcadamente diferentes de los dióxidos de carbono y silicio es una manifestación de la regla del doble enlace .
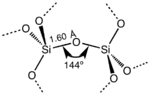
El SiO 2 tiene varias formas cristalinas distintas , pero casi siempre tienen la misma estructura local alrededor de Si y O. En el cuarzo α, la longitud del enlace Si-O es de 161 pm, mientras que en la α-tridimita está en el rango de 154-171 pm. . El ángulo Si-O-Si también varía entre un valor bajo de 140 ° en α-tridimita, hasta 180 ° en β-tridimita. En el cuarzo α, el ángulo Si-O-Si es de 144 °. [8]
El cuarzo alfa es la forma estable de SiO 2 sólido a temperatura ambiente. Los minerales de alta temperatura, cristobalita y tridimita , tienen densidades e índices de refracción más bajos que el cuarzo. La transformación de cuarzo α en cuarzo beta se produce de forma abrupta a 573 ° C. Dado que la transformación va acompañada de un cambio significativo de volumen, puede inducir fácilmente la fractura de cerámicas o rocas que atraviesan este límite de temperatura. [9] Sin embargo , los minerales de alta presión, seifertita , stishovita y coesita , tienen densidades e índices de refracción más altos que el cuarzo. [10] Stishovite tiene unestructura similar al rutilo donde el silicio tiene 6 coordenadas. La densidad de la stishovita es 4.287 g / cm 3 , que se compara con el cuarzo α, la más densa de las formas de baja presión, que tiene una densidad de 2.648 g / cm 3 . [11] La diferencia de densidad se puede atribuir al aumento de la coordinación, ya que las seis longitudes de enlace de Si-O más cortas en la stishovita (cuatro longitudes de enlace de Si-O de 176 pm y otras dos de 181 pm) son mayores que las de Si-O longitud de enlace (161 pm) en cuarzo α. [12] El cambio en la coordinación aumenta la ionicidad del enlace Si-O. [13] Más importante aún, cualquier desviación de estos parámetros estándar constituye diferencias o variaciones microestructurales, que representan una aproximación a un amorfo, vítreo o sólido vítreo.
La sílice faujasita , otro polimorfo, se obtiene por desaluminización de una zeolita Y ultraestable y baja en sodio con un tratamiento combinado de ácido y térmico. El producto resultante contiene más del 99% de sílice y tiene una alta cristalinidad y una superficie específica (más de 800 m 2 / g). La sílice de faujasita tiene una estabilidad térmica y ácida muy alta. Por ejemplo, mantiene un alto grado de cristalinidad o orden molecular de largo alcance incluso después de hervir en ácido clorhídrico concentrado . [14]
La sílice fundida exhibe varias características físicas peculiares que son similares a las observadas en el agua líquida : expansión de temperatura negativa, densidad máxima a temperaturas de ~ 5000 ° C y una capacidad calorífica mínima. [15] Su densidad disminuye de 2,08 g / cm 3 a 1950 ° C a 2,03 g / cm 3 a 2200 ° C. [dieciséis]