Doble capa (ciencia de superficies)
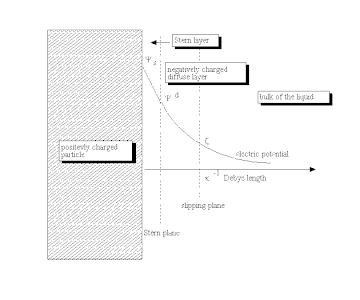
Una doble capa ( DL , también llamada doble capa eléctrica , EDL ) es una estructura que aparece en la superficie de un objeto cuando se expone a un fluido. El objeto puede ser una partícula sólida, una burbuja de gas, una gota de líquido o un cuerpo poroso . El DL se refiere a dos capas paralelas de carga que rodean el objeto. La primera capa, la carga superficial (ya sea positiva o negativa), consta de iones adsorbidos en el objeto debido a interacciones químicas. La segunda capa está compuesta de iones atraídos por la carga de la superficie a través de la fuerza de Coulomb , apantallando eléctricamentela primera capa. Esta segunda capa está vagamente asociada con el objeto. Está hecho de iones libres que se mueven en el fluido bajo la influencia de la atracción eléctrica y el movimiento térmico en lugar de estar firmemente anclados. Por lo tanto, se llama la "capa difusa".
Los DL interfaciales son más evidentes en sistemas con una gran relación de área superficial a volumen, como un coloide o cuerpos porosos con partículas o poros (respectivamente) en la escala de micrómetros a nanómetros. Sin embargo, los DL son importantes para otros fenómenos, como el comportamiento electroquímico de los electrodos .
Los DL juegan un papel fundamental en muchas sustancias cotidianas. Por ejemplo, la leche homogeneizada existe solo porque las gotas de grasa están cubiertas con una DL que evita que se coagule en mantequilla. Los DL existen en prácticamente todos los sistemas heterogéneos a base de fluidos, como sangre, pintura, tinta y lodos de cerámica y cemento .
Cuando un conductor electrónico se pone en contacto con un conductor iónico sólido o líquido (electrolito), aparece un límite común ( interfaz ) entre las dos fases . Hermann von Helmholtz [1] fue el primero en darse cuenta de que los electrodos cargados sumergidos en soluciones de electrolitos repelen los co-iones de la carga mientras atraen contraiones a sus superficies. Se forman dos capas de polaridad opuesta en la interfaz entre el electrodo y el electrolito. En 1853 demostró que una doble capa eléctrica (DL) es esencialmente un dieléctrico molecular y almacena carga electrostáticamente. [2] Por debajo del voltaje de descomposición del electrolito, la carga almacenada depende linealmente del voltaje aplicado.
Este primer modelo predijo una capacitancia diferencial constante independiente de la densidad de carga dependiendo de la constante dieléctrica del solvente electrolítico y el espesor de la doble capa. [3] [4] [5]
Este modelo, con una buena base para la descripción de la interfaz, no considera factores importantes como la difusión/mezcla de iones en solución, la posibilidad de adsorción en la superficie y la interacción entre los momentos dipolares del solvente y el electrodo.