cadena de descomposición
En ciencia nuclear , la cadena de desintegración se refiere a una serie de desintegraciones radiactivas de diferentes productos de desintegración radiactiva como una serie secuencial de transformaciones. También se conoce como "cascada radiactiva". La mayoría de los radioisótopos no se desintegran directamente a un estado estable, sino que sufren una serie de desintegraciones hasta que finalmente se alcanza un isótopo estable.
Las etapas de descomposición se denominan por su relación con las etapas anteriores o posteriores. Un isótopo padre es aquel que se desintegra para formar un isótopo hijo . Un ejemplo de esto es el uranio (número atómico 92) que se descompone en torio (número atómico 90). El isótopo hijo puede ser estable o puede decaer para formar un isótopo hijo propio. El hijo de un isótopo hijo a veces se denomina isótopo nieto .
El tiempo que tarda un átomo padre único en desintegrarse en un átomo de su isótopo hijo puede variar ampliamente, no solo entre diferentes pares padre-hijo, sino también aleatoriamente entre parejas idénticas de isótopos padre e hijo. La descomposición de cada átomo individual ocurre espontáneamente, y la descomposición de una población inicial de átomos idénticos a lo largo del tiempo t sigue una distribución exponencial de descomposición, e −λt , donde λ se denomina constante de descomposición . Una de las propiedades de un isótopo es su vida media., el tiempo en el que la mitad de un número inicial de radioisótopos originales idénticos han decaído en sus hijos, que está inversamente relacionado con λ. Se han determinado vidas medias en laboratorios para muchos radioisótopos (o radionúclidos). Estos pueden variar desde casi instantáneos (menos de 10 −21 segundos) hasta más de 10 19 años.
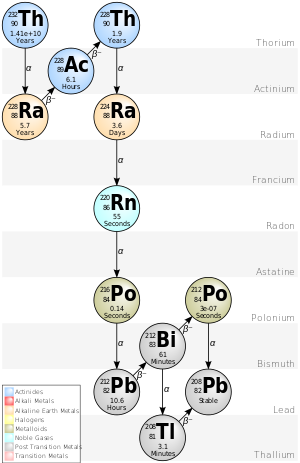
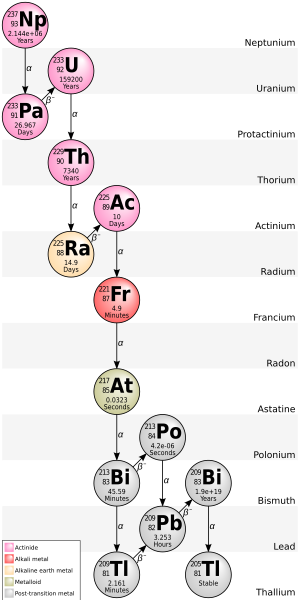
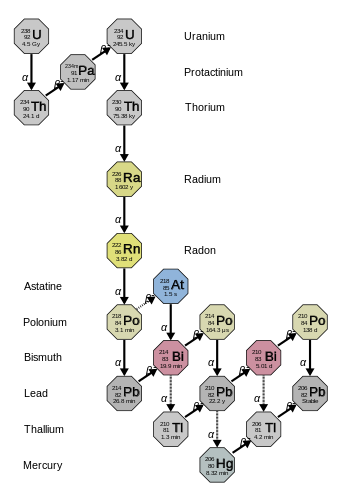
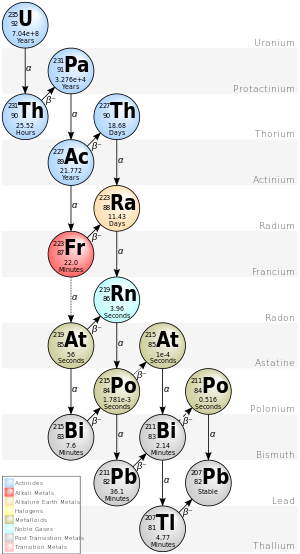
Cada una de las etapas intermedias emite la misma cantidad de radiactividad que el radioisótopo original (es decir, existe una relación de uno a uno entre el número de desintegraciones en etapas sucesivas), pero cada etapa libera una cantidad diferente de energía. Siempre y cuando se logre el equilibrio, cada isótopo hijo sucesivo estará presente en proporción directa a su vida media; pero como su actividad es inversamente proporcional a su vida media, cada nucleido en la cadena de decaimiento contribuye finalmente con tantas transformaciones individuales como la cabeza de la cadena, aunque no con la misma energía. Por ejemplo, el uranio-238 es débilmente radiactivo, pero la pechblenda , un mineral de uranio, es 13 veces más radiactivo que el uranio puro debido al radio.y otros isótopos hijos que contiene. Los isótopos de radio inestables no solo son importantes emisores de radiactividad, sino que, como siguiente etapa en la cadena de descomposición, también generan radón , un gas radiactivo pesado, inerte y natural. Las rocas que contienen torio y/o uranio (como algunos granitos) emiten gas radón que puede acumularse en lugares cerrados como sótanos o minas subterráneas. [1]
La cantidad de isótopos en las cadenas de desintegración en un momento determinado se calcula con la ecuación de Bateman .
Todos los elementos e isótopos que se encuentran en la Tierra, con la excepción del hidrógeno, el deuterio, el helio, el helio-3 y quizás pequeñas cantidades de isótopos estables de litio y berilio que se crearon en el Big Bang , fueron creados por el proceso s o el r-proceso en estrellas o colisiones estelares , y para que esos sean hoy una parte de la Tierra, deben haber sido creados a más tardar hace 4.500 millones de años . Todos los elementos creados hace más de 4.500 millones de años se denominan primordiales ., lo que significa que fueron generados por los procesos estelares del universo. En el momento en que fueron creados, los que eran inestables comenzaron a decaer inmediatamente. Todos los isótopos que tienen una vida media inferior a 100 millones de años se han reducido a2,8 × 10 −12 % o menos de las cantidades originales creadas y capturadas por la acumulación de la Tierra; son trazas en la actualidad, o se han descompuesto por completo. Solo hay otros dos métodos para crear isótopos: artificialmente , dentro de un reactor hecho por el hombre (o tal vez natural ), o mediante la descomposición de una especie isotópica original, el proceso conocido como cadena de descomposición .