 | |
cobalt(III)_chloride.jpg/440px-Trans_dichloribis(ethylenediamine)cobalt(III)_chloride.jpg) | |
| Nombres | |
|---|---|
| Nombre IUPAC ( OC -6-12 ′) - Cloruro de dicloridobis (etano-1,2-diamina-κ 2 N , N ′) cobalto (1+) (1−) | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
PubChem CID | |
| |
| |
| Propiedades | |
| C 4 H 16 Cl 3 CoN 4 | |
| Masa molar | 285,48 g · mol −1 |
| Apariencia | verde sólido |
| Punto de fusion | se descompone |
| bien | |
| Riesgos | |
| Pictogramas GHS |  |
| Palabra de señal GHS | Advertencia |
| H315 , H319 , H335 | |
| P261 , P305 + 351 + 338 | |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
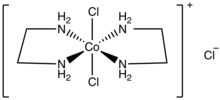
El cloruro de trans- diclorobis (etilendiamina) cobalto (III) es una sal con la fórmula [CoCl 2 (en) 2 ] Cl (en = etilendiamina ). Es un sólido diamagnético verde soluble en agua. Es la sal monocloruro del complejo de coordinación catiónica[CoCl 2 (en) 2 ] + . Un ión cloruro de esta sal experimenta fácilmente intercambio iónico, pero los otros dos cloruros son menos reactivos y están unidos al centro metálico. También se conoce el cloruro de cis- diclorobis (etilendiamina) cobalto (III) más estable.
Síntesis
El compuesto se sintetiza mediante la reacción de cloruro de cobalto (II) y etilendiamina en ácido clorhídrico en presencia de oxígeno:
- 4 CoCl 2 + 8 en + 4 HCl + O 2 → 4 trans - [CoCl 2 (en) 2 ] Cl + 2 H 2 O
El producto inicial contiene HCl, que se elimina por calentamiento. Alternativamente, el cloruro de (carbonato) bis (etilendiamina) cobalto (III) reacciona con ácido clorhídrico a 10 ° C para dar la misma especie. [1]
- [Co (CO 3 ) (en) 2 ] Cl + 2 HCl → trans - [CoCl 2 (en) 2 ] Cl + CO 2 + H 2 O
Comparación de cis y trans isómeros
Esta sal es más soluble que el isómero cis. Este par de isómeros fue importante en el desarrollo del área de la química de coordinación . [2]
El catión de isómero trans tiene simetría de grupo de puntos D 2h idealizada , mientras que el catión de isómero cis tiene simetría de C 2 .
Referencias
- ↑ Springbørg, J .; Schaffer, CE (1973). "Complejos de dianionobis (etilendiamina) cobalto (III)". Síntesis inorgánica . 14 : 63-77. doi : 10.1002 / 9780470132456.ch14 .
- ^ Jörgensen, SM "Ueber Metalldiaminverbindungen" Journal für praktische Chemie (en alemán), 1889, volumen 39, página 8. doi : 10.1002 / prac.18890390101
- Cloruros
- Complejos de cloro
- Complejos de cobalto
- Compuestos de cobalto (III)
- Complejos de etilendiamina
- Halogenuros metálicos
