 | |
| Nombres | |
|---|---|
| Nombre IUPAC Cloruro de uranio (III) | |
| Otros nombres Cloruro de uranio Tricloruro de uranio Cloruro hipouranoso | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| Cl 3 U | |
| Masa molar | 344,38 g · mol −1 |
| Apariencia | Sólido cristalino verde |
| Densidad | 5.500 g / cm 3 , líquido |
| Punto de fusion | 837 ° C (1,539 ° F; 1,110 K) |
| Punto de ebullición | 1.657 ° C (3.015 ° F; 1.930 K) |
| Soluble | |
| Estructura | |
| Hibridación | Prismático trigonal tricapado |
| Peligros | |
| punto de inflamabilidad | No es inflamable |
| No es inflamable | |
| Compuestos relacionados | |
Compuestos relacionados | Cloruro de uranio (IV) , Cloruro de uranio (V) , Cloruro de uranio (VI) |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El cloruro de uranio (III) , UCl 3 , es un compuesto químico que contiene el uranio y el cloro de metales terrosos . El UCl 3 se utiliza principalmente para reprocesar combustible nuclear gastado. El cloruro de uranio (III) se sintetiza de diversas formas a partir del cloruro de uranio (IV) ; sin embargo, el UCl 3 es menos estable que el UCl 4 .
Preparación [ editar ]
Hay dos formas de sintetizar el cloruro de uranio (III). Los siguientes procesos describen cómo producir cloruro de uranio (III).
(1) En una mezcla de NaCl-KCl a 670–710 ° C, agregue tetracloruro de uranio con uranio metálico.
- 3 UCl 4 + U → 4UCl 3 [1]
(2) Caliente el cloruro de uranio (IV) en gas hidrógeno.
- 2 UCl 4 + H 2 → 2UCl 3 + 2 HCl [2]
Propiedades [ editar ]
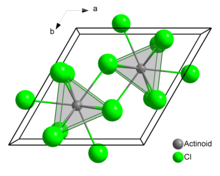
En el cloruro de uranio sólido (III), cada átomo de uranio tiene nueve átomos de cloro como vecinos cercanos, aproximadamente a la misma distancia, en una configuración prismática trigonal tricapada. [3]
El cloruro de uranio (III) es un sólido cristalino verde a temperatura ambiente. El UCl 3 se funde a 837 ° C y hierve a 1657 ° C. El cloruro de uranio (III) tiene una densidad de 5500 kg / m 3 o 5.500 g / cm 3 .
Su composición en peso:
- Cloro: 30,84%
- Uranio: 69,16%
Sus estados oxidativos formales:
- Cloro: -1
- Uranio: +3
El cloruro de uranio (III) es muy soluble en agua y también muy higroscópico . El UCl 3 es más estable en una solución de ácido clorhídrico . [4]
Usos [ editar ]
Reactivo [ editar ]
El cloruro de uranio (III) se usa en reacciones con tetrahidrofurano (THF) y metilciclopentadieno de sodio para preparar varios complejos de uranio metaloceno . [5]
Catalizador [ editar ]
El cloruro de uranio (III) se utiliza como catalizador durante las reacciones entre hidruro de litio y aluminio (LiAlH 4 ) y olefinas para producir compuestos de aluminato de alquilo. [6]
Forma fundida [ editar ]
La forma fundida del cloruro de uranio (III) es un compuesto típico en los procesos piroquímicos, ya que es importante en el reprocesamiento de combustibles nucleares gastados. [7] El UCl 3 suele ser la forma que adopta el uranio como combustible gastado en los procesos de electrorrefinación. [7] [8]
Hidrata [ editar ]
Hay tres hidratos de cloruro de uranio (III):
- UCl 3 . 2H 2 O . 2CH 3 CN
- UCl 3 . 6H 2 O
- UCl 3 . 7H 2 O
Cada uno se sintetiza mediante la reducción de cloruro de uranio (IV) en cianuro de metilo ( acetonitrilo ), con cantidades específicas de agua y ácido propiónico . [9]
Precauciones [ editar ]
Si bien no hay datos a largo plazo sobre los efectos tóxicos del UCl 3 , es importante minimizar la exposición a este compuesto cuando sea posible.
Al igual que otros compuestos de uranio que son solubles, es probable que el UCl 3 se absorba en la sangre a través de las bolsas alveolares de los pulmones a los pocos días de la exposición. La exposición al cloruro de uranio (III) conduce a la toxicidad del sistema renal . [10]
| Wikimedia Commons tiene medios relacionados con el cloruro de uranio (III) . |
Referencias [ editar ]
- ^ Serrano, K .; Taxil, P .; Dugne, O .; Bouvet, S .; Puech, EJ Nucl. Mater. 2000, 282, 137-145.
- ^ Remsen, Ira. Química Inorgánica. Nueva York: Henry Holt and Company, 1890.
- ^ Wells AF (1984) Química inorgánica estructural 5ta edición Publicaciones de ciencia de Oxford ISBN 0-19-855370-6
- ^ Comey, Arthur M .; Hahn, Dorothy A. Diccionario de solubilidades químicas: inorgánico. Nueva York: The MacMillan Company, 1921.
- ^ Brenna, JG; Anderson, RA; Zalkin, A. Inorg. Chem. 1986, 25, 1756-1760.
- ^ Le Marechal, JF; Ephritikhine, M .; Folcher, GJ Organomet. Chem. 1986, 309, C1-C3.
- ^ a b Okamoto, Y .; Madden, P .; Minato, KJ Nucl. Mater. 2005, 344, 109-114.
- ^ Okamoto, Y .; Kobayashi, F .; Ogawa, TJ Alloys Compd. 1998, 271, 355–358.
- ^ Mech, A .; Karbowick, M .; Lis, T. Poliedro. 2006, 25, 2083–2092.
- ^ Bertell, Rosalie. "Veteranos de la Guerra del Golfo y uranio empobrecido". Mayo de 1999. Disponible en: http://ccnr.org/du_hague.html
Enlaces externos [ editar ]
- Información sobre cloruro de uranio (III) en Webelements
- Cloruro de uranio (III) International Bio-Analytical Industries, Inc.
- Uranio empobrecido: todavía no se han respondido todas las preguntas sobre el uranio empobrecido y el síndrome de la guerra del Golfo