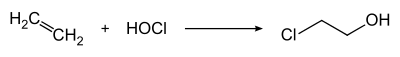| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido 2-cloroetan-1-ol [1] | |||
| Otros nombres | |||
| Identificadores | |||
Modelo 3D ( JSmol ) | |||
| 3DMet | |||
| 878139 | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.003.146 | ||
| Número CE |
| ||
| 25389 | |||
| KEGG | |||
| Malla | Etileno + Clorhidrina | ||
PubChem CID | |||
| Número RTECS |
| ||
| UNII | |||
| un numero | 1135 | ||
Tablero CompTox ( EPA ) | |||
| |||
| |||
| Propiedades | |||
| C 2 H 5 Cl O | |||
| Masa molar | 80,51 g · mol −1 | ||
| Apariencia | Líquido incoloro | ||
| Olor | como el éter | ||
| Densidad | 1,201 g · mL −1 | ||
| Punto de fusion | -62,60 ° C; -80,68 ° F; 210,55 K | ||
| Punto de ebullición | 127-131 ° C; 260–268 ° F; 400–404 K | ||
solubilidad en agua | Miscible [3] | ||
| log P | −0,107 | ||
| Presión de vapor | 700 Pa (a 20 ° C) | ||
Índice de refracción ( n D ) | 1.441 | ||
| Termoquímica | |||
Entalpía estándar de combustión (Δ c H ⦵ 298 ) | −1,1914 MJ · mol −1 | ||
| Riesgos | |||
| Pictogramas GHS |   | ||
| Palabra de señal GHS | Peligro | ||
Declaraciones de peligro GHS | H226 , H300 , H310 , H330 | ||
Consejos de prudencia del SGA | P260 , P280 , P284 , P301 + 310 , P302 + 350 | ||
| NFPA 704 (diamante de fuego) |  4 2 0 | ||
| punto de inflamabilidad | 55 ° C (131 ° F; 328 K) | ||
autoignición temperatura | 425 ° C (797 ° F; 698 K) | ||
| Límites explosivos | 5–16% | ||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis media ) |
| ||
LC 50 ( concentración media ) |
| ||
| NIOSH (límites de exposición a la salud de EE. UU.): | |||
PEL (permitido) | TWA 5 ppm (16 mg / m 3 ) [piel] [3] | ||
REL (recomendado) | C 1 ppm (3 mg / m 3 ) [piel] [3] | ||
IDLH (peligro inmediato) | 7 ppm [3] | ||
| Compuestos relacionados | |||
Compuestos relacionados |
| ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
El 2-cloroetanol es un compuesto químico con la fórmula HOCH 2 CH 2 Cl y la clorhidrina más simple . Este líquido incoloro tiene un agradable olor a éter. Es miscible con agua. La molécula es bifuncional y consta de grupos funcionales de cloruro de alquilo y de alcohol . [6]
Síntesis y aplicaciones
El 2-cloroetanol se produce mediante el tratamiento del etileno con ácido hipocloroso : [6]
El 2-cloroetanol se produjo una vez a gran escala como precursor del óxido de etileno :
Esta aplicación ha sido reemplazada por la oxidación directa más económica del etileno . De lo contrario, el cloroetanol todavía se usa en la producción de productos farmacéuticos , biocidas y plastificantes . [6] Muchas de estas aplicaciones implican su uso en la instalación de grupos 2-hidroxietilo. [7] Se preparan varios tintes mediante la alquilación de derivados de anilina con cloroetanol. [8] También se utiliza para la fabricación de tiodiglicol .
Es un solvente para acetato de celulosa y etilcelulosa , tintes de estampación textil, en desparafinado, refinado de colofonia , extracción de lignina de pino y limpieza de máquinas.
Aspectos ambientales
El cloroetanol es un metabolito en la degradación del 1,2-dicloroetano . A continuación, el alcohol se oxida adicionalmente mediante cloroacetaldehído a cloroacetato. Esta vía metabólica es tópica ya que anualmente se procesan miles de millones de kilogramos de 1,2-dicloroetano como precursor del cloruro de vinilo . [9]
Seguridad
El 2-cloroetanol es tóxico con una DL 50 de 89 mg / kg en ratas. Como la mayoría de los compuestos organoclorados, el cloroetanol se quema para producir cloruro de hidrógeno y fosgeno .
Con respecto a la exposición dérmica al 2-cloroetanol, la Administración de Salud y Seguridad Ocupacional ha establecido un límite de exposición permisible de 5 ppm (16 mg / m 3 ) durante un promedio ponderado de ocho horas, mientras que el Instituto Nacional de Seguridad Ocupacional y La salud tiene un límite de exposición recomendado más protector de un techo de exposición de 1 ppm (3 mg / m 3 ). [10]
Está clasificada como una sustancia extremadamente peligrosa en los Estados Unidos según se define en la Sección 302 de la Ley de Planificación de Emergencias y Derecho a la Información de la Comunidad de EE. UU. (42 USC 11002), y está sujeta a estrictos requisitos de notificación por parte de las instalaciones que producen, almacenan, o utilícelo en cantidades significativas. [11]
Referencias
- ^ a b Nomenclatura de la química orgánica: Recomendaciones de la IUPAC y nombres preferidos 2013 (Libro azul) . Cambridge: La Real Sociedad de Química . 2014. p. 29. doi : 10.1039 / 9781849733069-FP001 . ISBN 978-0-85404-182-4.
Por ejemplo, la omisión del localizador '1' en 2-cloroetanol, aunque es permisible en el uso general, no está permitida en los nombres IUPAC preferidos, por lo que el nombre 2-cloroetan-1-ol es el PIN.
- ^ a b c d e f g h i j k l Sinónimos proporcionados por el depositante para CID 34
- ^ a b c d Guía de bolsillo de NIOSH sobre peligros químicos. "# 0268" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ a b "Etileno clorhidrina" . Concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ "New Environment Inc. - NFPA Chemicals" .
- ^ a b c Liu, Gordon YT; Richey, W. Frank; Betso, Joanne E .; Hughes, Brian; Klapacz, Joanna; Lindner, Joerg (2014). "Clorohidrinas". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a06_565.pub2 .
- ^ Mayordomo J; Kellogg R (1987). "Síntesis de sulfuros macrocíclicos mediante tiolatos de cesio: 1,4,8,11-tetratiaciclotetradecano". Síntesis orgánicas . 65 (150): 150. doi : 10.15227 / orgsyn.065.0150 .
- ^ Raue, Roderich; Corbett, John F. (2002). "Colorantes Nitro y Nitroso". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a17_383 .
- ^ Janssen, DB; van der Ploeg, JR; Pries, F. (1994). "Genética y bioquímica de la degradación del 1,2-dicloroetano" (PDF) . Biodegradación . 5 (3–4): 249–57. doi : 10.1007 / BF00696463 . PMID 7765836 . S2CID 475768 .
- ^ CDC - Guía de bolsillo de NIOSH sobre peligros químicos
- ^ "40 CFR: Apéndice A de la parte 355: la lista de sustancias extremadamente peligrosas y sus cantidades de planificación de umbral" (PDF) . Código de Regulaciones Federales (1 de julio de 2008 ed.). Oficina de Imprenta del Gobierno . Archivado desde el original (PDF) el 25 de febrero de 2012 . Consultado el 29 de octubre de 2011 . [ verificación fallida ]