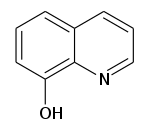
8-hidroxiquinolina
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido Quinolin-8-ol | |
| Otros nombres 1-azanaftaleno-8-ol, fennosano H 30, hidroxibenzopiridina, oxibenzopiridina, oxicinolina, oxiquinolina, fenopiridina, quinofenol, oxina, 8-quinolinol | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.005.193 |
| KEGG | |
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| Propiedades | |
| C 9 H 7 NO | |
| Masa molar | 145,16 g / mol |
| Apariencia | Agujas cristalinas blancas |
| Densidad | 1.034 g / cm 3 |
| Punto de fusion | 76 ° C (169 ° F; 349 K) |
| Punto de ebullición | 276 ° C (529 ° F; 549 K) |
| Farmacología | |
| G01AC30 ( OMS ) A01AB07 ( OMS ) D08AH03 ( OMS ) R02AA14 ( OMS ) | |
| Riesgos | |
| Principales peligros | inflamable |
| Ficha de datos de seguridad | MSDS externa |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
La 8-hidroxiquinolina (también conocida como oxina ) es un agente quelante que se ha utilizado para la determinación cuantitativa de iones metálicos.
En solución acuosa, la 8-hidroxiquinolina tiene un valor de pK de aprox. 9.9 [1] Se reacciona con iones metálicos, perdiendo el protón y la formación de 8-hydroxyquinolinato- quelatos complejos.
El complejo de aluminio [2] es un componente común de los diodos emisores de luz orgánicos (OLED). Las variaciones en los sustituyentes de los anillos de quinolina afectan sus propiedades luminiscentes . [3]
En el estado excitado fotoquímicamente inducido se forman isómeros zwiteriónicos en los que el átomo de hidrógeno se transfiere de oxígeno a nitrógeno. [4]
Los complejos, así como el heterociclo en sí, exhiben propiedades antisépticas , desinfectantes y pesticidas, [5] [6] funcionando como un inhibidor de la transcripción . [7] Su solución en alcohol se utiliza en vendajes líquidos . Alguna vez fue de interés como medicamento contra el cáncer. [8]
También se conoce un análogo de tiol, 8-mercaptoquinolina . [9]
Las raíces de la planta invasora Centaurea diffusa liberan 8-hidroxiquinolina , que tiene un efecto negativo en las plantas que no han co-evolucionado con ella. [10]
Ver también
- Clioquinol , un fármaco antifúngico y fármaco antiprotozoario.
- PBT2
- Ionóforo
Referencias
- ^ Albert, A .; Phillips, JN (1956). "264. Constantes de ionización de sustancias heterocíclicas. Parte II. Derivados hidroxi de compuestos de anillo de seis miembros nitrogenados". Revista de la Sociedad Química (reanudado) . 1956 : 1294–1304. doi : 10.1039 / JR9560001294 .
- ^ Katakura, R .; Koide, Y. (2006). "Síntesis de configuración específica de los isómeros faciales y meridionales de Tris (8-hidroxiquinolinato) aluminio (Alq 3 )". Química inorgánica . 45 (15): 5730–5732. doi : 10.1021 / ic060594s . PMID 16841973 .
- ^ Montes, VA; Pohl, R .; Shinar, J .; Anzenbacher, P. Jr. (2006). "Manipulación eficaz de los efectos electrónicos y su influencia en la emisión de complejos de aluminio (III) tris (8-quinolinolato) 5 sustituidos". Química: una revista europea . 12 (17): 4523–4535. doi : 10.1002 / quím.200501403 . PMID 16619313 .
- ^ Bardez, E .; Devol, I .; Larrey, B .; Valeur, B. (1997). "Procesos de estado excitado en 8-hidroxiquinolina: efectos de solvatación y tautomerización fotoinducida". El Journal of Physical Chemistry B . 101 (39): 7786–7793. doi : 10.1021 / jp971293u .
- ^ Phillips, JP (1956). "Las reacciones del 8-quinolinol". Revisiones químicas . 56 (2): 271-297. doi : 10.1021 / cr50008a003 .
- ^ "8-hidroxiquinolina" . Diccionario médico en línea. Archivado desde el original el 9 de octubre de 2016 . Consultado el 9 de marzo de 2016 .
- ^ "8-hidroxiquinolina" . Sigma-Aldrich . Consultado el 23 de mayo de 2012 .
- ^ Shen, AY; Wu, SN; Chiu, CT (1999). "Evaluación de la síntesis y citotoxicidad de algunos derivados de 8-hidroxiquinolina". Revista de Farmacia y Farmacología . 51 (5): 543–548. doi : 10.1211 / 0022357991772826 . PMID 10411213 .
- ^ Fleischer, Holger "Química estructural de complejos deiones metálicos(n - 1) d 10 ns m con ligandos de tiolato sustituidos de donante β-N (m = 0, 2)" Coordination Chemistry Reviews 2005, volumen 249, págs. 799- 827. doi : 10.1016 / j.ccr.2004.08.024
- ^ Vivanco, JM; Bais, HP; Stermitz, FR; Thelen, GC; Callaway, RM (2004). "Variación biogeográfica en la respuesta de la comunidad a la aleloquímica de la raíz: armas nuevas e invasión exótica". Cartas de ecología . 7 (4): 285-292. doi : 10.1111 / j.1461-0248.2004.00576.x .
- ^ Cölle, M .; Dinnebier, RE; Brütting, W. (2002). "La estructura de la fase δ luminiscente azul del tris (8-hidroxiquinolina) aluminio (III) (Alq 3 )". Comunicaciones químicas . 2002 (23): 2908–9. doi : 10.1039 / b209164j . PMID 12478807 .
- Antisépticos
- Quinolinoles