Translocador de nucleótidos de adenina
| Translocaciones de ADP / ATP | ||||||||
|---|---|---|---|---|---|---|---|---|
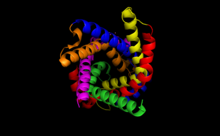 Vista citoplásmica de la bolsa de unión de ATP-ADP translocase 1, PDB : 1OKC . | ||||||||
| Identificadores | ||||||||
| Símbolo | Aden_trnslctor | |||||||
| Pfam | PF00153 | |||||||
| InterPro | IPR002113 | |||||||
| TCDB | 2.A.29.1.2 | |||||||
| Superfamilia OPM | 21 | |||||||
| Proteína OPM | 2c3e | |||||||
| ||||||||
| familia de portadores de solutos 25 (portador mitocondrial; translocador de nucleótidos de adenina), miembro 4 | ||||||
|---|---|---|---|---|---|---|
| Identificadores | ||||||
| Símbolo | SLC25A4 | |||||
| Alt. simbolos | PEO3, PEO2, ANT1 | |||||
| Gen NCBI | 291 | |||||
| HGNC | 10990 | |||||
| OMIM | 103220 | |||||
| RefSeq | NM_001151 | |||||
| UniProt | P12235 | |||||
| Otros datos | ||||||
| Lugar | Chr. 4 q35 | |||||
| ||||||
| familia de portadores de solutos 25 (portador mitocondrial; translocador de nucleótidos de adenina), miembro 5 | ||||||
|---|---|---|---|---|---|---|
| Identificadores | ||||||
| Símbolo | SLC25A5 | |||||
| Alt. simbolos | ANT2 | |||||
| Gen NCBI | 292 | |||||
| HGNC | 10991 | |||||
| OMIM | 300150 | |||||
| RefSeq | NM_001152 | |||||
| UniProt | P05141 | |||||
| Otros datos | ||||||
| Lugar | Chr. X q24-q26 | |||||
| ||||||
| familia de portadores de solutos 25 (portador mitocondrial; translocador de nucleótidos de adenina), miembro 6 | ||||||
|---|---|---|---|---|---|---|
| Identificadores | ||||||
| Símbolo | SLC25A6 | |||||
| Alt. simbolos | ANT3 | |||||
| Gen NCBI | 293 | |||||
| HGNC | 10992 | |||||
| OMIM | 403000 | |||||
| RefSeq | NM_001636 | |||||
| UniProt | P12236 | |||||
| Otros datos | ||||||
| Lugar | Chr. Y p | |||||
| ||||||
El translocador de nucleótidos de adenina ( ANT ), también conocido como translocasa de ADP / ATP ( ANT ), proteína transportadora de ADP / ATP ( AAC ) o transportador de ADP / ATP mitocondrial, intercambia ATP libre con ADP libre a través de la membrana mitocondrial interna . [1] [2] La ANT es la proteína más abundante en la membrana mitocondrial interna y pertenece a la familia de los portadores mitocondriales . [3]
El ADP libre se transporta desde el citoplasma a la matriz mitocondrial, mientras que el ATP producido a partir de la fosforilación oxidativa se transporta desde la matriz mitocondrial al citoplasma , proporcionando así a las células su principal moneda de energía. [4] Las translocaciones de ADP / ATP son exclusivas de los eucariotas y se cree que han evolucionado durante la eucariogénesis . [5] Las células humanas expresan cuatro translocasas de ADP / ATP: SLC25A4 , SLC25A5 , SLC25A6 y SLC25A31 , que constituyen más del 10% de la proteína en la membrana mitocondrial interna. [6]Estas proteínas se clasifican en la superfamilia de portadores mitocondriales .
Tipos
En los humanos, existen tres isoformas ANT paraólogas :
- SLC25A4 : se encuentra principalmente en el corazón y el músculo esquelético.
- SLC25A5 : expresado principalmente en fibroblastos
- SLC25A6 : se expresa principalmente en el hígado
Estructura
Durante mucho tiempo se pensó que la ANT funcionaba como un homodímero, pero este concepto fue desafiado por la estructura de proyección de la levadura Aac3p resuelta por cristalografía electrónica, que mostró que la proteína era tres veces simétrica y monomérica, con la ruta de translocación del sustrato a través de el centro. [7] La estructura atómica del ANT bovino confirmó esta noción y proporcionó el primer pliegue estructural de un portador mitocondrial. [8] Trabajos posteriores han demostrado que ANT es un monómero en los detergentes [9] y funciona como un monómero en las membranas mitocondriales. [10] [11]
ADP / ATP translocase 1 es el principal AAC en las células humanas y la proteína arquetípica de esta familia. Tiene una masa de aproximadamente 30 kDa, que consta de 297 residuos. [12] Forma seis hélices α transmembrana que forman un barril que da como resultado una profunda depresión en forma de cono accesible desde el exterior donde se une el sustrato . La bolsa de unión, conservada en la mayoría de las isoformas , consiste principalmente en residuos básicos que permiten una fuerte unión a ATP o ADP y tiene un diámetro máximo de 20 Å y una profundidad de 30 Å. [8] De hecho, se ha demostrado que los residuos de arginina 96, 204, 252, 253 y 294, así como la lisina 38, son esenciales para la actividad del transportador.[13]
Función
La translocasa de ADP / ATP transporta el ATP sintetizado a partir de la fosforilación oxidativa al citoplasma, donde puede usarse como la principal moneda de energía de la célula para impulsar reacciones termodinámicamente desfavorables. Después de la consiguiente hidrólisis de ATP en ADP, el ADP se transporta de regreso a la matriz mitocondrial, donde se puede refosforilar a ATP. Debido a que un ser humano normalmente intercambia el equivalente de su propia masa de ATP a diario, la translocasa de ADP / ATP es una proteína transportadora importante con importantes implicaciones metabólicas . [4] [8]
ANT transporta las formas libres, es decir, desprotonadas, sin magnesio , sin calcio, de ADP y ATP , en una proporción de 1: 1. [1] El transporte es completamente reversible y su direccionalidad está gobernada por las concentraciones de sus sustratos (ADP y ATP dentro y fuera de las mitocondrias), los quelantes de los nucleótidos de adenina y el potencial de membrana mitocondrial. La relación de estos parámetros puede expresarse mediante una ecuación que resuelva el "potencial de inversión del ANT" (Erev_ANT), un valor del potencial de membrana mitocondrial en el que el ANT no realiza ningún transporte neto de nucleótidos de adenina. [14] [ 15] [16] La ANT y la ATP sintasa F0-F1no están necesariamente en sincronía direccional. [14]
Además del intercambio de ADP y ATP a través de la membrana mitocondrial interna, el ANT también exhibe una actividad de desacoplamiento intrínseca [1] [17]
La ANT es un importante modulador [18] y posible componente estructural del Poro de Transición de Permeabilidad Mitocondrial, un canal involucrado en diversas patologías cuya función aún es difícil de alcanzar. Karch y col. proponen un "modelo de múltiples poros" en el que ANT es al menos uno de los componentes moleculares del poro. [19]
Mecanismo Translocase
En condiciones normales, el ATP y el ADP no pueden atravesar la membrana mitocondrial interna debido a sus altas cargas negativas, pero la translocasa de ADP / ATP, un antiportador , acopla el transporte de las dos moléculas. La depresión en ADP / ATP translocase alternativamente se enfrenta a la matriz y los lados citoplásmicos de la membrana. El ADP en el espacio intermembrana, proveniente del citoplasma, se une a la translocasa e induce su eversión, lo que resulta en la liberación de ADP en la matriz. La unión de ATP de la matriz induce la eversión y da como resultado la liberación de ATP en el espacio intermembrana, que posteriormente se difunde al citoplasma y, concomitantemente, devuelve la translocasa a su conformación original. [4] El ATP y el ADP son los únicos nucleótidos naturales.reconocido por el translocase. [8]
El proceso neto se denota por:
- ADP 3− citoplasma + ATP 4− matriz → ADP 3− matriz + ATP 4− citoplasma
El intercambio de ADP / ATP es energéticamente caro: aproximadamente el 25% de la energía producida por la transferencia de electrones por respiración aeróbica , o un ión de hidrógeno , se consume para regenerar el potencial de membrana que es aprovechado por ADP / ATP translocase. [4]
El translocador circula entre dos estados, llamados estado citoplasmático y de matriz, abriéndose a estos compartimentos de forma alterna. [1] [2] Hay estructuras disponibles que muestran el translocador bloqueado en un estado citoplasmático por el inhibidor carboxatractyloside , [8] [20] o en el estado de matriz por el inhibidor ácido bongkrekic. [21]
Alteraciones
Enfermedades raras pero graves, como las miopatías mitocondriales, se asocian con translocasas de ADP / ATP humano disfuncionales. Las miopatías mitocondriales (MM) se refieren a un grupo de trastornos clínica y bioquímicamente heterogéneos que comparten características comunes de las principales anomalías estructurales mitocondriales en el músculo esquelético . El principal sello morfológico del MM son las fibras rojas irregulares que contienen acumulaciones periféricas e intermiofibrilares de mitocondrias anormales. [22] [23] En particular, oftalmoplejía externa progresiva autosómica dominante (adPEO) es un trastorno común asociado con translocasa disfuncional de ADP / ATP y puede inducir la parálisis de los músculos responsables de los movimientos oculares. Los síntomas generales no se limitan a los ojos y pueden incluir intolerancia al ejercicio, debilidad muscular, déficit auditivo y más. adPEO muestra patrones de herencia mendeliana pero se caracteriza por deleciones de ADN mitocondrial (ADNmt) a gran escala . El ADNmt contiene pocos intrones o regiones de ADN no codificantes, lo que aumenta la probabilidad de mutaciones perjudiciales . Por lo tanto, cualquier modificación del ADNmt de translocasas de ADP / ATP puede conducir a un transportador disfuncional, [24] particularmente residuos involucrados en el bolsillo de unión que comprometerán la eficacia de las translocasas. [13] El MM se asocia comúnmente con translocasas disfuncionales de ADP / ATP, pero el MM puede inducirse a través de muchas anomalías mitocondriales diferentes.
Inhibición
La translocasa de ADP / ATP es inhibida muy específicamente por dos familias de compuestos. La primera familia, que incluye atractyloside (ATR) y carboxatractyloside (CATR), se une a la translocasa de ADP / ATP desde el lado citoplásmico, bloqueándola en una conformación abierta del lado citoplásmico. En contraste, la segunda familia, que incluye el ácido bongkrekico (BA) y el ácido isobongkrekico (isoBA), une la translocasa de la matriz, bloqueándola en una conformación abierta del lado de la matriz. [7] Los grupos cargados negativamente de los inhibidores se unen fuertemente a los residuos cargados positivamente en lo profundo del bolsillo de unión. La alta afinidad ( K den el rango nanomolar) hace que cada inhibidor sea un veneno mortal al obstruir la respiración celular / transferencia de energía al resto de la célula. [8] Hay estructuras disponibles que muestran al translocador bloqueado en un estado citoplásmico por el inhibidor carboxiatractilosido , [8] [20] o en el estado de matriz por el inhibidor ácido bongkrekico. [21]
Historia
En 1955, Siekevitz y Potter demostraron que los nucleótidos de adenina se distribuían en las células en dos grupos ubicados en los compartimentos mitocondrial y citosólico. [25] Poco después, Pressman planteó la hipótesis de que los dos grupos podrían intercambiar nucleótidos. [26] Sin embargo, la existencia de un transportador ADP / ATP no se postuló hasta 1964 cuando Bruni et al. descubrió un efecto inhibidor de atractyloside sobre el sistema de transferencia de energía (fosforilación oxidativa) y los sitios de unión de ADP de las mitocondrias de hígado de rata . [27] Poco después, se realizó una cantidad abrumadora de investigación para probar la existencia y dilucidar el vínculo entre ADP / ATP translocase y el transporte de energía. [28][29] [30] El cDNA de ADP / ATP translocase fue secuenciado para bovinos en 1982 [31] y una especie de levadura Saccharomyces cerevisiae en 1986 [32] antes de que finalmente Battini et al. secuenció un clon de ADNc del transportador humano en 1989. La homología en las secuencias codificantes entre translocasas de ADP / ATP humana y de levadura fue del 47%, mientras que las secuencias bovina y humana se extendieron notablemente hasta 266 de 297 residuos, o el 89,6%. En ambos casos, los residuos más conservados se encuentran en el bolsillo de unión del sustrato de ADP / ATP. [12]
Ver también
- Portador mitocondrial
- Respiración celular
- Fosforilación oxidativa
Referencias
- ↑ a b c d Klingenberg M (octubre de 2008). "El transporte de ADP y ATP en la mitocondria y su portador" . Biochimica et Biophysica Acta (BBA) - Biomembranas . 1778 (10): 1978-2021. doi : 10.1016 / j.bbamem.2008.04.011 . PMID 18510943 .
- ^ a b Kunji ER, Aleksandrova A, King MS, Majd H, Ashton VL, Cerson E, Springett R, Kibalchenko M, Tavoulari S, Crichton PG, Ruprecht JJ (octubre de 2016). "El mecanismo de transporte del portador de ADP / ATP mitocondrial" . Biochimica et Biophysica Acta (BBA) - Investigación de células moleculares . Canales y transportadores en el metabolismo celular. 1863 (10): 2379–93. doi : 10.1016 / j.bbamcr.2016.03.015 . PMID 27001633 .
- ^ Palmieri F, Monné M (octubre de 2016). "Descubrimientos, funciones metabólicas y enfermedades de los portadores mitocondriales: una revisión" . Biochimica et Biophysica Acta (BBA) - Investigación de células moleculares . Canales y transportadores en el metabolismo celular. 1863 (10): 2362–78. doi : 10.1016 / j.bbamcr.2016.03.007 . PMID 26968366 .
- ↑ a b c d Stryer L, Berg JM, Tymoczko JL (2007). Bioquímica . San Francisco: WH Freeman. pag. 553. ISBN 978-0-7167-8724-2.
- ^ Radzvilavicius AL, Blackstone NW (octubre de 2015). "Conflicto y cooperación en eucariogénesis: implicaciones para el momento de la endosimbiosis y la evolución del sexo" . Revista de la Royal Society, Interface . 12 (111): 20150584. doi : 10.1098 / rsif.2015.0584 . PMC 4614496 . PMID 26468067 .
- ^ Brandolin G, Dupont Y, Vignais PV (abril de 1985). "Modificaciones inducidas por el sustrato de la fluorescencia intrínseca de la proteína transportadora de nucleótidos de adenina aislada: demostración de distintos estados conformacionales". Bioquímica . 24 (8): 1991–7. doi : 10.1021 / bi00329a029 . PMID 2990548 .
- ↑ a b Kunji ER, Harding M (septiembre de 2003). "Estructura de proyección del portador de ADP / ATP mitocondrial inhibido por atractilosido de Saccharomyces cerevisiae" . La revista de química biológica . 278 (39): 36985–8. doi : 10.1074 / jbc.C300304200 . PMID 12893834 .
- ↑ a b c d e f g Pebay-Peyroula E, Dahout-Gonzalez C, Kahn R, Trézéguet V, Lauquin GJ, Brandolin G (noviembre de 2003). "Estructura del portador de ADP / ATP mitocondrial en complejo con carboxatractilosido". Naturaleza . 426 (6962): 39–44. Código Bibliográfico : 2003Natur.426 ... 39P . doi : 10.1038 / nature02056 . PMID 14603310 . S2CID 4338748 .
- ^ Bamber L, Slotboom DJ, Kunji ER (agosto de 2007). "Los portadores de ADP / ATP mitocondriales de levadura son monoméricos en los detergentes, como lo demuestra la purificación por afinidad diferencial" . Revista de Biología Molecular . 371 (2): 388–95. doi : 10.1016 / j.jmb.2007.05.072 . PMID 17572439 .
- ^ Bamber L, Harding M, Monné M, Slotboom DJ, Kunji ER (junio de 2007). "El portador de ADP / ATP mitocondrial de levadura funciona como un monómero en las membranas mitocondriales" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 104 (26): 10830–4. Código bibliográfico : 2007PNAS..10410830B . doi : 10.1073 / pnas.0703969104 . PMC 1891095 . PMID 17566106 .
- ^ Kunji ER, Crichton PG (marzo de 2010). "Los portadores mitocondriales funcionan como monómeros" . Biochimica et Biophysica Acta (BBA) - Bioenergética . 1797 (6–7): 817–31. doi : 10.1016 / j.bbabio.2010.03.023 . PMID 20362544 .
- ↑ a b Battini R, Ferrari S, Kaczmarek L, Calabretta B, Chen ST, Baserga R (marzo de 1987). "Clonación molecular de un ADNc para un portador de ADP / ATP humano que está regulado por el crecimiento" . La revista de química biológica . 262 (9): 4355–9. doi : 10.1016 / S0021-9258 (18) 61355-9 . PMID 3031073 .
- ↑ a b Nelson DR, Lawson JE, Klingenberg M, Douglas MG (abril de 1993). "Mutagénesis dirigida al sitio del translocador de ADP / ATP mitocondrial de levadura. Seis argininas y una lisina son esenciales". Revista de Biología Molecular . 230 (4): 1159–70. doi : 10.1006 / jmbi.1993.1233 . PMID 8487299 .
- ^ a b Chinopoulos C, Gerencser AA, Mandi M, Mathe K, Töröcsik B, Doczi J, Turiak L, Kiss G, Konràd C, Vajda S, Vereczki V, Oh RJ, Adam-Vizi V (julio de 2010). "Operación directa de translocasas de nucleótidos de adenina durante la inversión de F0F1-ATPasa: papel crítico de la fosforilación de nivel de sustrato de matriz" . Revista FASEB . 24 (7): 2405–16. doi : 10.1096 / fj.09-149898 . PMC 2887268 . PMID 20207940 .
- ^ Chinopoulos C (mayo de 2011). "Consumo mitocondrial de ATP citosólico: no tan rápido" . Cartas FEBS . 585 (9): 1255–9. doi : 10.1016 / j.febslet.2011.04.004 . PMID 21486564 . S2CID 24773903 .
- ^ Chinopoulos C (diciembre de 2011). "El" espacio B "de la fosforilación mitocondrial" . Revista de Investigación en Neurociencias . 89 (12): 1897–904. doi : 10.1002 / jnr.22659 . PMID 21541983 . S2CID 6721812 .
- ^ Brustovetsky N, Klingenberg M (noviembre de 1994). "El portador de ADP / ATP reconstituido puede mediar el transporte de H + por ácidos grasos libres, que es estimulado adicionalmente por mersalyl" . La revista de química biológica . 269 (44): 27329–36. doi : 10.1016 / S0021-9258 (18) 46989-X . PMID 7961643 .
- ^ Doczi J, Torocsik B, Echaniz-Laguna A, Mousson de Camaret B, Starkov A, Starkova N, Gál A, Molnár MJ, Kawamata H, Manfredi G, Adam-Vizi V, Chinopoulos C (mayo de 2016). "Alteraciones en la detección de voltaje del poro de transición de la permeabilidad mitocondrial en células deficientes en ANT1" . Informes científicos . 6 : 26700. Código Bibliográfico : 2016NatSR ... 626700D . doi : 10.1038 / srep26700 . PMC 4879635 . PMID 27221760 .
- ^ Karch J, Bround MJ, Khalil H, et al. Inhibición de la transición de la permeabilidad mitocondrial por deleción de la familia ANT y CypD. Sci Adv. 2019; 5 (8): eaaw4597. Publicado el 28 de agosto de 2019. doi: 10.1126 / sciadv.aaw4597
- ^ a b Ruprecht JJ, Hellawell AM, Harding M, Crichton PG, McCoy AJ, Kunji ER (enero de 2014). "Las estructuras de los portadores de ADP / ATP mitocondriales de levadura apoyan un mecanismo de transporte de acceso alterno basado en dominios" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 111 (4): E426-34. Código Bibliográfico : 2014PNAS..111E.426R . doi : 10.1073 / pnas.1320692111 . PMC 3910652 . PMID 24474793 .
- ^ a b Ruprecht JJ, King MS, Zögg T, Aleksandrova AA, Pardon E, Crichton PG, Steyaert J, Kunji ER (enero de 2019). "El mecanismo molecular de transporte por el portador de ADP / ATP mitocondrial" . Celular . 176 (3): 435–447.e15. doi : 10.1016 / j.cell.2018.11.025 . PMC 6349463 . PMID 30611538 .
- ^ Harding AE, Petty RK, Morgan-Hughes JA (agosto de 1988). "Miopatía mitocondrial: un estudio genético de 71 casos" . Revista de Genética Médica . 25 (8): 528–35. doi : 10.1136 / jmg.25.8.528 . PMC 1080029 . PMID 3050098 .
- ^ Rose MR (enero de 1998). "Miopatías mitocondriales: mecanismos genéticos" . Archivos de Neurología . 55 (1): 17-24. doi : 10.1001 / archneur.55.1.17 . PMID 9443707 .
- ^ Kaukonen J, Juselius JK, Tiranti V, Kyttälä A, Zeviani M, Comi GP, Keränen S, Peltonen L, Suomalainen A (agosto de 2000). "Papel del translocador de nucleótidos de adenina 1 en el mantenimiento del ADNmt". Ciencia . 289 (5480): 782–5. Código Bibliográfico : 2000Sci ... 289..782K . doi : 10.1126 / science.289.5480.782 . PMID 10926541 .
- ^ Siekevitz P, Potter VR (julio de 1955). "Estructura bioquímica de las mitocondrias. II. Marcado radiactivo de nucleótidos intramitocondriales durante la fosforilación oxidativa" . La revista de química biológica . 215 (1): 237–55. doi : 10.1016 / S0021-9258 (18) 66032-6 . PMID 14392158 .
- ^ Pressman BC (junio de 1958). "Nucleótidos intramitocondriales. I. Algunos factores que afectan las interconversiones netas de nucleótidos de adenina" . La revista de química biológica . 232 (2): 967–78. doi : 10.1016 / S0021-9258 (19) 77415-8 . PMID 13549480 .
- ^ Bruni A, Luciani S, Contessa AR (marzo de 1964). "Inhibición por atractyloside de la unión de adenina-nucleótidos a mitocondrias de hígado de rata". Naturaleza . 201 (1): 1219–20. Código Bibliográfico : 1964Natur.201.1219B . doi : 10.1038 / 2011219a0 . PMID 14151375 . S2CID 4170544 .
- ^ Duee ED, Vignais PV (agosto de 1965). "[Intercambio entre nucleótidos de adenina extra e intramitocondrial]". Biochimica et Biophysica Acta . 107 (1): 184–8. doi : 10.1016 / 0304-4165 (65) 90419-8 . PMID 5857365 .
- ^ Pfaff E, Klingenberg M, Heldt HW (junio de 1965). "Permeación inespecífica e intercambio específico de nucleótidos de adenina en mitocondrias hepáticas". Biochimica et Biophysica Acta (BBA) - Temas generales . 104 (1): 312–5. doi : 10.1016 / 0304-4165 (65) 90258-8 . PMID 5840415 .
- ^ Saks VA, Lipina NV, Smirnov VN, Chazov EI (marzo de 1976). "Estudios de transporte de energía en las células del corazón. El acoplamiento funcional entre la creatinfosfocinasa mitocondrial y ATP ADP translocase: evidencia cinética". Archivos de Bioquímica y Biofísica . 173 (1): 34–41. doi : 10.1016 / 0003-9861 (76) 90231-9 . PMID 1259440 .
- ^ Aquila H, Misra D, Eulitz M, Klingenberg M (marzo de 1982). "Secuencia completa de aminoácidos del portador de ADP / ATP de las mitocondrias de corazón de res". Zeitschrift für Physiologische Chemie de Hoppe-Seyler . 363 (3): 345–9. doi : 10.1515 / bchm2.1982.363.1.345 . PMID 7076130 .
- ^ Adrian GS, McCammon MT, Montgomery DL, Douglas MG (febrero de 1986). "Secuencias necesarias para la entrega y localización del translocador de ADP / ATP a la membrana interna mitocondrial" . Biología Molecular y Celular . 6 (2): 626–34. doi : 10.1128 / mcb.6.2.626 . PMC 367554 . PMID 3023860 .
enlaces externos
- Adenina + Nucleótido + Translocador + 1 en los Encabezamientos de Materia Médica (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- Adenina + Nucleótido + Translocador + 2 en los Encabezamientos de Materia Médica (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- Adenina + Nucleótido + Translocador + 3 en los Encabezamientos de Materia Médica (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- Genes en el cromosoma 4 humano
- Genes en el cromosoma X humano
- Genes en el cromosoma Y humano
- Familia de portadores de solutos
- Respiración celular