 | |
 | |
| Nombres | |
|---|---|
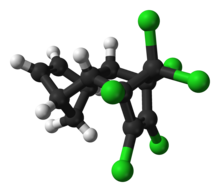
| Nombre IUPAC preferido (1 R , 4 S , 4a S , 5 S , 8 R , 8a R ) -1,2,3,4,10,10-Hexacloro-1,4,4a, 5,8,8a-hexahidro-1, 4: 5,8-dimetanonaftaleno | |
| Otros nombres | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.005.652 |
| Número CE |
|
| KEGG | |
PubChem CID | |
| Número RTECS |
|
| UNII | |
| un numero | 2762, 2761 |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 12 H 8 Cl 6 | |
| Masa molar | 364,90 g · mol −1 |
| Apariencia | Sólido incoloro |
| Densidad | 1,60 g / ml [1] |
| Punto de fusion | 104 ° C (219 ° F; 377 K) |
| ligeramente soluble (0,003%) [1] | |
| Presión de vapor | 7,5 × 10 −5 mmHg a 20 ° C |
| Peligros | |
| Principales peligros | potencial carcinógeno ocupacional [1] |
| Pictogramas GHS |    |
| Palabra de señal GHS | Peligro |
Declaraciones de peligro GHS | H300 , H301 , H301 , H310 , H311 , H351 , H372 , H400 , H410 |
Consejos de prudencia del SGA | P201 , P202 , P260 , P262 , P264 , P270 , P273 , P280 , P281 , P301 + 310 , P302 + 350 , P302 + 352 , P308 + 313 , P310 , P312 , P314 , P321 , P322 , P330 , P361 , P363 , P391 , P405 , P501 |
| NFPA 704 (diamante de fuego) |  4 0 0 |
| punto de inflamabilidad | 66 ° C (151 ° F; 339 K) |
| Dosis o concentración letal (LD, LC): | |
LD 50 ( dosis mediana ) | 50 mg / kg (conejo, oral) 33 mg / kg (conejillo de indias, oral) 39 mg / kg (rata, oral) 44 mg / kg (ratón, oral) [2] |
LC Lo ( más bajo publicado ) | 5,8 mg / m 3 (rata, 4 h) [2] |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
PEL (permitido) | TWA 0,25 mg / m 3 [piel] [1] |
REL (recomendado) | Ca TWA 0,25 mg / m 3 [piel] [1] |
IDLH (peligro inmediato) | 25 mg / m 3 [1] |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El aldrín es un insecticida organoclorado que se usó ampliamente hasta la década de 1990, cuando fue prohibido en la mayoría de los países. Aldrin es un miembro del grupo de plaguicidas llamados "organoclorados clásicos" (COC). Los AOC disfrutaron de un fuerte aumento de popularidad durante y después de la Segunda Guerra Mundial . Otros ejemplos notables de AOC incluyen el DDT . [3] Después de que la investigación mostró que los organoclorados pueden ser altamente tóxicos para el ecosistema a través de la bioacumulación , se prohibió el uso de la mayoría. Es un sólido incoloro. Antes de la prohibición, se usaba mucho como pesticida para tratar semillas y suelo. Plaguicidas de aldrina y "ciclodieno" relacionados (un término para los plaguicidas derivados del hexaclorociclopentadieno) se hizo notorio como contaminantes orgánicos persistentes . [4]
Estructura y reactividad [ editar ]
La fórmula de estructura de la aldrina es C 12 H 8 Cl 6 . La molécula tiene un peso molecular de 364,896 g / mol. El punto de fusión del aldrin es una temperatura de 105 ° C y el coeficiente de reparto octanol-agua es 6.5 (logP). [5]
El aldrín puro toma la forma de un polvo cristalino blanco. Aunque no es soluble en agua (0,003% de solubilidad), la aldrina se disuelve muy bien en disolventes orgánicos, como cetonas y parafinas . [6] El aldrín se descompone muy lentamente una vez que se libera al medio ambiente. Aunque las plantas y las bacterias lo convierten rápidamente en dieldrín , el dieldrín mantiene los mismos efectos tóxicos y la descomposición lenta del aldrina. [7] El aldrín se transporta fácilmente a través del aire mediante partículas de polvo. La aldrina no reacciona con ácidos o bases suaves y es estable en un ambiente con un pH entre 4 y 8. Es altamente inflamable cuando se expone a temperaturas superiores a 200 ° C [5] En presencia de agentes oxidantes el aldrin reacciona con ácidos concentrados y fenoles.
Síntesis [ editar ]
Aldrin no se forma en la naturaleza. Se sintetiza combinando hexaclorociclopentadieno con norbornadieno en una reacción de Diels-Alder para dar el aducto. [8] En 1967, se informó que la composición de la aldrina de grado técnico consistía en un 90,5% de hexaclorohexahidrodimetanonaftaleno (HHDN). [7]
De manera similar, un isómero de aldrina, conocido como isodrina , se produce por reacción del hexaclorobornadieno con ciclopentadieno . [9] La isodrina también se produce como un subproducto de la síntesis de aldrina, y la aldrina de grado técnico contiene aproximadamente un 3,5% de isodrina. [7]
Aldrin lleva el nombre del químico alemán Kurt Alder , uno de los co-inventores de este tipo de reacción. Se estima que entre 1946 y 1976 se produjeron unos 270 millones de kilogramos de aldrina y plaguicidas de ciclodieno relacionados.
Formas disponibles [ editar ]
Hay varias formas disponibles de aldrin. Uno de ellos es el isómero isodrina , que no se puede encontrar en la naturaleza, pero debe sintetizarse como aldrina. Cuando el aldrín ingresa al cuerpo humano o al medio ambiente, se convierte rápidamente en dieldrín . La degradación por radiación ultravioleta o microbios puede convertir la dieldrina en fotodieldrina y la aldrina en fotoaldrina . [7]
Mecanismo de acción [ editar ]
Aunque se han descubierto muchos efectos tóxicos de la aldrina, aún no se han determinado los mecanismos exactos subyacentes a la toxicidad. El único proceso inducido por la aldrina tóxica que se conoce ampliamente es el de la neurotoxicidad.
Neurotoxicidad [ editar ]
Uno de los efectos que produce la intoxicación por aldrina es la neurotoxicidad . Los estudios han demostrado que la aldrina estimula el sistema nervioso central (SNC) , lo que puede provocar hiperexcitación y convulsiones . [10] Este fenómeno ejerce su efecto a través de dos mecanismos diferentes.
Uno de los mecanismos utiliza la capacidad de la aldrina para inhibir las ATPasas de calcio en el cerebro . [11] Estas bombas de iones alivian la terminal nerviosa del calcio al bombearlo activamente. Sin embargo, cuando la aldrina inhibe estas bombas, los niveles de calcio intracelular aumentan. Esto da como resultado una mayor liberación de neurotransmisores .
El segundo mecanismo utiliza la capacidad de la aldrina para bloquear la actividad del ácido gamma-aminobutírico (GABA) . [12] GABA es un neurotransmisor inhibidor importante en el sistema nervioso central. La aldrina induce efectos neurotóxicos al bloquear el complejo del canal de cloruro y receptor GABA A. Al bloquear este receptor, el cloruro no puede entrar en la sinapsis, lo que evita la hiperpolarización de las sinapsis neuronales. Por lo tanto, es más probable que las sinapsis generen potenciales de acción.
Metabolismo [ editar ]
El metabolismo de la exposición oral al aldrina no se ha estudiado en humanos. Sin embargo, los estudios en animales pueden proporcionar una amplia descripción del metabolismo de la aldrina. Estos datos pueden estar relacionados con los humanos.
La biotransformación de la aldrina comienza con la epoxidación de la aldrina por las oxidasas de función mixta ( CYP-450 ), [13] que forma la dieldrina. Esta conversión ocurre principalmente en el hígado. Los tejidos con baja expresión de CYP-450 utilizan en su lugar la prostaglandina endoperóxido sintasa (PES) . [14] Esta vía oxidativa bisdioxigeniza el ácido araquidónico a prostaglandina G 2 (PGG 2 ) . Posteriormente, la PGG 2 se reduce a prostaglandina H 2 (PGH 2 ) por la hidroperoxidasa.
A continuación, la dieldrina puede oxidarse directamente mediante citocromo oxidasas, que forma 9-hidroxidieldrina. Una alternativa para la oxidación implica la apertura del anillo epoxi por hidrasas epoxi, que forma el producto 6,7-trans-dihidroxidroaldrina. [15] Ambos productos pueden conjugarse para formar glucurónido de 6,7-trans-dihidroxidroaldrina y glucurónido de 9-hidroxidieldrina, respectivamente. La 6,7-trans-dihidroxidihidroaldrina también se puede oxidar para formar ácido aldrina dicarboxílico. [16] [17]
Eficacia y efectos secundarios [ editar ]
Teniendo en cuenta la toxicocinética de la aldrina en el medio ambiente, se ha determinado la eficacia del compuesto. Además, se demuestran los efectos adversos tras la exposición al aldrin, lo que indica el riesgo con respecto al compuesto.
Eficacia [ editar ]
Se examina la capacidad del aldrin, en su uso para el control de termitas, con el fin de determinar la respuesta máxima cuando se aplica. En 1953, investigadores estadounidenses probaron el aldrín y el dieldrín en terrenos con ratas conocidas por portar niguas , a una tasa de 2,25 libras por acre. El tratamiento con Aldrin y Dieldrin demostró una disminución de 75 veces menos niguas en ratas para terrenos tratados con Dieldrin y 25 veces menos niguas en las ratas cuando se trataron con Aldrin. El tratamiento con Aldrin indica una alta productividad, especialmente en comparación con otros insecticidas que se utilizaron, como DDT , Sulphur o BHC . [18]
Efectos adversos [ editar ]
La exposición de Aldrin al medio ambiente conduce a la localización del compuesto químico en el aire, el suelo y el agua. [7] El aldrín se cambia rápidamente a dieldrín y ese compuesto se degrada lentamente, lo que explica las concentraciones de aldrín en el ambiente alrededor de la exposición primaria y en las plantas. [19] Estas concentraciones también se pueden encontrar en animales, que comen plantas contaminadas o animales que residen en el agua contaminada. Esta biomagnificación puede dar lugar a concentraciones elevadas en su grasa.
Hay algunos casos reportados de trabajadores que desarrollaron anemia después de múltiples exposiciones al dieldrín. Sin embargo, el principal efecto adverso de Aldrin y Dieldrin está relacionado con el sistema nervioso central. [7] Se creía que los niveles acumulados de Dieldrin en el cuerpo producían convulsiones . [20] Además de que también se informaron otros síntomas como dolores de cabeza, náuseas y vómitos, anorexia, espasmos musculares y espasmos mioclónicos y distorsiones del electroencefalograma . En todos estos casos, la eliminación de la fuente de exposición a aldrín / dieldrín condujo a una rápida recuperación. [21]
Toxicidad [ editar ]
La toxicidad de la aldrina y la dieldrina está determinada por los resultados de varios estudios en animales. No se han encontrado informes de un aumento significativo en la muerte de trabajadores en relación con el aldrin, aunque en algunos casos se informa muerte por anemia después de exposiciones múltiples al aldrin. Las pruebas inmunológicas relacionaron una respuesta antigénica a los eritrocitos recubiertos con dieldrina en esos casos. [22] Aún no se han examinado las relaciones directas entre dosis y respuesta que son una causa de muerte.
El NOAEL que se derivó de estudios en ratas: [7]
- El nivel de riesgo mínimo en la exposición oral aguda a Aldrin es de 0,002 mg / kg / día.
- El nivel de riesgo mínimo en una exposición intermedia a Dieldrin es 0,0001 mg / kg / día.
- El nivel de riesgo mínimo en la exposición crónica a Aldrin es 0,00003 mg / kg / día.
- El nivel de riesgo mínimo en la exposición crónica a Dieldrin es 0.00005 mg / kg / día.
Además de estos estudios, se realizaron estudios de riesgo de cáncer de mama que demostraron un aumento significativo del riesgo de cáncer de mama. Después de comparar las concentraciones sanguíneas con el número de ganglios linfáticos y el tamaño del tumor, se determinó un riesgo de muerte 5 veces mayor, comparando el rango del cuartil más alto en la investigación con el rango del cuartil más bajo. [23] Los niños pequeños también son más susceptibles al fármaco, lo que provoca convulsiones generalizadas graves . [24]
Efectos sobre los animales [ editar ]
La mayoría de los estudios en animales realizados con aldrín y dieldrín utilizaron ratas. Las dosis altas de aldrin y dieldrin demostraron neurotoxicidad , pero en múltiples estudios en ratas también mostraron una sensibilidad única del hígado de ratón a la hepatocarcinogenicidad inducida por dieldrin . [25] Además, las ratas tratadas con Aldrin demostraron una mayor mortalidad posnatal , en la que los adultos mostraron una mayor susceptibilidad a los compuestos en comparación con los niños en las ratas. [26]
Impacto ambiental y regulación [ editar ]
Al igual que los pesticidas policlorados relacionados, la aldrina es altamente lipofílica. Su solubilidad en agua es de solo 0.027 mg / L, lo que agrava su persistencia en el medio ambiente. Fue prohibido por el Convenio de Estocolmo sobre contaminantes orgánicos persistentes . En los Estados Unidos, el aldrin fue cancelado en 1974. La sustancia está prohibida por la UE para su uso para la protección de plantas . [27]
Aspectos medioambientales y de seguridad [ editar ]
Aldrin tiene rata LD 50 de los 39 a 60 mg / kg (oral en ratas). Sin embargo, para los peces es extremadamente tóxico, con una CL50 de 0,006 - 0,01 para la trucha y el bluegill . [4]
En los Estados Unidos, el aldrin es considerado un carcinógeno ocupacional potencial por la Administración de Salud y Seguridad Ocupacional y el Instituto Nacional de Salud y Seguridad Ocupacional ; Estas agencias han establecido un límite de exposición ocupacional para exposiciones dérmicas en 0.25 mg / m 3 durante un promedio ponderado de ocho horas. [28] Además, se ha establecido un límite de IDLH en 25 mg / m 3 , basado en datos de toxicidad aguda en humanos a los que los sujetos reaccionaron con convulsiones dentro de los 20 minutos posteriores a la exposición. [29]
Está clasificada como una sustancia extremadamente peligrosa en los Estados Unidos según se define en la Sección 302 de la Ley de Planificación de Emergencias y Derecho a la Información de la Comunidad de EE. UU. (42 USC 11002), y está sujeta a estrictos requisitos de informes por parte de las instalaciones que producen, almacenan, o utilícelo en cantidades significativas. [30]
Referencias [ editar ]
- ^ a b c d e f g h Guía de bolsillo de NIOSH sobre peligros químicos. "# 0016" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ a b "Aldrin" . Concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Zitko, Vladimir (2003), "Plaguicidas clorados: Aldrin, DDT, Endrin, Dieldrin, Mirex", en Fiedler, H. (ed.), Persistent Organic Pollutants , The Handbook of Environmental Chemistry, 3O , Springer Berlin Heidelberg, págs. . 47–90, doi : 10.1007 / 10751132_4 , ISBN 9783540479321
- ^ a b Robert L. Metcalf "Control de insectos" en la Enciclopedia de química industrial de Ullmann "Wiley-VCH, Weinheim, 2002. doi : 10.1002 / 14356007.a14_263
- ^ a b PubChem. "Aldrin" . pubchem.ncbi.nlm.nih.gov . Consultado el 6 de abril de 2019 .
- ^ "Aldrin (PIM 573)" . www.inchem.org . Consultado el 6 de abril de 2019 .
- ^ a b c d e f g "Perfil toxicológico de aldrin / dieldrin" (PDF) .
- ^ Jubb, AH (1975). Química Orgánica Básica, Parte 5 Productos industriales . Londres: Wiley. ISBN 0-471-85014-4.
- ^ Pájaro, CW; Cookson, RC; Crundwell, E. (1961). "946. Ciclizaciones y reordenamientos en la serie isodrin? Aldrin". Revista de la Sociedad Química (reanudado) : 4809–4816. doi : 10.1039 / JR9610004809 .
- ^ Gupta (mayo de 1975). "Neurotoxicidad de la intoxicación crónica por insecticidas de hidrocarburos clorados: un estudio clínico y electroencefalográfico en el hombre" . The Indian Journal of Medical Research . 63 : 601–606.
- ^ Mehrotra, BD; Ravichandra Reddy, S .; Desaiah, D. (1988). "Efecto del tratamiento con dieldrina subcrónica sobre la actividad de la bomba de Ca2 + regulada por calmodulina en el cerebro de rata". Revista de Toxicología y Salud Ambiental . 25 (4): 461–469. doi : 10.1080 / 15287398809531224 . ISSN 0098-4108 . PMID 2974087 .
- ↑ Glotfelty, Dwight E. (1 de septiembre de 1978). "La atmósfera como fregadero de plaguicidas aplicados". Revista de la Asociación de Control de la Contaminación del Aire . 28 (9): 917–921. doi : 10.1080 / 00022470.1978.11490579 . ISSN 0002-2470 .
- ^ Wong, DT; Terriere, LC (marzo de 1965). "EPOXIDACIÓN DE ALDRINA, ISODRINA Y HEPTACLOR POR MICROSOMAS DE HÍGADO DE RATA". Farmacología bioquímica . 14 (3): 375–377. doi : 10.1016 / 0006-2952 (65) 90210-8 . ISSN 0006-2952 . PMID 14314340 .
- ^ Lang, B .; Frei, K .; Maier, P. (15 de octubre de 1986). "Epoxidación de aldrina dependiente de prostaglandina sintasa en tejidos hepáticos y extrahepáticos de ratas". Farmacología bioquímica . 35 (20): 3643–3645. doi : 10.1016 / 0006-2952 (86) 90640-4 . ISSN 0006-2952 . PMID 3094543 .
- ^ Iatropoulos, MJ (diciembre de 1975). "Absorción, transporte y organotropismo de diclorobifenilo (DCB), dieldrina y hexaclorobenceno (HCB) en ratas". Investigación ambiental . 10 (3): 384–389. Código bibliográfico : 1975ER ..... 10..384I . doi : 10.1016 / 0013-9351 (75) 90033-X . ISSN 0013-9351 . PMID 1213019 .
- ^ Baldwin, MK; Robinson, J .; Parke, DV (junio de 1972). "Una comparación del metabolismo de HEOD (dieldrin) en el ratón CF1 con el de la rata CFE". Toxicología alimentaria y cosmética . 10 (3): 333–351. doi : 10.1016 / S0015-6264 (72) 80252-9 . ISSN 0015-6264 . PMID 5045677 .
- ^ Hutson, DH (diciembre de 1976). "Metabolismo comparativo del dieldrín en la rata (CFE) y en dos cepas de ratón (CF1 y LACG)". Toxicología alimentaria y cosmética . 14 (6): 577–591. doi : 10.1016 / S0015-6264 (76) 80012-0 . ISSN 0015-6264 . PMID 1017774 .
- ^ Traub, Robert; Newson, Harold D .; Walton, Bryce C .; Audy, JR (1 de junio de 1954). "Eficacia de Dieldrin y Aldrin en el control de área de los vectores Chigger del tifus de los matorrales". Revista de Entomología Económica . 47 (3): 429–435. doi : 10.1093 / jee / 47.3.429 . ISSN 1938-291X .
- ^ Castro, Teresita F .; Yoshida, Tomio. (Noviembre de 1971). "Degradación de insecticidas organoclorados en suelos inundados en Filipinas". Revista de Química Agrícola y Alimentaria . 19 (6): 1168-1170. doi : 10.1021 / jf60178a041 . ISSN 0021-8561 . PMID 5132645 .
- ^ Versteeg, JPJ; Jager, KW (1 de abril de 1973). "Exposición ocupacional a largo plazo a los insecticidas aldrin dieldrin, endrin y telodrin" . Medicina ocupacional y ambiental . 30 (2): 201–202. doi : 10.1136 / oem.30.2.201 . ISSN 1351-0711 . PMC 1009505 . PMID 4703092 .
- ^ Avar, P .; Czegledi-Janko, G. (1 de julio de 1970). "Exposición ocupacional al aldrin: hallazgos clínicos y de laboratorio" . Medicina ocupacional y ambiental . 27 (3): 279–282. doi : 10.1136 / oem.27.3.279 . ISSN 1351-0711 . PMC 1009144 . PMID 4194425 .
- ^ Krzystyniak, Krzystof; Hugo, Patrice; Flipo, Denis; Fournier, Michel (septiembre de 1985). "Mayor susceptibilidad al virus de la hepatitis de ratón 3 de los macrófagos peritoneales expuestos al dieldrín" . Toxicología y Farmacología Aplicada . 80 (3): 397–408. doi : 10.1016 / 0041-008x (85) 90384-9 . ISSN 0041-008X . PMC 7173191 . PMID 2994259 .
- ^ Høyer, Annette Pernille; Jørgensen, Torben; Brock, John W .; Grandjean, Philippe (marzo de 2000). "Exposición a organoclorados y supervivencia al cáncer de mama". Revista de epidemiología clínica . 53 (3): 323–330. doi : 10.1016 / s0895-4356 (99) 00165-1 . ISSN 0895-4356 .
- ^ MATSUSHITA, Toshio; TADOKORO, Yasuo (1975). "UN ESTUDIO ELECTROENCEFALOGRÁFICO PARA EL ENVENENAMIENTO CRÓNICO POR NITROGLICOL" . Salud industrial . 13 (4): 237–241. doi : 10.2486 / indhealth.13.237 . ISSN 0019-8366 .
- ^ Black, AMS (noviembre de 1974). "Auto envenenamiento con dieldrín: informe de un caso y discusión farmacocinética" . Anestesia y Cuidados Intensivos . 2 (4): 369–374. doi : 10.1177 / 0310057x7400200413 . ISSN 0310-057X . PMID 4614682 .
- ^ Virgo, Bruce B .; Bellward, Gail D. (octubre de 1975). "Efecto de la dieldrina dietética sobre el hígado y el metabolismo de fármacos en el ratón hembra Swiss-Vancouver". Revista Canadiense de Fisiología y Farmacología . 53 (5): 903–911. doi : 10.1139 / y75-124 . ISSN 0008-4212 . PMID 1201496 .
- ^ Dirección de Regulación de Productos Químicos . "Plaguicidas prohibidos y no autorizados en el Reino Unido" . Consultado el 1 de diciembre de 2009 .
- ^ Centros para el Control y la Prevención de Enfermedades (4 de abril de 2011). "Aldrin" . Guía de bolsillo de NIOSH sobre peligros químicos . Consultado el 13 de noviembre de 2013 .
- ^ Centros para el Control y la Prevención de Enfermedades (mayo de 1994). "Aldrin" . Documentación para concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Consultado el 13 de noviembre de 2013 .
- ^ "40 CFR: Apéndice A de la parte 355: la lista de sustancias extremadamente peligrosas y sus cantidades de planificación de umbral" (PDF) (1 de julio de 2008 ed.). Oficina de Imprenta del Gobierno . Archivado desde el original (PDF) el 25 de febrero de 2012 . Consultado el 29 de octubre de 2011 . Cite journal requiere
|journal=( ayuda )