Complejos de aminoácidos de metales de transición
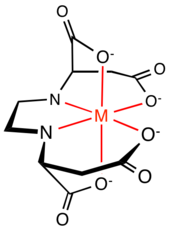
Los complejos de aminoácidos de metales de transición son una gran familia de complejos de coordinación que contienen las bases conjugadas de los aminoácidos , los 2-aminocarboxilatos. Los aminoácidos prevalecen en la naturaleza y todos ellos funcionan como ligandos hacia los metales de transición. [1] No se incluyen en este artículo los complejos de amidas (incluido el péptido) y derivados de éster de aminoácidos. También se excluyen los poliaminoácidos, incluidos los agentes quelantes EDTA y NTA .
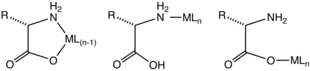
Más comúnmente, los aminoácidos se coordinan con los iones metálicos como ligandos N,O bidentados, utilizando el grupo amino y el carboxilato. Son ligandos "LX". Se forma un anillo de quelato de cinco miembros. El anillo de quelato está sólo ligeramente ondulado en los centros de carbono y nitrógeno con hibridación sp 3 .
Para aquellos aminoácidos que contienen sustituyentes coordinantes, los complejos resultantes son estructuralmente más diversos ya que estos sustituyentes pueden coordinarse. La histidina , el ácido aspártico , la metionina y la cisteína a veces forman complejos tridentados N,N,O, N,O,O, S,N,O y S,N,O, respectivamente.
Utilizando iones metálicos cinéticamente inertes, se han caracterizado complejos que contienen aminoácidos monodentados. Estos complejos existen en los isómeros de enlace N o O. Puede suponerse que dichos complejos monodentados existen transitoriamente para muchos iones metálicos cinéticamente lábiles (p. ej., Zn 2+ ).
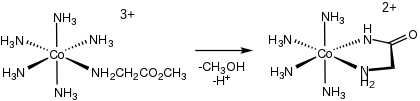
La mezcla de sales metálicas simples con soluciones de aminoácidos con un pH casi neutro o elevado a menudo produce complejos bis o tris. Para los iones metálicos que prefieren la coordinación octaédrica, estos complejos suelen adoptar la estequiometría M(aa) 3 (aa = amino carboxilato, como el glicinato, H 2 NCH 2 CO 2 − ).
Los complejos de la estequiometría 3:1 tienen la fórmula [M(O 2 CC(R)HNH 2 ) 3 ] z . Estos complejos adoptan una geometría de coordinación octaédrica . Estos complejos pueden existir en isómeros faciales y meridionales, ambos quirales. Las posibilidades estereoquímicas aumentan cuando los ligandos de aminoácidos no son homoquirales .