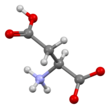
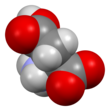
Fórmula esquelética de ácido L- aspártico | |||
| Nombres | |||
|---|---|---|---|
Nombre IUPAC
| |||
Otros nombres
| |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.000.265 | ||
| Número CE |
| ||
| KEGG | |||
PubChem CID | |||
| UNII |
| ||
Tablero CompTox ( EPA ) | |||
| |||
| |||
| Propiedades | |||
| C 4 H 7 N O 4 | |||
| Masa molar | 133,103 g · mol −1 | ||
| Apariencia | cristales incoloros | ||
| Densidad | 1,7 g / cm 3 | ||
| Punto de fusion | 270 ° C (518 ° F; 543 K) | ||
| Punto de ebullición | 324 ° C (615 ° F; 597 K) (se descompone) | ||
solubilidad en agua | 4,5 g / L [2] | ||
| Acidez (p K a ) |
| ||
| Base conjugada | Aspartato | ||
Susceptibilidad magnética (χ) | -64,2 · 10 −6 cm 3 / mol | ||
| Peligros | |||
| Ficha de datos de seguridad | Ver: página de datos | ||
| NFPA 704 (diamante de fuego) |  1 1 0 | ||
| Página de datos complementarios | |||
Estructura y propiedades | Índice de refracción ( n ), constante dieléctrica (ε r ), etc. | ||
Datos termodinámicos | Comportamiento de fase sólido-líquido-gas | ||
Datos espectrales | UV , IR , RMN , MS | ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
El ácido aspártico (símbolo Asp o D ; [4] la forma iónica se conoce como aspartato ), es un α-aminoácido que se utiliza en la biosíntesis de proteínas. [5] Como todos los demás aminoácidos, contiene un grupo amino y un ácido carboxílico. Su grupo α-amino está en el –NH protonado+
3formar en condiciones fisiológicas, mientras que su grupo de ácido α-carboxílico se desprotona -COO - en condiciones fisiológicas. El ácido aspártico tiene una cadena lateral ácida (CH 2 COOH) que reacciona con otros aminoácidos, enzimas y proteínas del cuerpo. [5] En condiciones fisiológicas (pH 7,4) en las proteínas, la cadena lateral suele presentarse como la forma de aspartato cargada negativamente, −COO - . [5] Es un aminoácido no esencial en los seres humanos, lo que significa que el cuerpo puede sintetizarlo según sea necesario. Está codificado por los codones GAT y GAC. En ARNm, CUA y CUG.
El D- aspartato es uno de los dos D -aminoácidos que se encuentran comúnmente en los mamíferos. [3]
En las proteínas, las cadenas laterales de aspartato a menudo están unidas por enlaces de hidrógeno para formar giros asx o motivos asx , que ocurren con frecuencia en los extremos N de las hélices alfa .
El isómero L de Asp es uno de los 22 aminoácidos proteinogénicos , es decir, los componentes básicos de las proteínas . El ácido aspártico, como el ácido glutámico , se clasifica como un aminoácido ácido, con un pK a de 3,9; sin embargo, en un péptido, esto depende en gran medida del entorno local y podría llegar a 14. Asp es un factor dominante en la biosíntesis. Debido a que el cuerpo puede sintetizar el aspartato, se clasifica como un aminoácido no esencial.
Descubrimiento [ editar ]
El ácido aspártico fue descubierto por primera vez en 1827 por Auguste-Arthur Plisson y Étienne Ossian Henry [6] por hidrólisis de asparagina , que había sido aislada del jugo de espárragos en 1806. [7] Su método original usaba hidróxido de plomo , pero varios otros ácidos o bases. ahora se utilizan más comúnmente. [ cita requerida ]
Formularios y nomenclatura [ editar ]
Hay dos formas o enantiómeros de ácido aspártico. El nombre "ácido aspártico" puede referirse a un enantiómero o una mezcla de dos. [8] De estas dos formas, solo una, el " ácido L- aspártico", se incorpora directamente a las proteínas. Las funciones biológicas de su homólogo, el " ácido D- aspártico", son más limitadas. Cuando la síntesis enzimática producirá una u otra, la mayoría de las síntesis químicas producirán ambas formas, " DL -ácido aspártico", conocido como mezcla racémica . [ cita requerida ]
Síntesis [ editar ]
Biosíntesis [ editar ]
En el cuerpo humano, el aspartato se sintetiza con mayor frecuencia mediante la transaminación de oxaloacetato . La biosíntesis de aspartato es facilitada por una enzima aminotransferasa : la transferencia de un grupo amina de otra molécula como alanina o glutamina produce aspartato y un alfa-cetoácido. [5]
El aspartato también juega un papel importante en el ciclo de la urea . [ cita requerida ]
Síntesis química [ editar ]
Industrialmente, el aspartato se produce por aminación de fumarato catalizada por L- aspartato amoniaco liasa . [9]
El ácido aspártico racémico se puede sintetizar a partir de ftalimidomalonato de dietil sodio, (C 6 H 4 (CO) 2 NC (CO 2 Et) 2 ). [10]
Metabolismo [ editar ]
En plantas y microorganismos , el aspartato es el precursor de varios aminoácidos, incluidos cuatro que son esenciales para los humanos: metionina , treonina , isoleucina y lisina . La conversión de aspartato a estos otros aminoácidos comienza con la reducción de aspartato a su "semialdehído", O 2 CCH (NH 2 ) CH 2 CHO. [11] La asparagina se deriva del aspartato mediante transamidación:
- -O 2 CCH (NH 2 ) CH 2 CO 2 - + G C (O) NH 3 + O 2 CCH (NH 2 ) CH 2 CONH 3 + + G C (O) O
(donde G C (O) NH 2 y G C (O) OH son glutamina y ácido glutámico , respectivamente)
Participación en el ciclo de la urea [ editar ]
En el ciclo de la urea , el aspartato y el amoníaco donan grupos amino que conducen a la formación de urea . [ cita requerida ]
Otras funciones bioquímicas [ editar ]
El aspartato tiene muchas otras funciones bioquímicas. Es un metabolito del ciclo de la urea y participa en la gluconeogénesis . Lleva equivalentes reductores en la lanzadera malato-aspartato , que utiliza la interconversión fácil de aspartato y oxalacetato , que es el derivado oxidado (deshidrogenado) del ácido málico . El aspartato dona un átomo de nitrógeno en la biosíntesis de la inosina , el precursor de las bases purínicas . Además, el ácido aspártico actúa como aceptor de hidrógeno en una cadena de ATP sintasa. Se ha demostrado que el ácido L-aspártico de la dieta actúa como inhibidor de la beta-glucuronidasa., que sirve para regular la circulación enterohepática de bilirrubina y ácidos biliares. [12]
Mapa de ruta interactivo [ editar ]
Haga clic en genes, proteínas y metabolitos a continuación para enlazar con los artículos respectivos. [§ 1]
- ^ El mapa de ruta interactivo se puede editar en WikiPathways: "GlycolysisGluconeogenesis_WP534" .
Neurotransmisor [ editar ]
El aspartato (la base conjugada del ácido aspártico) estimula los receptores NMDA , aunque no con tanta fuerza como lo hace el neurotransmisor de aminoácidos L-glutamato . [13]
Aplicaciones y mercado [ editar ]
En 2014, el mercado mundial de ácido aspártico era de 39,3 mil toneladas cortas (35,7 mil toneladas ) [14] o alrededor de $ 117 millones anuales [15] con áreas potenciales de crecimiento que representan un mercado direccionable [ aclaración necesaria ] de $ 8,78 mil millones (Bn) . [16] Los tres segmentos de mercado más importantes son Estados Unidos, Europa occidental y China. Las aplicaciones actuales incluyen polímeros biodegradables ( ácido poliaspártico ), edulcorantes bajos en calorías ( aspartamo ), inhibidores de incrustaciones y corrosión y resinas. [ cita requerida ]
Polímeros superabsorbentes [ editar ]
Un área de crecimiento del mercado del ácido aspártico son los polímeros superabsorbentes biodegradables (SAP). [ síntesis incorrecta? ] Se prevé que el mercado de polímeros superabsorbentes crezca a una tasa de crecimiento anual compuesta del 5,5% entre 2014 y 2019 para alcanzar un valor de 8,78 mil millones de dólares a nivel mundial. [16] Alrededor del 75% de los polímeros superabsorbentes se utilizan en pañales desechables y un 20% adicional se utiliza para la incontinencia de adultos y productos de higiene femenina . El ácido poliaspártico , el producto de polimerización del ácido aspártico, es un sustituto biodegradable del poliacrilato . [17]El mercado de poliaspartato comprende una pequeña fracción (est. <1%) del mercado total de SAP. [ cita requerida ]
Usos adicionales [ editar ]
Además de SAP, el ácido aspártico tiene aplicaciones en la industria de fertilizantes de $ 19 mil millones, donde el poliaspartato mejora la retención de agua y la absorción de nitrógeno; [18] el mercado de revestimientos para pisos de concreto de $ 1.100 millones (2020), donde el poliaspártico es una alternativa baja en COV y baja energía a las resinas epoxi tradicionales; [19] y, por último, el mercado de inhibidores de corrosión e incrustaciones> $ 5 mil millones. [20]
Fuentes [ editar ]
Esta sección necesita citas adicionales para su verificación . ( Enero de 2021 ) ( Obtenga información sobre cómo y cuándo eliminar este mensaje de plantilla ) |
Fuentes dietéticas [ editar ]
El ácido aspártico no es un aminoácido esencial , lo que significa que puede sintetizarse a partir de intermediarios de la vía metabólica central en humanos. Sin embargo, el ácido aspártico se encuentra en:
- Fuentes animales: ostras, fiambres, embutidos, caza silvestre.
- Fuentes vegetales: semillas germinadas, copos de avena , aguacate , [21] espárragos, [22] caña de azúcar tierna y melaza de remolacha azucarera . [1]
- Suplementos dietéticos , ya sea como ácido aspártico en sí o sales (como aspartato de magnesio )
- El edulcorante aspartamo , un ácido aspártico, fenilalanina , trímero de formaldehído (marcas: NutraSweet, Equal, Canderel, etc.)
Ver también [ editar ]
- Aspartato transaminasa
- Ácido poliaspártico
- Poli (aspartato) de sodio , una poliamida sintética
Referencias [ editar ]
- ^ a b Budavari, Susan; Co, Merck (1989). "862. Ácido aspártico" . The Merck Index (11ª ed.). pag. 132 . ISBN 978-0-911910-28-5.
- ^ "ICSC 1439 - ÁCIDO L-ASPARTICO" . inchem.org .
- ^ Haynes, William M., ed. (2016). Manual CRC de Química y Física (97ª ed.). Prensa CRC . págs. 5-89. ISBN 978-1498754286.
- ^ "Nomenclatura y simbolismo de aminoácidos y péptidos" . Comisión Conjunta IUPAC-IUB sobre Nomenclatura Bioquímica. 1983. Archivado desde el original el 9 de octubre de 2008 . Consultado el 5 de marzo de 2018 .
- ^ a b c d G., Voet, Judith; W., Pratt, Charlotte (29 de febrero de 2016). Fundamentos de la bioquímica: vida a nivel molecular . ISBN 9781118918401. OCLC 910538334 .
- ↑ Berzelius JJ , Öngren OG (1839). Traité de chimie (en francés). 3 . Bruselas: A. Wahlen et Cie. P. 81 . Consultado el 25 de agosto de 2015 .
- ^ Plimmer R (1912) [1908]. Plimmer R, Hopkins F (eds.). La composición química de las proteínas . Monografías de Bioquímica. Parte I. Análisis (2ª ed.). Londres: Longmans, Green and Co. p. 112 . Consultado el 18 de enero de 2010 .
- ^ "Nomenclatura y simbolismo de aminoácidos y péptidos (Recomendaciones IUPAC-IUB 1983)", Pure Appl. Chem. , 56 (5): 595–624, 1984, doi : 10.1351 / pac198456050595.
- ^ Karlheinz Drauz, Ian Grayson, Axel Kleemann, Hans-Peter Krimmer, Wolfgang Leuchtenberger, Christoph Weckbecker (2006). Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a02_057.pub2 .CS1 maint: varios nombres: lista de autores ( enlace )
- ^ Dunn MS, Smart BW (1950). "Ácido DL-aspártico" . Síntesis orgánicas . 30 : 7.; Volumen colectivo , 4 , p. 55.
- ^ Lehninger AL, Nelson DL, Cox MM (2000). Principios de bioquímica (3ª ed.). Nueva York: W. H. Freeman. ISBN 1-57259-153-6.
- ^ Kreamer, Siegel y Gourley (octubre de 2001). "Un nuevo inhibidor de la beta-glucuronidasa: ácido L-aspártico" . Investigación pediátrica . 50 (4): 460–466. doi : 10.1203 / 00006450-200110000-00007 . PMID 11568288 . CS1 maint: multiple names: authors list (link)
- ^ Chen PE, Geballe MT, Stansfeld PJ, Johnston AR, Yuan H, Jacob AL, Snyder JP, Traynelis SF, Wyllie DJ (mayo de 2005). "Características estructurales del sitio de unión del glutamato en los receptores N-metil-D-aspartato NR1 / NR2A recombinantes determinados por mutagénesis dirigida al sitio y modelado molecular". Farmacología molecular . 67 (5): 1470–84. doi : 10.1124 / mol.104.008185 . PMID 15703381 . S2CID 13505187 .
- ^ "Mercado global de ácido aspártico por aplicación" . Investigación de Grand View . Consultado el 30 de noviembre de 2019 .
- ^ Evans J (2014). Aminoácidos comerciales . Investigación BCC. págs. 101-103.
- ^ a b Investigación de mercado de transparencia. Mercado de polímeros superabsorbentes: análisis de la industria global, tamaño, participación, crecimiento, tendencias y pronóstico, 2014-2020. (2014).
- ^ Alford DD, Wheeler AP, Pettigrew CA (1994). "Biodegradación de poliaspartato sintetizado térmicamente". J Environ Polym Degr . 2 (4): 225–236. doi : 10.1007 / BF02071970 .
- ^ Kelling K (2001). Respuestas de cultivos a Amisorb en la región centro norte . Universidad de Wisconsin-Madison.
- ^ El mercado global de revestimientos para pisos de concreto tendrá un valor de US $ 1.100 millones para 2020. Transparencia Market Research (2015).
- ^ Análisis de mercado de inhibidores de corrosión por producto, por aplicación, por industria de uso final y pronósticos de segmento hasta 2020. Grand View Research (2014)
- ^ Salunkhe DK, Kadam S (18 de agosto de 1995). Manual de ciencia y tecnología de frutas: producción, composición, almacenamiento y procesamiento . Prensa CRC. págs. 368–. ISBN 978-0-8247-9643-3.
- ^ Considine DM (6 de diciembre de 2012). Enciclopedia de alimentos y producción de alimentos . Springer Science & Business Media. págs. 114–. ISBN 978-1-4684-8511-0.
Enlaces externos [ editar ]
- Espectro de GMD MS
- American Chemical Society (21 de abril de 2010). "Cristal de Eva ancestral puede explicar el origen de la zurda de la vida" . ScienceDaily . Archivado desde el original el 23 de abril de 2010 . Consultado el 21 de abril de 2010 .