| Parte de una serie sobre el |
| Pandemia de COVID-19 |
|---|
|
| Portal COVID-19 |
Una vacuna COVID-19 es una vacuna destinada a proporcionar inmunidad adquirida contra el síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2), el virus que causa la enfermedad por coronavirus 2019 (COVID-19). Antes de la pandemia de COVID-19 , existía un conjunto de conocimientos establecido sobre la estructura y función de los coronavirus que causan enfermedades como el síndrome respiratorio agudo severo (SARS) y el síndrome respiratorio de Oriente Medio (MERS), que permitió el desarrollo acelerado de diversas tecnologías de vacunas durante principios de 2020. [1]El 10 de enero de 2020, los datos de la secuencia genética del SARS-CoV-2 se compartieron a través de GISAID y, para el 19 de marzo, la industria farmacéutica mundial anunció un importante compromiso para abordar el COVID-19. [2]
En marzo de 2021 [update], 308 vacunas candidatas se encontraban en diversas etapas de desarrollo, con 73 en investigación clínica , incluidas 24 en ensayos de fase I , 33 en ensayos de fase I-II y 16 en desarrollo de fase III . [3] En los ensayos de fase III, varias vacunas COVID-19 han demostrado una eficacia de hasta el 95% en la prevención de infecciones sintomáticas por COVID-19. En marzo de 2021 [update], al menos una autoridad reguladora nacional autorizó 12 vacunas para uso público: dos vacunas de ARN (la vacuna Pfizer-BioNTech y la vacuna Moderna ), cuatro vacunas convencionalesvacunas inactivadas ( BBIBP-CorV , CoronaVac , Covaxin y CoviVac ), cuatro vacunas de vectores virales ( Sputnik V , la vacuna Oxford-AstraZeneca , Convidicea y la vacuna Johnson & Johnson ) y dos vacunas de subunidad proteica ( EpiVacCorona y RBD-Dimer ). [3]
Muchos países han implementado planes de distribución por etapas que dan prioridad a las personas con mayor riesgo de complicaciones, como los ancianos, y las personas con alto riesgo de exposición y transmisión, como los trabajadores de la salud. [4] Al 13 de marzo de 2021 [update], se habían administrado 355,16 millones de dosis de la vacuna COVID-19 en todo el mundo, según informes oficiales de las agencias nacionales de salud. [5] AstraZeneca-Oxford anticipa producir 3 mil millones de dosis en 2021, Pfizer-BioNTech 1,3 mil millones de dosis y Sputnik V, Sinopharm, Sinovac y Johnson & Johnson 1 mil millones de dosis cada uno. Moderna tiene como objetivo producir 600 millones de dosis y Convidicea 500 millones de dosis en 2021. [6] [7] Para diciembre de 2020, más de 10 Los países habían pedido con antelación mil millones de dosis de vacunas [8], y aproximadamente la mitad de las dosis compradas por los países de ingresos altos representaban el 14% de la población mundial. [9]
Fondo
Antes de COVID-19, nunca se había producido una vacuna para una enfermedad infecciosa en menos de varios años, y no existía ninguna vacuna para prevenir una infección por coronavirus en humanos. [10] Sin embargo, se han producido vacunas contra varias enfermedades animales causadas por coronavirus, incluido (a partir de 2003) el virus de la bronquitis infecciosa en aves, el coronavirus canino y el coronavirus felino . [11] Los proyectos anteriores para desarrollar vacunas contra virus de la familia Coronaviridae que afectan a los seres humanos se han dirigido al síndrome respiratorio agudo severo (SARS) y al síndrome respiratorio de Oriente Medio (MERS). Vacunas contra el SARS[12] y MERS [13] se han probado en animales no humanos.
Según estudios publicados en 2005 y 2006, la identificación y el desarrollo de nuevas vacunas y medicamentos para tratar el SRAS era una prioridad para los gobiernos y las agencias de salud pública de todo el mundo en ese momento. [14] [15] [16] A partir de 2020, no existe una cura o vacuna protectora que haya demostrado ser segura y eficaz contra el SARS en humanos. [17] [18] Tampoco existe una vacuna probada contra el MERS. [19] Cuando MERS se volvió común, se creía que la investigación existente sobre el SARS podría proporcionar una plantilla útil para desarrollar vacunas y terapias contra una infección por MERS-CoV. [17] [20] En marzo de 2020, había una vacuna MERS (basada en ADN) que completó la Fase I de ensayos clínicos en seres humanos [21] y otros tres en curso, todas las vacunas virales vectorizada es: dos (ChAdOx1-Mers, BVRS-GamVac)-adenovirales vectorizada y uno MVA -vectored (MVA-MERS-S). [22]
Planificación y desarrollo
Desde principios de 2020, el desarrollo de vacunas se ha acelerado a través de una colaboración sin precedentes en la industria farmacéutica multinacional y entre gobiernos. [23] Según la Coalition for Epidemic Preparedness Innovations (CEPI), la distribución geográfica del desarrollo de la vacuna COVID-19 sitúa a las entidades norteamericanas con alrededor del 40% de la actividad en comparación con el 30% en Asia y Australia, el 26% en Europa, y algunos proyectos en América del Sur y África. [23] [24]
Se evalúan varios pasos a lo largo de toda la ruta de desarrollo, que incluyen: [10] [25]
- el nivel de toxicidad aceptable de la vacuna (su seguridad),
- dirigidos a poblaciones vulnerables,
- la necesidad de avances en la eficacia de las vacunas,
- la duración de la protección por vacunación,
- sistemas de administración especiales (como oral o nasal, en lugar de por inyección),
- régimen de dosis,
- características de estabilidad y almacenamiento,
- autorización de uso de emergencia antes de la licencia formal,
- fabricación óptima para escalar a miles de millones de dosis, y
- difusión de la vacuna autorizada.
Desafíos
Ha habido varios desafíos únicos con el desarrollo de la vacuna COVID-19.
La urgencia de crear una vacuna para COVID-19 llevó a calendarios comprimidos que acortaron el cronograma estándar de desarrollo de vacunas, en algunos casos combinando pasos de ensayos clínicos durante meses, un proceso que generalmente se lleva a cabo secuencialmente durante años. [26]
Los plazos para realizar la investigación clínica, que normalmente es un proceso secuencial que requiere años, se están comprimiendo en ensayos de seguridad, eficacia y dosificación que se ejecutan simultáneamente durante meses, lo que potencialmente compromete la garantía de seguridad. [26] [27] Como ejemplo, los desarrolladores de vacunas chinos y el Centro para el Control y la Prevención de Enfermedades del gobierno chino comenzaron sus esfuerzos en enero de 2020, [28] y en marzo estaban buscando a numerosos candidatos en plazos cortos, con el objetivo de mostrar a los chinos fortalezas tecnológicas sobre las de los Estados Unidos, y para tranquilizar al pueblo chino sobre la calidad de las vacunas producidas en China. [26] [29]
El rápido desarrollo y la urgencia de producir una vacuna para la pandemia de COVID-19 pueden aumentar los riesgos y la tasa de fracaso de la administración de una vacuna segura y eficaz. [24] [30] [31] Además, la investigación en las universidades se ve obstaculizada por el distanciamiento físico y el cierre de laboratorios. [32] [33]
Las vacunas deben progresar a través de varias fases de ensayos clínicos para probar la seguridad, inmunogenicidad , efectividad, niveles de dosis y efectos adversos de la vacuna candidata. [34] [35] Los desarrolladores de vacunas deben invertir recursos a nivel internacional para encontrar suficientes participantes para los ensayos clínicos de fase II-III cuando el virus ha demostrado ser un " objetivo móvil " de la tasa de transmisión cambiante entre países y dentro de ellos, lo que obliga a las empresas a competir participantes del ensayo; [36] Los organizadores de ensayos clínicos pueden encontrar personas que no estén dispuestas a vacunarse debido a dudas sobre la vacunación [37]o no creer en la ciencia de la tecnología de las vacunas y su capacidad para prevenir infecciones. [38] Incluso cuando se desarrollan nuevas vacunas durante la pandemia de COVID-19, la autorización de vacunas candidatas a COVID-19 requiere la presentación de un expediente completo de información sobre el desarrollo y la calidad de fabricación. [39] [40] [41]
Organizaciones
A nivel internacional, Access to COVID-19 Tools Accelerator es una iniciativa del G20 y de la Organización Mundial de la Salud (OMS) anunciada en abril de 2020. [42] [43] Es una estructura de apoyo interdisciplinar para permitir que los socios compartan recursos y conocimientos. Consta de cuatro pilares, cada uno gestionado por dos o tres socios colaboradores: vacunas (también llamado " COVAX "), diagnóstico, terapéutica y conector de sistemas de salud. [44] El "Plan de I + D (para el) nuevo Coronavirus" de la OMS de abril de 2020 documentó un "ensayo clínico grande, internacional, de múltiples sitios, aleatorizado individualmente" para permitir "la evaluación simultánea de los beneficios y riesgos de cada vacuna candidata prometedora dentro de 3– 6 meses después de que esté disponible para la prueba ". La coalición de vacunas de la OMS priorizará qué vacunas deben pasar a los ensayos clínicos de fase II y III, y determinará protocolos armonizados de fase III para todas las vacunas que alcancen la etapa de ensayo fundamental . [45]
Los gobiernos nacionales también han participado en el desarrollo de vacunas. Canadá anunció financiación para 96 proyectos de investigación de vacunas en empresas y universidades canadienses, con planes para establecer un "banco de vacunas" que podría utilizarse si se produce otro brote de coronavirus, [46] y para apoyar ensayos clínicos y desarrollar cadenas de fabricación y suministro de vacunas. . [47] China otorgó préstamos a bajo tipo de interés a un desarrollador de vacunas a través de su banco central y "rápidamente puso terrenos a disposición de la empresa" para construir plantas de producción. [27] El gobierno apoya a tres empresas de vacunas e institutos de investigación chinos para financiar la investigación, realizar ensayos clínicos y fabricar. [48]Gran Bretaña formó un grupo de trabajo sobre la vacuna COVID-19 en abril de 2020 para estimular los esfuerzos locales para el desarrollo acelerado de una vacuna a través de colaboraciones de la industria, universidades y agencias gubernamentales. Abarcaba todas las fases del desarrollo, desde la investigación hasta la fabricación. [49] En los Estados Unidos, la Autoridad de Investigación y Desarrollo Biomédico Avanzado (BARDA), una agencia federal que financia la tecnología de lucha contra enfermedades, anunció inversiones para apoyar el desarrollo de la vacuna COVID-19 estadounidense y la fabricación de los candidatos más prometedores. [27] [50] En mayo de 2020, el gobierno anunció la financiación de un programa de vía rápida llamado Operation Warp Speed . [51] [52]
Grandes empresas farmacéuticas con experiencia en la fabricación de vacunas a gran escala, incluidas Johnson & Johnson, AstraZeneca y GlaxoSmithKline (GSK), formaron alianzas con empresas de biotecnología , gobiernos y universidades para acelerar la progresión hacia una vacuna eficaz. [27] [26]
Historia
Después de que se aisló un coronavirus en diciembre de 2019, [53] su secuencia genética se publicó el 11 de enero de 2020, lo que desencadenó una respuesta internacional urgente para prepararse para un brote y acelerar el desarrollo de una vacuna preventiva COVID-19. [54] [55] [56] Desde principios de 2020, el desarrollo de vacunas se ha acelerado a través de una colaboración sin precedentes en la industria farmacéutica multinacional y entre gobiernos. [57] En junio de 2020, corporaciones, gobiernos, organizaciones internacionales de salud y grupos de investigación universitarios habían invertido decenas de miles de millones de dólares para desarrollar docenas de vacunas candidatas y prepararse para los programas de vacunación mundial para inmunizar contra la infección por COVID-19.[55] [58] [59] [60] Según la Coalition for Epidemic Preparedness Innovations (CEPI), la distribución geográfica del desarrollo de la vacuna COVID-19 sitúa a las entidades norteamericanas con alrededor del 40% de la actividad en comparación con el 30% en Asia. y Australia, 26% en Europa y algunos proyectos en Sudamérica y África. [54] [57]
En febrero de 2020, la OMS dijo que no esperaba que una vacuna contra el síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2), el virus causante, estuviera disponible en menos de 18 meses. [61] El rápido crecimiento de la tasa de infección de COVID-19 en todo el mundo durante principios de 2020 estimuló las alianzas internacionales y los esfuerzos gubernamentales para organizar urgentemente recursos para fabricar múltiples vacunas en plazos más cortos, [62] con cuatro candidatos a vacunas que ingresaron a evaluación humana en marzo (ver el cuadro de los ensayos clínicos iniciados en 2020 , a continuación). [54] [63]
El 24 de junio de 2020, China aprobó la vacuna CanSino para uso limitado en el ejército y dos vacunas de virus inactivados para uso de emergencia en ocupaciones de alto riesgo. [64] El 11 de agosto de 2020, Rusia anunció la aprobación de su vacuna Sputnik V para uso de emergencia, aunque un mes después solo se habían distribuido pequeñas cantidades de la vacuna para su uso fuera del ensayo de fase 3. [sesenta y cinco]
La asociación Pfizer-BioNTech presentó una solicitud EUA a la FDA para la vacuna de ARNm BNT162b2 (ingrediente activo tozinameran ) el 20 de noviembre de 2020. [66] [67] El 2 de diciembre de 2020, la Agencia Reguladora de Medicamentos y Productos Sanitarios del Reino Unido (MHRA) otorgó aprobación regulatoria temporal para la vacuna Pfizer-BioNTech , [68] [69] convirtiéndose en el primer país en aprobar esta vacuna y el primer país del mundo occidental en aprobar el uso de cualquier vacuna COVID-19. [70] [71] [72] Al 21 de diciembre, muchos países y la Unión Europea [73] han autorizado o aprobado la vacuna Pfizer – BioNTech COVID-19.Bahrein y los Emiratos Árabes Unidos concedieron la autorización de comercialización de emergencia para BBIBP-CorV, fabricado por Sinopharm . [74] [75] El 11 de diciembre de 2020, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) otorgó una Autorización de uso de emergencia (EUA) para la vacuna Pfizer – BioNTech COVID-19. [76] Una semana después, otorgaron un EUA para mRNA-1273 , la vacuna Moderna. [77] [78] [79]Tipos de vacunas
En enero de 2021, se están investigando y desarrollando nueve plataformas tecnológicas diferentes, con la tecnología de numerosos candidatos sin definir, para crear una vacuna eficaz contra COVID-19. [3] [80] La mayoría de las plataformas de vacunas candidatas en los ensayos clínicos se centran en la proteína del pico de coronavirus y sus variantes como antígeno principal de la infección por COVID-19. [80] Las plataformas que se estaban desarrollando en 2020 incluían tecnologías de ácidos nucleicos ( ARN y ADN mensajeros modificados con nucleósidos ), vectores virales no replicantes , péptidos , proteínas recombinantes ,virus atenuados y virus inactivados . [10] [80] [24] [30]
Muchas tecnologías de vacunas que se están desarrollando para COVID-19 no son como las vacunas que ya se usan para prevenir la influenza, sino que utilizan estrategias de "próxima generación" para lograr precisión en los mecanismos de infección por COVID-19. [80] [24] [30] Las plataformas de vacunas en desarrollo pueden mejorar la flexibilidad para la manipulación de antígenos y la eficacia de los mecanismos dirigidos a la infección por COVID-19 en subgrupos de población susceptibles, como trabajadores de la salud, ancianos, niños, mujeres embarazadas y personas con sistemas inmunológicos debilitados existentes . [80] [24]
Vacunas de ARN
Una vacuna de ARN contiene ARN que, cuando se introduce en un tejido, actúa como ARN mensajero (ARNm) para hacer que las células construyan la proteína extraña y estimulen una respuesta inmune adaptativa que le enseña al cuerpo cómo identificar y destruir el patógeno o las células cancerosas correspondientes. . Las vacunas de ARN a menudo, pero no siempre, usan ARN mensajero modificado con nucleósidos . La entrega de ARNm se logra mediante una coformulación de la molécula en nanopartículas lipídicas que protegen las cadenas de ARN y ayudan a su absorción en las células. [81] [82] [83] [84]
Las vacunas de ARN fueron las primeras vacunas COVID-19 autorizadas en los Estados Unidos y la Unión Europea. [85] [86] A enero de 2021 [update], las vacunas autorizadas de este tipo son la vacuna Pfizer-BioNTech COVID-19
Vacunas de vectores de adenovirus
Estas vacunas son ejemplos de vectores virales que no se replican , que utilizan una capa de adenovirus que contiene ADN que codifica una proteína del SARS-CoV-2. [93] Las vacunas basadas en vectores virales contra COVID-19 no se replican, lo que significa que no producen nuevas partículas de virus, sino que solo producen el antígeno que provoca una respuesta inmunitaria sistémica. [93]
En enero de 2021, las vacunas autorizadas de este tipo son la vacuna COVID-19 británica Oxford-AstraZeneca ,
Las vacunas de Convidicia y Johnson & Johnson son vacunas de una sola inyección que ofrecen una logística menos complicada; y se puede almacenar en refrigeración normal durante varios meses. [100] [101]
Sputnik V usa Ad26 para la primera dosis de la misma manera que la vacuna de Johnson & Johnson y Ad5 para la segunda dosis de la misma forma que Convidicia con una eficacia de dosis única similar y una prueba completa que se está llevando a cabo sobre la eficacia de la dosis única.
Vacunas de virus inactivados
Las vacunas inactivadas consisten en partículas de virus que se han cultivado en cultivo y luego se eliminan mediante un método como el calor o el formaldehído para perder la capacidad de producir enfermedades y, al mismo tiempo, estimular una respuesta inmunitaria. [102]
En enero de 2021, las vacunas autorizadas de este tipo son la CoronaVac china [103] [104] [105] , BBIBP-CorV
Vacunas de subunidades
Las vacunas de subunidades presentan uno o más antígenos sin introducir partículas patógenas completas. Los antígenos involucrados son a menudo subunidades de proteínas , pero pueden ser cualquier molécula que sea un fragmento del patógeno. [110]
A enero de 2021, la única vacuna autorizada de este tipo es la vacuna peptídica EpiVacCorona .
Otros tipos
Otros tipos de vacunas que se encuentran en ensayos clínicos incluyen múltiples vacunas de plásmido de ADN , [115]
Los científicos investigaron si las vacunas existentes para afecciones no relacionadas podrían estimular el sistema inmunológico y disminuir la gravedad de la infección por COVID-19. [124] Existe evidencia experimental de que la vacuna BCG para la tuberculosis tiene efectos no específicos sobre el sistema inmunológico, pero no hay evidencia de que esta vacuna sea eficaz contra COVID-19. [125]
Estado de prueba y autorización
Los ensayos de fase I evalúan principalmente la seguridad y la dosificación preliminar en unas pocas docenas de sujetos sanos, mientras que los ensayos de fase II, después del éxito en la fase I, evalúan la inmunogenicidad , los niveles de dosis (eficacia basada en biomarcadores ) y los efectos adversos de la vacuna candidata, generalmente en cientos. de la gente. [34] [35] Un ensayo de Fase I-II consiste en pruebas preliminares de seguridad e inmunogenicidad, generalmente es aleatorizado, controlado con placebo, mientras se determinan dosis más precisas y efectivas. [35] Los ensayos de fase III generalmente involucran a más participantes en múltiples sitios, incluyen un grupo de controly probar la efectividad de la vacuna para prevenir la enfermedad (un ensayo "intervencionista" o "fundamental"), mientras se monitorean los efectos adversos a la dosis óptima. [34] [35] La definición de seguridad, eficacia y criterios de valoración clínicos de la vacuna en un ensayo de fase III puede variar entre los ensayos de diferentes empresas, como definir el grado de efectos secundarios, la infección o la cantidad de transmisión, y si la vacuna previene infección por COVID-19 moderada o grave. [36] [126] [127]
Un diseño de ensayo clínico en curso puede modificarse como un "diseño adaptativo" si la acumulación de datos en el ensayo proporciona una comprensión temprana sobre la eficacia positiva o negativa del tratamiento. [128] [129] Los diseños adaptativos dentro de los ensayos clínicos de Fase II-III en curso sobre vacunas candidatas pueden acortar la duración de los ensayos y utilizar menos sujetos, posiblemente acelerando las decisiones para la terminación temprana o el éxito, evitando la duplicación de esfuerzos de investigación y mejorando la coordinación de los cambios de diseño para el ensayo de Solidaridad en sus ubicaciones internacionales. [128] [130]
Lista de vacunas autorizadas y aprobadas
Las autoridades reguladoras nacionales han otorgado autorizaciones de uso de emergencia para once vacunas. Seis de ellos han sido aprobados para uso completo o de emergencia por al menos una autoridad reguladora estricta reconocida por la OMS .
|
| Vacuna, desarrolladores / patrocinadores | País de origen | Tipo (tecnología) | Dosis, intervalo | Temperatura de almacenamiento | Fase actual (participantes) | Autorización |
|---|---|---|---|---|---|---|
| Vacuna Pfizer – BioNTech COVID-19 (Comirnaty) BioNTech , Pfizer | Estados Unidos, Alemania | ARN ( ARN mod en nanopartículas lipídicas ) | 2 dosis 3-4 semanas | -70 ± 10 ° C ( ULT ) | Fase III (43.448) Aleatorizado, controlado con placebo. Los resultados positivos de un análisis intermedio se anunciaron el 18 de noviembre de 2020 [136] y se publicaron el 10 de diciembre de 2020, informando una eficacia global del 95%. [137] [138] julio de 2020 - noviembre de 2020, [139] [140] Alemania, Estados Unidos | Emergencia (35)
Completo (12)
|
| Vacuna Sputnik V COVID-19 Instituto de Investigación de Epidemiología y Microbiología Gamaleya | Rusia | Vector de adenovirus ( Ad5 y Ad26 recombinantes ) [201] | 2 dosis 3 semanas | -18 ° C ( congelador ) | Fase III (40.000) Doble ciego aleatorizado, controlado con placebo para evaluar la eficacia, inmunogenicidad y seguridad. [204] El análisis provisional del ensayo se publicó en The Lancet , que indica una eficacia del 91,6% sin efectos secundarios inusuales . [205] Agosto de 2020 - mayo de 2021, Rusia, Bielorrusia, [206] India, [207] [208] Venezuela, [209] [210] Emiratos Árabes Unidos [211] | Emergencia (43)
Completo (8)
|
| Vacuna COVID-19 de Oxford – AstraZeneca (Covishield) Universidad de Oxford , AstraZeneca , CEPI | Reino Unido, Suecia | Vector de adenovirus ( ChAdOx1 ) | 2 dosis 4 a 12 semanas | 2-8 ° C | Fase III (30.000) Intervencionista; estudio aleatorizado y controlado con placebo de eficacia, seguridad e inmunogenicidad. [265] Eficacia general del 76% después de la primera dosis y del 81% después de una segunda dosis tomada 12 semanas o más después de la primera. [266] Mayo de 2020 - agosto de 2021, Brasil (5.000), [267] Reino Unido, India [268] | Emergencia (39)
Completo (10)
|
| BBIBP-CorV Sinopharm : Instituto de Productos Biológicos de Beijing, Instituto de Productos Biológicos de Wuhan | porcelana | SRAS-CoV-2 inactivado ( células vero ) | 2 dosis 3-4 semanas | 2-8 ° C | Fase III (48.000) Aleatorizado, doble ciego, paralelo controlado con placebo, para evaluar la seguridad y la eficacia protectora. El análisis interno de Sinopharm indicó una eficacia del 79%. [328] Julio de 2020 - Julio de 2021, Emiratos Árabes Unidos, Baréin, Jordania, [329] Argentina, [330] Marruecos, [331] Perú [332] | Emergencia (27)
Completo (4)
|
| CoronaVac [103] [104] [105] Sinovac | porcelana | SRAS-CoV-2 inactivado ( células vero ) | 2 dosis 2 semanas | 2-8 ° C | Fase III (33,620) Doble ciego, aleatorizado, controlado con placebo para evaluar la eficacia y seguridad. Los resultados finales de la fase III de Turquía mostraron una eficacia del 83,5%. [365] Indonesia anunció resultados adicionales con una eficacia del 65,3%. [366] Brasil anunció resultados que muestran un 50,4% de eficacia en la prevención de infecciones sintomáticas, un 78% de eficacia en la prevención de casos leves y un 100% de eficacia en la prevención de casos graves. [367] Julio de 2020 - Octubre de 2021, Brasil (15.000); [368] Agosto de 2020 - enero de 2021, Indonesia (1.620); Chile (3.000); [369] Turquía (13.000) [370] | Emergencia (20)
Completo (2)
|
| Vacuna Moderna COVID-19 Moderna , NIAID , BARDA , CEPI | Estados Unidos | ARN ( ARN mod en nanopartículas lipídicas ) | 2 dosis 4 semanas | -20 ± 5 ° C ( congelador ) | Fase III (30.000) Intervencionista; estudio aleatorizado y controlado con placebo de eficacia, seguridad e inmunogenicidad. Los resultados positivos de un análisis intermedio se anunciaron el 15 de noviembre de 2020 [392] y se publicaron el 30 de diciembre de 2020, informando una eficacia global del 94%. [393] Julio de 2020 - Octubre de 2022, Estados Unidos | Emergencia (10)
Completo (5)
|
| Vacuna Johnson & Johnson COVID-19 [98] [99] Janssen Pharmaceutica ( Johnson & Johnson ), BIDMC | Estados Unidos, Bélgica | Vector de adenovirus ( Ad26 recombinante ) [409] | 1 dosis [410] | 2-8 ° C [410] | Fase III (40.000) El 29 de enero de 2021 se anunciaron resultados positivos aleatorios, doble ciego, controlados con placebo. [411] Julio de 2020 - 2023, Estados Unidos, Argentina, Brasil, Chile, Colombia, México, Perú, Filipinas, Sudáfrica, Ucrania | Emergencia (8)
Completo (5)
|
| Ad5-nCoV (Convidicea) CanSino Biologics , Instituto de Biotecnología de Beijing de la Academia de Ciencias Médicas Militares | porcelana | Vector de adenovirus ( Ad5 recombinante ) [424] | 1 dosis [425] | 2-8 ° C [425] | Fase III (40.000) Global multicéntrico, aleatorizado, doble ciego, controlado con placebo para evaluar la eficacia, la seguridad y la inmunogenicidad. En febrero de 2021, el análisis intermedio de los ensayos globales mostró una eficacia del 65,7% contra casos moderados de COVID-19 y una eficacia del 90,98% contra casos graves. [425] marzo-diciembre de 2020, China; Septiembre de 2020 - diciembre de 2021, Pakistán; Septiembre de 2020 - noviembre de 2020, Rusia, [426] China, Argentina, Chile; [427] México; [428] Pakistán; [429] Arabia Saudita [430] [431] | Emergencia (2)
Completo (1)
|
| BBV152 (Covaxin) Bharat Biotech , Consejo Indio de Investigación Médica | India | SRAS-CoV-2 inactivado ( células vero ) | 2 dosis 4 semanas | 2-8 ° C | Fase III (25.800) Aleatorizado, ciego al observador, controlado con placebo [436] La tasa de eficacia provisional es del 81% según la tercera fase del ensayo. [437] Todos los datos del segundo análisis intermedio y final aún no están disponibles a través de una revista revisada por pares. [438] Noviembre de 2020 - marzo de 2021, India. | Emergencia (3)
Completo (0)
|
| EpiVacCorona Instituto de vectores | Rusia | Subunidad ( péptido ) | 2 dosis 3-4 semanas | 2-8 ° C | Fase III (40.000) Doble ciego aleatorizado, controlado con placebo para evaluar la eficacia, la inmunogenicidad y la seguridad, noviembre de 2020 - diciembre de 2021, Rusia [442] | Emergencia (1)
Completo (1)
|
| ZF2001 (RBD-Dimer) [3] Anhui Zhifei Longcom Biopharmaceutical Co. Ltd. | porcelana | Subunidad ( recombinante ) | 3 dosis 30 días | Fase III (29.000) Aleatorizado, doble ciego, controlado con placebo [447] Diciembre de 2020 - Abril de 2022, China, Ecuador, Indonesia, Malasia, Pakistán, Uzbekistán [449] [450] | Emergencia (2)
Completo (0)
| |
| CoviVac [454] Centro Chumakov de la Academia de Ciencias de Rusia | Rusia | SRAS-CoV-2 inactivado | 2 dosis 2 semanas | 2-8 ° C | Fase III (3000) Doble ciego, aleatorizado, controlado con placebo para evaluar la eficacia y la seguridad. | Emergencia (1)
Completo (0)
|
Candidatos a vacuna en ensayos en humanos
| Candidatos, desarrolladores y patrocinadores de vacunas | País de origen | Tipo (tecnología) | Diseño de la fase actual (participantes) | Fase completada [g] (participantes) Respuesta inmune | Pendiente de autorización |
|---|---|---|---|---|---|
| Vacuna Novavax COVID-19 Novavax , CEPI | Estados Unidos | Subunidad [460] [461] [462] / partícula similar a virus [463] [464] ( nanopartícula de proteína de pico recombinante del SARS-CoV-2 con adyuvante ) | Fase III (45.000) Ensayo aleatorizado, ciego al observador y controlado con placebo [465] septiembre de 2020 - enero de 2021, Reino Unido (15.000); Diciembre de 2020 - marzo de 2021, EE. UU., México, (30.000) [466] | Fase I-II (131) IgG y respuesta de anticuerpos neutralizantes con adyuvante después de la dosis de refuerzo . [467] | Emergencia (3)
|
| FINLAY-FR-2 (SOBERANA 02) Instituto Finlay de Vacunas | Cuba | Conjugado | Fase III (44,010) Multicéntrico, adaptativo, de grupos paralelos, aleatorizado, controlado con placebo, doble ciego marzo de 2021 - noviembre de 2021, Cuba | Fase I-II (950) Fase I (40): ensayo controlado no aleatorizado. Enmascaramiento: Abierto. Grupo de control: incontrolado. Diseño del estudio: Adaptativo, secuencial Fase II (910): Ensayo controlado aleatorio. Enmascaramiento: Doble ciego. Grupo de control: placebo. Diseño del estudio: Paralelo. Nov 2020 - Mar 2021, Cuba | |
| Vacuna CureVac COVID-19 (CVnCoV) CureVac , CEPI | Alemania | ARN ( ARN no modificado) [476] | Fase III (36.500) Fase 2b / 3: Ensayo multicéntrico de eficacia y seguridad en adultos, noviembre de 2020 -?, Argentina, Bélgica, Colombia, República Dominicana, Francia, Alemania, México, Países Bajos, Panamá, Perú, España | Fase I-II (944) Fase I (284): escalada de dosis controlada, parcialmente ciega para evaluar la seguridad, reactogenicidad e inmunogenicidad. Fase IIa (660): parcialmente ciego al observador, multicéntrico, controlado, confirmación de dosis. Junio de 2020 - Octubre de 2021, Bélgica (fase I), Alemania (fase I), Panamá (fase IIa), Perú (fase IIa) | Emergencia (1)
|
| Sin nombre Academia China de Ciencias Médicas | porcelana | SARS-CoV-2 inactivado | Fase III (34.020) Aleatorizado, doble ciego, unicéntrico, controlado con placebo, de enero de 2021 a septiembre de 2021, Brasil, Malasia | Fase I-II (942) Aleatorizado, doble ciego, unicéntrico, controlado con placebo, mayo de 2020 - septiembre de 2020, Chengdu | |
| QazCovid-in [482] Instituto de Investigación para Problemas de Seguridad Biológica | Kazajstán | SARS-CoV-2 inactivado | Fase III (3.000) Ensayo aleatorizado, ciego y controlado con placebo [483] diciembre de 2020 - julio de 2021, Kazajstán [483] | Fase I-II (244 [484] ) septiembre de 2020 - noviembre de 2020, Kazajstán | |
| ZyCoV-D Cadila Healthcare | India | ADN ( plásmido que expresa la proteína S del SARS-CoV-2 ) | Fase III (26 000) Ensayo aleatorizado, ciego y controlado con placebo [486] Enero de 2021 -?, India [487] | Fase I-II (1.000) Intervencionista; aleatorizado, doble ciego, controlado con placebo [488] [486] julio de 2020 - enero de 2021, India | |
| CoVLP [489] Medicago , GSK | Canadá, Reino Unido | Partículas similares a virus [h] ( recombinantes , de origen vegetal con AS03 ) | Fase II-III (30,612) Impulsado por eventos, aleatorizado, observador ciego, controlado con placebo [491] noviembre de 2020 - abril de 2022, Canadá | Los anticuerpos neutralizantes de fase I (180) el día 42 después de la primera inyección (día 21 después de la segunda inyección) estaban a niveles 10 veces superiores a los de los supervivientes de COVID-19. | |
| SCB-2019 Clover Biofarmacéuticos, [494] [495] GSK , CEPI | China, Reino Unido | Subunidad ( subunidad trimérica de la proteína Spike con AS03 ) | Fase II-III (22.000) Aleatorizado, doble ciego, controlado De marzo de 2021 a julio de 2022, Bélgica, Brasil, Colombia, República Dominicana, Alemania, Nepal, Panamá, Filipinas, Polonia, Sudáfrica | Fase I (150) junio de 2020 - marzo de 2021, Perth | |
| MVC-COV1901 Medicamentos biológicos de la vacuna | Taiwán | Subunidad ( recombinante ) | Fase II (3700) Prospectivo, doble ciego, multicéntrico, multirregional diciembre de 2020 - junio de 2021, Taiwán, Vietnam | Fase I (45) Prospectiva, de etiqueta abierta, unicéntrico, octubre de 2020 a enero de 2021, Taiwán | |
| IIBR-100 (Brilife) Instituto de Investigaciones Biológicas de Israel | Israel | Vector de estomatitis vesicular ( recombinante ) | Fase II (1000) diciembre de 2020 - primavera de 2021, Israel | Fase I (80) Sujetos (de 18 a 55 años de edad) que reciben aleatoriamente una sola administración de IIBR-100 en dosis baja, media o alta, o solución salina, o dos administraciones en una dosis baja o solución salina, 28 días de diferencia. Octubre-noviembre de 2020, Israel | |
| Nano Covax [499] Nanogen Pharmaceutical Biotechnology JSC | Vietnam | Subunidad ( proteína de pico recombinante del SARS-CoV-2 con adyuvante de aluminio ) [500] [501] | Fase II (560) Aleatorización, doble ciego, multicéntrico, controlado con placebo de febrero a mayo de 2021, Vietnam | Fase I (60) Etiqueta abierta, escalada de dosis, diciembre de 2020 - enero de 2021, Vietnam | |
| INO-4800 [116] [117] Inovio , CEPI , Instituto Nacional de Salud de Corea , Instituto Internacional de Vacunas | Corea del Sur, Estados Unidos | Vacuna de ADN (plásmido administrado por electroporación ) | Fase II-III (401) Aleatorizado, controlado con placebo, multicéntrico. [503] Noviembre de 2020 - septiembre de 2022, Estados Unidos | Fase I-II (280) Fase Ia (120): ensayo de etiqueta abierta. Fase Ib-IIa (160): Ensayo de rango de dosis. [504] Abril de 2020 - Enero de 2021, Estados Unidos, Corea del Sur (fase Ib-IIa) | |
| AG0302-COVID-19 AnGes Inc., [506] AMED | Japón | Vacuna de ADN (plásmido) | Fase II-III (500) Aleatorizado, doble ciego, controlado con placebo [507] noviembre de 2020 - mayo de 2021, Japón | Fase I-II (30) Aleatorizado / no aleatorizado, centro único, dos dosis Junio de 2020 - Noviembre de 2020, Osaka | |
Sanofi Pasteur sin nombre , GSK | Francia, Reino Unido | Subunidad | Fase I-II (1,160) Fase I-IIa (440): Inmunogenicidad y seguridad de las formulaciones de la vacuna de proteína recombinante SARS-CoV-2 (con o sin adyuvante) en adultos sanos de 18 años de edad y mayores. [508] Fase IIb (720): Inmunogenicidad y seguridad de la vacuna de proteína recombinante SARS-CoV-2 con adyuvante AS03 en adultos mayores de 18 años. [509] Septiembre de 2020 - Septiembre de 2022, Estados Unidos | Preclínico | |
| Lunar-COV19 / ARCT-021 [510] [511] Arcturus Therapeutics , Facultad de Medicina de Duke – NUS | Estados Unidos, Singapur | ARN | Fase I-II (798) Fase I / II (92): Aleatorizado, doble ciego, controlado con placebo Fase IIa (106): Extensión abierta [512] Fase IIb (600): Aleatorizado, ciego al observador, controlado con placebo [513] Agosto de 2020 - junio de 2022, Singapur, Estados Unidos (fase IIb) | Preclínico | |
| VBI-2902a VBI Vaccines Inc | Estados Unidos | Partícula parecida a un virus | Fase I-II (780) Aleatorizado, ciego al observador, escalada de dosis, controlado con placebo de marzo de 2021 a junio de 2022, Canadá | Preclínico | |
| GX-19 (GX-19N) Consorcio Genexine, [516] Instituto Internacional de Vacunas | Corea del Sur | Vacuna de ADN | Fase I-II (380) Fase I-II (170-210): multicéntrico, aleatorizado, doble ciego, controlado con placebo, junio de 2020 - marzo de 2021, Seúl | Preclínico | |
| VLA2001 [108] [109] Valneva | Francia | SARS-CoV-2 inactivado | Fase I-II (150) Aleatorizado, multicéntrico, doble ciego, diciembre de 2020 - febrero de 2021, Reino Unido | Preclínico | |
| TAK-919 [517] Takeda | Japón | ARN | Fase I-II (200) Aleatorizado, ciego al observador, controlado con placebo de enero de 2021 a marzo de 2022, Japón | Preclínico | |
| TAK-019 [519] Takeda | Japón | Subunidad | Fase I-II (200) Aleatorizado, ciego al observador, controlado con placebo de febrero de 2021 a abril de 2022, Japón | Preclínico | |
| COVID-19 / aAPC Instituto Médico Genoinmune de Shenzhen [521] | porcelana | Vector lentiviral (con minigen modificadores AAPCS ) | Fase I (100) marzo 2020-2023, Shenzhen | Preclínico | |
| LV-SMENP-DC Instituto Médico Genoinmune de Shenzhen [521] | porcelana | Vector lentiviral (con DC modificadoras de minigen ) | Fase I (100) marzo 2020-2023, Shenzhen | Preclínico | |
| LNP-nCoVsaRNA Unidad de ensayos clínicos del MRC en el Imperial College de Londres | Reino Unido | ARN | Fase I (105) Ensayo aleatorizado, con estudio de aumento de dosis (15) y estudio de seguridad ampliado (al menos 200) junio de 2020 - julio de 2021, Reino Unido | Preclínico | |
| GRAd-COV2 ReiThera, Instituto Nacional de Enfermedades Infecciosas Lazzaro Spallanzani | Italia | Vector de adenovirus ( vector de adenovirus de chimpancé modificado , GRAd) | Fase I (90) Sujetos (dos grupos: de 18 a 55 y de 65 a 85 años) que recibieron aleatoriamente una de las tres dosis crecientes de GRAd-COV2 o un placebo, y luego se controlaron durante un período de 24 semanas. El 93% de los sujetos que recibieron GRAd-COV2 desarrollaron anticuerpos. Ago-diciembre de 2020, Roma | Preclínico | |
| COVAX-19 Vaxine Pty Ltd [527] | Australia | Subunidad ( proteína recombinante ) | Fase I (40) junio de 2020 - julio de 2021, Adelaida | Preclínico | |
| Sin nombre Academia de Ciencias Militares del EPL , Walvax Biotech [529] | porcelana | ARN | Fase I (168) junio de 2020 - diciembre de 2021, China | Preclínico | |
| HGC019 Gennova Biopharmaceuticals, HDT Biotech Corporation [531] | India, Estados Unidos | ARN | Fase I (120) Enero de 2021 -?, India | Preclínico | |
| Bio E COVID-19 Biological E. Limited , Baylor College of Medicine , [535] CEPI | India, Estados Unidos | SARS-CoV-2 inactivado (usando un antígeno) | Fase I-II (360) Ensayo de grupo paralelo, aleatorizado, noviembre de 2020 - febrero de 2021, India | Preclínico | |
| Bangavax Globe Biotech Ltd. de Bangladesh | Bangladesh | ARN | Fase I (100) Ensayo de grupo paralelo aleatorizado de febrero de 2021 a febrero de 2022, [540] Bangladesh | Preclínico | |
| PTX-COVID19-B [541] Providence Therapeutics | Canadá | ARN | Fase I (60) Enero de 2021 - Mayo de 2021, Canadá | Preclínico | |
| COVAC-2 [542] VIDO ( Universidad de Saskatchewan ) | Canadá | Subunidad | Fase I (108) Febrero de 2021 - Enero de 2022, Halifax | Preclínico | |
| COVI-VAC Codagenix Inc. | Estados Unidos | Atenuado | Fase I (48) Primera escalada de dosis en humanos, aleatorizada, doble ciego, controlada con placebo, diciembre de 2020 - junio de 2021, Reino Unido | Preclínico | |
| CoV2 SAM (LNP) GSK | Reino Unido | ARN | Fase I (48) Etiqueta abierta, escalada de dosis, no aleatorizado, de febrero de 2021 a junio de 2021, Estados Unidos | Preclínico | |
| COVIran Barakat [545] Barakat Pharmaceutical Group , Shifa Pharmed Industrial Group | Iran | SARS-CoV-2 inactivado | Fase I (56) diciembre de 2020 -?, Irán | Preclínico | |
| BBV154 Bharat Biotech [547] | India | Vector de adenovirus (intranasal) | Fase I (175) Marzo de 2021 - Mayo de 2021, India | Preclínico | |
| SARS-CoV-2 Sclamp / V451 UQ , Syneos Health , CEPI , Seqirus | Australia | Subunidad ( proteína de pico estabilizada por pinza molecular con MF59 ) | Terminado (120) Aleatorizado, doble ciego, controlado con placebo, con rango de dosis. Se encontró una prueba de VIH falsa positiva entre los participantes. De julio a octubre de 2020, Brisbane | ? | |
| V590 [548] y V591 / MV-SARS-CoV-2 [549] Merck & Co. (Themis BIOscience), Institut Pasteur , Centro de Investigación de Vacunas (CVR) de la Universidad de Pittsburgh, CEPI | Estados Unidos, Francia | Vector del virus de la estomatitis vesicular [550] / Vector del virus del sarampión [551] | Terminado En la fase I, las respuestas inmunitarias fueron inferiores a las observadas después de una infección natural y a las notificadas para otras vacunas contra el SARS-CoV-2 / COVID-19. [552] |
- ^ a b Intervalo recomendado. La segunda dosis de las vacunas Pfizer-BioNTech y Moderna se puede administrar hasta 6 semanas después de la primera dosis para aliviar la escasez de suministros. [132] [133]
- ^ Temperatura de almacenamiento a largo plazo. La vacuna Pfizer – BioNTech COVID-19 se puede conservar entre −25 y −15 ° C (−13 y 5 ° F) hasta dos semanas antes de su uso, y entre 2 y 8 ° C (36 y 46 ° F) para hasta cinco días antes de su uso. [134] [135]
- ^ a b c La autorización de EE. UU. también incluye a las tres naciones soberanas del Pacto de Libre Asociación : Palau , las Islas Marshall y Micronesia . [177] [178]
- ^ Temperatura de almacenamiento para la formulación congelada de Gam-COVID-Vac. Laformulación liofilizada de Gam-COVID-Vac-Lyo se puede almacenar a 2-8 ° C. [203]
- ^ Serum Institute of India producirá la vacuna ChAdOx1 nCoV-19 para India [260] y otros países de ingresos bajos y medios. [261]
- ^ Nombre de Oxford: ChAdOx1 nCoV-19 . Fabricación en Brasil a cargo de la Fundación Oswaldo Cruz . [262]
- ^ Última fase con resultados publicados.
- ^ Partículas similares a virus cultivadas en Nicotiana benthamiana [490]
- ^ Fase I-IIa en Corea del Sur en paralelo con la Fase II-III en los EE. UU.
Eficacia
La efectividad de una nueva vacuna se define por su eficacia durante los ensayos clínicos. [140] La eficacia es el riesgo de contraer la enfermedad por los participantes vacunados en el ensayo en comparación con el riesgo de contraer la enfermedad por los participantes no vacunados. [140] Una eficacia del 0% significa que la vacuna no funciona (idéntica al placebo). Una eficacia del 50% significa que hay la mitad de casos de infección que en personas no vacunadas.
No es sencillo comparar la eficacia de las diferentes vacunas porque los ensayos se realizaron con diferentes poblaciones, geografías y variantes del virus. [554] En el caso de COVID-19, una eficacia de la vacuna del 67% puede ser suficiente para frenar la pandemia, pero esto supone que la vacuna confiere inmunidad esterilizante , que es necesaria para prevenir la transmisión. La eficacia de la vacuna refleja la prevención de enfermedades, un mal indicador de la transmisibilidad del SARS-CoV-2, ya que las personas asintomáticas pueden ser muy infecciosas. [555] La Administración de Drogas y Alimentos de los Estados Unidos (FDA) y la Agencia Europea de Medicamentos (EMA) establecieron un límite del 50% como la eficacia requerida para aprobar una vacuna COVID-19.[556] [557] Con el objetivo de lograr una tasa de cobertura de vacunación de la población realista del 75%, y dependiendo del número de reproducción básico real, se espera que la efectividad necesaria de una vacuna COVID-19 sea de al menos el 70% para prevenir una epidemia y en al menos un 80% para extinguirlo sin más medidas, como el distanciamiento social. [558]
En los cálculos de eficacia, el COVID-19 sintomático se define generalmente como tener una prueba de PCR positiva y al menos uno o dos de una lista definida de síntomas de COVID-19 , aunque las especificaciones exactas varían entre los ensayos. La ubicación del ensayo también afecta la eficacia informada porque diferentes países tienen diferentes prevalencias de variantes del SARS-CoV-2 . Los rangos siguientes son intervalos de confianza del 95% a menos que se indique lo contrario, y todos los valores son para todos los participantes independientemente de su edad. La eficacia frente a COVID-19 severo es la más importante, ya que las hospitalizaciones y las muertes son una carga de salud pública cuya prevención es una prioridad. [559] Las vacunas autorizadas y aprobadas han mostrado la siguiente eficacia:
| Vacuna | Eficacia por gravedad de COVID-19 | Lugar de prueba | Refs | |
|---|---|---|---|---|
| Leve o moderada [A] | Grave [B] | |||
| Vacuna moderna | ~ 94% (89 a 97%) | ~ 100% [C] | Estados Unidos | [560] |
| Vacuna Pfizer – BioNTech | ~ 95% (90-98%) | No reportado | Multinacional | [561] |
| Sputnik V | ~ 92% (86–95%) | ~ 100% (94-100%) | Rusia | [562] |
| Vacuna Oxford-AstraZeneca | ~ 81% (60-91%) [D] | ~ 100% (72-100%) [E] | Multinacional | [266] |
| Vacuna Novavax | ~ 89% (75–95%) | ~ 100% [C] | Reino Unido | [563] [564] |
| ~ 60% (20–80%) | ~ 100% [C] | Sudáfrica | ||
| BBIBP-CorV | ~ 79% | ~ 100% [565] | Multinacional | [566] [ fuente médica no confiable? ] |
| CoronaVac | ~ 78% | ~ 100% | Brasil | [567] [568] [569] [ fuente médica no confiable? ] |
| Vacuna Johnson & Johnson | ~ 66% (55-75%) [F] | ~ 85% (54–97%) | Multinacional | [570] |
| ~ 72% (58-82%) [F] | ~ 86% (−9–100%) [G] | Estados Unidos | ||
| ~ 68% (49-81%) [F] | ~ 88% (8-100%) | Brasil | ||
| ~ 64% (41-79%) [F] | ~ 82% (46–95%) | Sudáfrica | ||
| Covaxina | ~ 81% | No reportado | India | [571] [572] [ fuente médica no confiable? ] |
| Convidicea | ~ 66% | ~ 91% | Multinacional | [425] [ fuente médica no confiable? ] |
- ^ Síntomas leves: fiebre, tos seca, fatiga, mialgia, artralgia, dolor de garganta, diarrea, náuseas, vómitos, dolor de cabeza, anosmia, ageusia, congestión nasal, rinorrea, conjuntivitis, erupción cutánea, escalofríos, mareos. Síntomas moderados: neumonía leve.
- ^ Los síntomas graves son aquellos que requieren hospitalización o que provocan la muerte: disnea, hipoxia, dolor torácico persistente, anorexia, confusión, fiebre superior a 38 ° C (100 ° F), insuficiencia respiratoria, insuficiencia renal, disfunción multiorgánica, sepsis, shock.
- ^ a b c No se detectaron casos en el juicio.
- ^ Con 12 semanas o más de intervalo entre dosis. Durante un intervalo de menos de 6 semanas, el ensayo encontró una eficacia del 55% (33-70%).
- ^ Intervalo de confianza del 97,5%
- ^ a b c d Casos moderados.
- ^ La fuente en realidad dice negativo 9.
Variantes
La aparición de una variante del SARS-CoV-2 que sea moderada o totalmente resistente a la respuesta de anticuerpos provocada por la generación actual de vacunas COVID-19 puede requerir la modificación de las vacunas. [573] Los ensayos indican que muchas vacunas desarrolladas para la cepa inicial tienen menor eficacia para algunas variantes contra el COVID-19 sintomático. [574] En febrero de 2021, la Administración de Drogas y Alimentos de los EE. UU . Creía que todas las vacunas autorizadas por la FDA seguían siendo eficaces para proteger contra las cepas circulantes del SARS-CoV-2. [573]
En diciembre de 2020, se identificó una nueva variante del SARS-CoV-2 , B.1.1.7 , en el Reino Unido. [575] Los primeros resultados sugieren la protección de la variante del Reino Unido de las vacunas Pfizer y Moderna. [576] Un estudio indicó que la vacuna Oxford-AstraZeneca tenía una eficacia de 42 a 89% contra la variante B.1.1.7, en comparación con 71 a 91% contra variantes no B.1.1.7. [577] Los datos preliminares de un ensayo clínico indicaron que la vacuna Novavax fue ~ 96% efectiva para los síntomas contra la variante original, ~ 86% contra B.1.1.7 y ~ 60% contra la variante "sudafricana" B.1.351 . [578]
Variante 501.V2
Moderna ha lanzado una prueba de una nueva vacuna para combatir la variante sudafricana 501.V2 (también conocida como B.1.351). [579] El 17 de febrero de 2021, Pfizer anunció que la actividad de neutralización se redujo en dos tercios para la variante 501.V2, mientras que aún no afirmó que se podía hacer ninguna afirmación sobre la eficacia de la vacuna para prevenir la enfermedad de esta variante. [580]
En enero, Johnson & Johnson, que realizó ensayos para su vacuna Ad26.COV2.S en Sudáfrica, informó que el nivel de protección contra la infección por COVID-19 de moderada a grave era del 72% en los Estados Unidos y del 57% en Sudáfrica. [581]
El 6 de febrero de 2021, el Financial Times informó que los datos del ensayo provisional de un estudio realizado por la Universidad de Witwatersrand de Sudáfrica junto con la Universidad de Oxford demostraron una eficacia reducida de la vacuna COVID-19 de Oxford-AstraZeneca contra la variante 501.V2 . [582] El estudio encontró que en un tamaño de muestra de 2000, la vacuna AZD1222 ofrecía sólo una "protección mínima" en todos los casos de COVID-19, excepto en los más graves. [583] El 7 de febrero de 2021, el Ministro de SaludSudáfrica suspendió el despliegue planificado de alrededor de 1 millón de dosis de la vacuna mientras examinan los datos y esperan asesoramiento sobre cómo proceder. [584] [585]
Formulación
En septiembre de 2020 [update], once de las vacunas candidatas en desarrollo clínico utilizan adyuvantes para mejorar la inmunogenicidad. [80] Un adyuvante inmunológico es una sustancia formulada con una vacuna para elevar la respuesta inmunitaria a un antígeno , como el virus COVID-19 o el virus de la influenza. [586] Específicamente, se puede utilizar un adyuvante en la formulación de una vacuna candidata a COVID-19 para aumentar su inmunogenicidad y eficacia para reducir o prevenir la infección por COVID-19 en personas vacunadas. [586] [587] Los adyuvantes usados en la formulación de la vacuna COVID-19 pueden ser particularmente efectivos para tecnologías que usan el virus COVID-19 inactivado y vacunas basadas en proteínas recombinantes o basadas en vectores.[587] Las sales de aluminio , conocidas como "alumbre", fueron el primer adyuvante utilizado para las vacunas autorizadas y son el adyuvante de elección en aproximadamente el 80% de las vacunas con adyuvante. [587] El adyuvante de alumbre inicia diversos mecanismos moleculares y celulares para mejorar la inmunogenicidad, incluida la liberación de citocinas proinflamatorias. [586] [587]
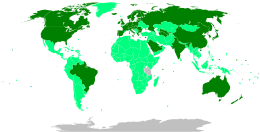
Despliegue
| Localización | Vacunado [b] | % de pop. [C] | |
|---|---|---|---|
| | 225,766,827 | 2,9% | |
| 71,054,445 | 21,3% | ||
| 64,980,000 | - | ||
| 35,560,656 | 8,0% | ||
| 27,079,484 | 2,0% | ||
| 24,453,221 | 36,0% | ||
| 8,919,356 | 4,2% | ||
| 7,911,946 | 9,4% | ||
| 6.578.881 | - | ||
| 6,507,159 | 7,8% | ||
| 5.545.133 | 3,8% | ||
| 5.200.395 | 60,1% | ||
| 5.135.616 | 7,6% | ||
| 4.954.541 | 25,9% | ||
| 4.798.638 | 7,9% | ||
| 4.398.094 | 2,7% | ||
| 4.225.311 | 11,5% | ||
| 4.166.862 | 1,5% | ||
| 3.951.221 | 8.5% | ||
| 3.794.719 | 2,9% | ||
| 2,924,629 | 7,7% | ||
| 2,550,387 | 6,8% | ||
| 2,336,749 | - | ||
| 1,952,883 | 4,3% | ||
| 1,446,358 | 7,5% | ||
| 1.347.073 | 13,9% | ||
| 1.249.044 | 18,4% | ||
| 1.207.904 | 7,1% | ||
| 877,644 | 8,4% | ||
| 827,508 | 8,1% | ||
| 811,322 | 7,6% | ||
| 778,715 | 8,7% | ||
| 776.061 | 6,7% | ||
| 773.011 | - | ||
| 758,884 | 7,5% | ||
| 749,059 | 1,5% | ||
| 675.000 | 6,2% | ||
| 666,550 | 7,7% | ||
| 602,150 | 1,2% | ||
| 597,471 | 10,8% | ||
| 586,153 | 10,1% | ||
| 549.000 | 9,4% | ||
| 453,586 | 4,5% | ||
| 447,635 | 8,3% | ||
| 451,589 | 9,2% | ||
| 417,395 | 7,7% | ||
| 402,264 | -- | ||
| 380,000 | -- | ||
| 379,274 | 1.2% | ||
| 349,970 | 20.6% | ||
| 322,000 | 7.5% | ||
| 301,699 | 0.9% | ||
| 300,000 | 1.0% | ||
| 282,398 | 0.2% | ||
| 281,713 | 4.1% | ||
| 260,616 | 9.6% | ||
| 257,000 | 2.0% | ||
| 253,800 | -- | ||
| 233,423 | 5.7% | ||
| 212,711 | -- | ||
| 212,220 | 6.1% | ||
| 206,000 | 2.8% | ||
| 190,088 | 3.7% | ||
| 174,402 | 8.4% | ||
| 170,659 | 1.0% | ||
| 164,781 | -- | ||
| 155,772 | 1.5% | ||
| 147,753 | 0.3% | ||
| 138,543 | 10.4% | ||
| 131,814 | 1.1% | ||
| 131,186 | 0.8% | ||
| 119,222 | 0.7% | ||
| 118,294 | -- | ||
| 114,500 | 0.1% | ||
| 103,142 | 0.2% | ||
| 85,984 | 1.7% | ||
| 82,671 | 18.7% | ||
| 82,432 | 4.4% | ||
| 81,802 | 1.2% | ||
| 75,000 | -- | ||
| 72,882 | 0.0% | ||
| 70,534 | 8.1% | ||
| 69,095 | 0.4% | ||
| 62,083 | 0.1% | ||
| 61,070 | 62.1% | ||
| 51,595 | 18.0% | ||
| 44,963 | -- | ||
| 43,479 | 7.0% | ||
| 38,073 | 37.7% | ||
| 37,660 | 0.3% | ||
| 34,217 | 0.2% | ||
| 34,171 | 10.0% | ||
| 29,631 | 88.0% | ||
| 27,637 | 4.3% | ||
| 25,000 | 0.4% | ||
| 24,164 | -- | ||
| 23,635 | -- | ||
| 21,864 | 33.3% | ||
| 21,500 | 32.1% | ||
| 21,405 | 25.2% | ||
| 20,944 | 0.2% | ||
| 18,000 | 0.4% | ||
| 17,395 | 27.9% | ||
| 15,865 | 0.0% | ||
| 15,181 | 0.1% | ||
| 12,754 | 0.3% | ||
| 12,194 | 0.0% | ||
| 11,000 | -- | ||
| 10,000 | 0.0% | ||
| 9,144 | 0.0% | ||
| 7,579 | 0.1% | ||
| 7,444 | 1.9% | ||
| 7,202 | 10.0% | ||
| 6,433 | 16.6% | ||
| 6,169 | 0.0% | ||
| 5,130 | 15.1% | ||
| 4,901 | 10.0% | ||
| 3,929 | 26.2% | ||
| 3,927 | 6.9% | ||
| 3,843 | 0.3% | ||
| 3,793 | 0.6% | ||
| 3,650 | 4.7% | ||
| 3,536 | -- | ||
| 3,000 | 2.7% | ||
| 2,684 | 0.0% | ||
| 2,400 | -- | ||
| 2,094 | 1.1% | ||
| 2,076 | 0.0% | ||
| 1,852 | 0.2% | ||
| 1,732 | 49.7% | ||
| 1,315 | -- | ||
| 1,215 | 0.0% | ||
| 652 | 13.0% | ||
| 440 | 0.0% | ||
| 107 | -- | ||
| 12,362 | 11.9% | ||
| 11,204 | 19.2% | ||
| 6,660 | 37.2% | ||
| 2 | 0.2% | ||
Sources List of sources by country. Notes
| |||
Al 14 de marzo de 2021, se habían administrado 359,54 millones de dosis de vacuna COVID-19 en todo el mundo según informes oficiales de agencias nacionales de salud recopilados por Our World in Data . [591]
Durante una pandemia en el cronograma rápido y la escala de las infecciones por COVID-19 durante 2020, organizaciones internacionales como la OMS y CEPI, los desarrolladores de vacunas, los gobiernos y la industria están evaluando la distribución de las vacunas eventuales. [592] Se puede persuadir a los países individuales que producen una vacuna para que favorezcan al mejor postor para la fabricación o proporcionen el primer servicio a su propio país. [593] [594] [595] [596] Los expertos enfatizan que las vacunas autorizadas deben estar disponibles y ser asequibles para las personas que se encuentran en la primera línea del cuidado de la salud y que tienen las mayores necesidades. [593] [594] [596]En abril, se informó que el Reino Unido acordó trabajar con otros 20 países y organizaciones globales, incluidos Francia, Alemania e Italia para encontrar una vacuna y compartir los resultados, y que los ciudadanos del Reino Unido no tendrían acceso preferencial a ninguna nueva vacuna COVID-19. desarrollado por universidades del Reino Unido financiadas por los contribuyentes. [597] Varias empresas planean fabricar inicialmente una vacuna a un precio artificialmente bajo , y luego aumentar los precios por rentabilidad si se necesitan vacunaciones anuales y a medida que los países acumulan existencias para necesidades futuras. [596]
Un informe de la CEPI de abril de 2020 declaró: "Se necesitará una sólida coordinación y cooperación internacional entre los desarrolladores de vacunas, los reguladores, los encargados de formular políticas, los financiadores, los organismos de salud pública y los gobiernos para garantizar que las vacunas candidatas en etapa avanzada prometedoras puedan fabricarse en cantidades suficientes y suministrarse equitativamente a todas las áreas afectadas, particularmente a las regiones de bajos recursos ". [598] La OMS y el CEPI están desarrollando recursos financieros y directrices para el despliegue mundial de varias vacunas COVID-19 seguras y eficaces, reconociendo que la necesidad es diferente entre países y segmentos de población. [592] [599] [600] [601] Por ejemplo, las vacunas COVID-19 exitosas probablemente se asignarían primero al personal de atención médicay las poblaciones con mayor riesgo de enfermedad grave y muerte a causa de la infección por COVID-19, como los ancianos o las personas empobrecidas densamente pobladas . [602] [603] La OMS, CEPI y GAVI han expresado su preocupación de que los países ricos no deberían tener acceso prioritario al suministro mundial de eventuales vacunas COVID-19, sino que es necesario proteger al personal sanitario y a las personas con alto riesgo de infección para abordar los problemas de salud pública y reducir el impacto económico de la pandemia. [598] [600] [602]Responsabilidad
Es posible que los ejemplos y la perspectiva de esta sección no representen una visión mundial del tema . ( Diciembre de 2020 ) ( Obtenga información sobre cómo y cuándo eliminar este mensaje de plantilla ) |
El 4 de febrero de 2020, el Secretario de Salud y Servicios Humanos de EE. UU., Alex Azar, publicó un aviso de declaración en virtud de la Ley de preparación pública y preparación para emergencias para contramedidas médicas contra COVID-19, que cubre "cualquier vacuna, utilizada para tratar, diagnosticar, curar, prevenir, o mitigar COVID-19, o la transmisión del SARS-CoV-2 o un virus que mute a partir del mismo ", y declarando que la declaración excluye" reclamaciones de responsabilidad que aleguen negligencia de un fabricante al crear una vacuna, o negligencia de un proveedor de atención médica al recetar la dosis incorrecta, en ausencia de mala conducta intencional ". [604] La declaración entra en vigor en los Estados Unidos hasta el 1 de octubre de 2024. [604]
En la Unión Europea, las vacunas COVID-19 están autorizadas bajo una Autorización de Comercialización Condicional que no exime a los fabricantes de reclamos de responsabilidad civil y administrativa. [605] Si bien los contratos de compra con los fabricantes de vacunas siguen siendo secretos, no contienen exenciones de responsabilidad ni siquiera por efectos secundarios desconocidos en el momento de la concesión de la licencia. [606]
sociedad y Cultura
Acceso
Las naciones se comprometieron a comprar dosis de la vacuna COVID-19 antes de que las dosis estuvieran disponibles. Aunque las naciones de altos ingresos representan solo el 14% de la población mundial, al 15 de noviembre de 2020, se habían contratado para comprar el 51% de todas las dosis pre-vendidas. Algunas naciones de altos ingresos compraron más dosis de las necesarias para vacunar a toda su población. [607]
El 18 de enero de 2021, el Director General de la OMS, Tedros Adhanom Ghebreyesus, advirtió sobre los problemas de la distribución equitativa: "Se han administrado más de 39 millones de dosis de vacuna en al menos 49 países de ingresos más altos. Solo se han administrado 25 dosis en uno de los país de ingresos. No 25 millones; no 25 mil; sólo 25 ". [608]
La vacuna COVID-19 de China Sinopharm fue autorizada para uso de emergencia por Bahrein y los Emiratos Árabes Unidos en diciembre de 2020. [609] [610]
Según los informes, algunas naciones involucradas en disputas territoriales de larga data han tenido su acceso a las vacunas bloqueado por naciones competidoras; Palestina ha acusado a Israel de bloquear la entrega de vacunas a Gaza , mientras que Taiwán ha sugerido que China ha obstaculizado sus esfuerzos para adquirir dosis de vacunas. [611] [612] [613]
Una sola dosis de la vacuna COVID-19 de AstraZeneca costaría 47 libras egipcias (EGP) y las autoridades la están vendiendo entre 100 y 200 EGP. Un informe de Carnegie Endowment for International Peace citó la tasa de pobreza actual en Egipto en alrededor del 29,7 por ciento, que constituye aproximadamente 30,5 millones de personas, y afirmó que alrededor de 15 millones de egipcios no podrían acceder al lujo de la vacunación. Khaled Ali, abogado de derechos humanos, inició una demanda contra el gobierno, obligándolo a proporcionar vacunas gratuitas a todos los miembros del público. [614]
Según el inmunólogo Anthony Fauci , las cepas mutantes del virus y la distribución limitada de vacunas plantean riesgos continuos y dijo: "Tenemos que vacunar a todo el mundo, no solo a nuestro propio país". [615] Edward Bergmark y Arick Wierson están pidiendo un esfuerzo de vacunación global y escribieron que la mentalidad de "yo primero" de las naciones más ricas podría finalmente ser contraproducente, porque la propagación del virus en los países más pobres conduciría a más variantes, contra las cuales la corriente las vacunas podrían ser menos efectivas. [616]
El 10 de marzo de 2021, Estados Unidos, Gran Bretaña, naciones de la Unión Europea y otros miembros de la OMC bloquearon un impulso de más de 80 países en desarrollo para renunciar a los derechos de patente de la vacuna COVID-19 en un esfuerzo por impulsar la producción de vacunas para las naciones pobres. [617]
Desinformación
Vacilación ante la vacuna
Alrededor del 10% del público percibe las vacunas como inseguras o innecesarias y rechaza la vacunación, una amenaza para la salud mundial denominada vacilación ante las vacunas [618] , que aumenta el riesgo de una mayor propagación viral que podría provocar brotes de COVID-19. [37] En mayo de 2020, las estimaciones de dos encuestas indicaron que el 67% o el 80% de las personas en los EE. UU. Aceptarían una nueva vacuna contra COVID-19, con una gran disparidad por nivel de educación, situación laboral, etnia y geografía. [619] En marzo de 2021, el 19% de los adultos estadounidenses afirman haber sido vacunados y el 50% de los adultos estadounidenses planean vacunarse. [620] [621]
En un esfuerzo por demostrar la seguridad de la vacuna, destacados políticos la han recibido en cámara, y otros se han comprometido a hacerlo. [622] [623] [624]
Ver también
- Vacuna contra la pandemia de gripe porcina de 2009
- Desarrollo de fármacos COVID-19
- Investigación de reutilización de fármacos COVID-19
Referencias
- ^ Li YD, Chi WY, Su JH, Ferrall L, Hung CF, Wu TC (diciembre de 2020). "Desarrollo de la vacuna contra el coronavirus: de SARS y MERS a COVID-19" . Revista de Ciencias Biomédicas . 27 (1): 104. doi : 10.1186 / s12929-020-00695-2 . PMC 7749790 . PMID 33341119 .
- ^ Padilla, Teodoro (24 de febrero de 2021). "Nadie está a salvo a menos que todos estén a salvo" . BusinessWorld . Consultado el 24 de febrero de 2021 .
- ^ a b c d e f "Canal de desarrollo de la vacuna COVID-19 (Actualizar URL para actualizar)" . Centro de Vacunas, Escuela de Higiene y Medicina Tropical de Londres. 1 de marzo de 2021 . Consultado el 10 de marzo de 2021 .
- ^ Beaumont, Peter (18 de noviembre de 2020). "Vacuna Covid-19: ¿a quiénes priorizan los países para las primeras dosis?" . The Guardian . ISSN 0261-3077 . Consultado el 26 de diciembre de 2020 .
- ^ "Vacunas contra el coronavirus (COVID-19) - Estadísticas e investigación" . Nuestro mundo en datos . Consultado el 7 de febrero de 2021 .
- ^ "¿Qué compañías probablemente producirán la mayor cantidad de vacuna COVID-19 en 2021?" . Mundo de procesamiento farmacéutico . 5 de febrero de 2021 . Consultado el 1 de marzo de 2021 .
- ^ "China puede alcanzar la capacidad anual de 500 millones de dosis de la vacuna CanSinoBIO COVID-19 este año" . Yahoo! Deporte . Consultado el 1 de marzo de 2021 .
- ^ Mullard A (30 de noviembre de 2020). "Cómo se distribuyen las vacunas COVID en todo el mundo Canadá lidera el grupo en términos de dosis aseguradas per cápita" . Naturaleza . doi : 10.1038 / d41586-020-03370-6 . PMID 33257891 . S2CID 227246811 .
- ^ So AD, Woo J (diciembre de 2020). "Reserva de vacunas de la enfermedad del coronavirus 2019 para el acceso global: análisis transversal" . BMJ . 371 : m4750. doi : 10.1136 / bmj.m4750 . ISSN 1756-1833 . PMC 7735431 . PMID 33323376 .
- ^ a b c Gates B (30 de abril de 2020). "Explicación de la carrera de la vacuna: lo que necesita saber sobre la vacuna COVID-19" . Las notas de Gates. Archivado desde el original el 14 de mayo de 2020 . Consultado el 2 de mayo de 2020 .
- ^ Cavanagh D (diciembre de 2003). "Desarrollo de la vacuna del síndrome respiratorio agudo severo: experiencias de vacunación contra el coronavirus de la bronquitis infecciosa aviar" . Patología aviar . 32 (6): 567–82. doi : 10.1080 / 03079450310001621198 . PMC 7154303 . PMID 14676007 .
- ^ Gao W, Tamin A, Soloff A, D'Aiuto L, Nwanegbo E, Robbins PD, et al. (Diciembre de 2003). "Efectos de una vacuna contra el coronavirus asociado al SARS en monos" . Lancet . 362 (9399): 1895–96. doi : 10.1016 / S0140-6736 (03) 14962-8 . PMC 7112457 . PMID 14667748 .
- ^ Kim E, Okada K, Kenniston T, Raj VS, AlHajri MM, Farag EA, et al. (Octubre de 2014). "Inmunogenicidad de una vacuna de coronavirus del síndrome respiratorio de Oriente Medio basada en adenovirus en ratones BALB / c" . La vacuna . 32 (45): 5975–82. doi : 10.1016 / j.vaccine.2014.08.058 . PMC 7115510 . PMID 25192975 .
- ^ Greenough TC, Babcock GJ, Roberts A, Hernandez HJ, Thomas WD, Coccia JA, et al. (Febrero de 2005). "Desarrollo y caracterización de un anticuerpo monoclonal humano neutralizador de coronavirus asociado al síndrome respiratorio agudo severo que proporciona inmunoprofilaxis eficaz en ratones" . La Revista de Enfermedades Infecciosas . 191 (4): 507-14. doi : 10.1086 / 427242 . PMC 7110081 . PMID 15655773 .
- ^ Tripp RA, Haynes LM, Moore D, Anderson B, Tamin A, Harcourt BH, et al. (Septiembre de 2005). "Anticuerpos monoclonales al coronavirus asociado al SARS (SARS-CoV): identificación de anticuerpos neutralizantes y reactivos a las proteínas virales S, N, M y E" . Revista de métodos virológicos . 128 (1-2): 21-28. doi : 10.1016 / j.jviromet.2005.03.021 . PMC 7112802 . PMID 15885812 .
- ^ Roberts A, Thomas WD, Guarner J, Lamirande EW, Babcock GJ, Greenough TC, et al. (Marzo de 2006). "La terapia con un anticuerpo monoclonal humano neutralizador de coronavirus asociado al síndrome respiratorio agudo severo reduce la gravedad de la enfermedad y la carga viral en hámsters sirios dorados" . La Revista de Enfermedades Infecciosas . 193 (5): 685–92. doi : 10.1086 / 500143 . PMC 7109703 . PMID 16453264 .
- ↑ a b Jiang S, Lu L, Du L (enero de 2013). "Todavía se necesita el desarrollo de vacunas y terapias contra el SARS" . Virología futura . 8 (1): 1–2. doi : 10.2217 / fvl.12.126 . PMC 7079997 . PMID 32201503 .
- ^ "SARS (síndrome respiratorio agudo severo)" . Servicio Nacional de Salud . 5 de marzo de 2020. Archivado desde el original el 9 de marzo de 2020 . Consultado el 31 de enero de 2020 .
- ^ Shehata MM, Gomaa MR, Ali MA, Kayali G (enero de 2016). "Coronavirus del síndrome respiratorio de Oriente Medio: una revisión completa" . Fronteras de la Medicina . 10 (2): 120–36. doi : 10.1007 / s11684-016-0430-6 . PMC 7089261 . PMID 26791756 .
- ^ Butler D (octubre de 2012). "Los veteranos del SARS abordan el coronavirus" . Naturaleza . 490 (7418): 20. Bibcode : 2012Natur.490 ... 20B . doi : 10.1038 / 490020a . PMID 23038444 .
- ^ Modjarrad K, Roberts CC, Mills KT, Castellano AR, Paolino K, Muthumani K, et al. (Septiembre de 2019). "Seguridad e inmunogenicidad de una vacuna de ADN de coronavirus del síndrome respiratorio de Oriente Medio: una fase 1, de etiqueta abierta, un solo brazo, prueba de escalada de dosis" . La lanceta. Enfermedades infecciosas . 19 (9): 1013–22. doi : 10.1016 / S1473-3099 (19) 30266-X . PMC 7185789 . PMID 31351922 .
- ^ Yong CY, Ong HK, Yeap SK, Ho KL, Tan WS (2019). "Avances recientes en el desarrollo de vacunas contra el síndrome respiratorio-coronavirus de Oriente Medio" . Fronteras en microbiología . 10 : 1781. doi : 10.3389 / fmicb.2019.01781 . PMC 6688523 . PMID 31428074 .
- ^ a b Le TT, Cramer JP, Chen R, Mayhew S (septiembre de 2020). "Evolución del panorama de desarrollo de la vacuna COVID-19" . Nature Reviews Descubrimiento de medicamentos . 19 (10): 667–68. doi : 10.1038 / d41573-020-00151-8 . ISSN 1474-1776 . PMID 32887942 . S2CID 221503034 .
- ^ a b c d e Thanh Le T, Andreadakis Z, Kumar A, Gómez Román R, Tollefsen S, Saville M, et al. (9 de abril de 2020). "El panorama del desarrollo de la vacuna COVID-19" . Nature Reviews Descubrimiento de medicamentos . 19 (5): 305–06. doi : 10.1038 / d41573-020-00073-5 . ISSN 1474-1776 . PMID 32273591 .
- ^ Simpson S, Kaufmann MC, Glozman V, Chakrabarti A (mayo de 2020). "Enfermedad X: acelerar el desarrollo de contramedidas médicas para la próxima pandemia" . La lanceta. Enfermedades infecciosas . 20 (5): e108-15. doi : 10.1016 / S1473-3099 (20) 30123-7 . ISSN 1474-4457 . PMC 7158580 . PMID 32197097 .
- ^ a b c d Sanger DE, Kirkpatrick DD, Zimmer C, Thomas K, Wee S (2 de mayo de 2020). "Con la presión creciente, se intensifica la carrera mundial por una vacuna" . The New York Times . ISSN 0362-4331 . Archivado desde el original el 11 de mayo de 2020 . Consultado el 2 de mayo de 2020 .
- ↑ a b c d Steenhuysen J, Eisler P, Martell A, Nebehay S (27 de abril de 2020). "Informe especial: países, empresas arriesgan miles de millones en la carrera por la vacuna contra el coronavirus" . Reuters. Archivado desde el original el 15 de mayo de 2020 . Consultado el 2 de mayo de 2020 .
- ^ Jeong-ho L, Zheng W, Zhou L (26 de enero de 2020). "Los científicos chinos corren para desarrollar una vacuna a medida que aumenta el número de muertes por coronavirus" . Poste matutino del sur de China . Archivado desde el original el 26 de enero de 2020 . Consultado el 28 de enero de 2020 .
- ^ Wee S (4 de mayo de 2020). "La campaña de vacunación contra el coronavirus de China potencia una industria en problemas" . The New York Times . ISSN 0362-4331 . Archivado desde el original el 4 de mayo de 2020 . Consultado el 4 de mayo de 2020 .
- ^ a b c Diamond MS, Pierson TC (13 de mayo de 2020). "Los desafíos del desarrollo de una vacuna contra un nuevo virus durante una pandemia" . Anfitrión celular y microbio . 27 (5): 699–703. doi : 10.1016 / j.chom.2020.04.021 . PMC 7219397 . PMID 32407708 .
- ^ Thorp HH (27 de marzo de 2020). "Subpromesa, sobreentrega" . Ciencia . 367 (6485): 1405. Bibcode : 2020Sci ... 367.1405T . doi : 10.1126 / science.abb8492 . PMID 32205459 .
- ^ Blackwell T (20 de abril de 2020). "Los investigadores de la vacuna COVID-19 dicen que el bloqueo pandémico coloca muchos obstáculos serios para su trabajo" . Correo Nacional . Archivado desde el original el 1 de noviembre de 2020 . Consultado el 3 de mayo de 2020 .
- ^ Chen J (4 de mayo de 2020). "Covid-19 ha cerrado laboratorios. Podría poner en riesgo a una generación de investigadores" . Stat . Archivado desde el original el 6 de mayo de 2020 . Consultado el 4 de mayo de 2020 .
- ^ a b c "Seguridad de las vacunas: vacunas" . vacunas.gov . Departamento de Salud y Servicios Humanos de EE. UU. Archivado desde el original el 22 de abril de 2020 . Consultado el 13 de abril de 2020 .
- ^ a b c d "El proceso de desarrollo de fármacos" . EE.UU. Administración de Drogas y Alimentos (FDA). 4 de enero de 2018. Archivado desde el original el 22 de febrero de 2020 . Consultado el 12 de abril de 2020 .
- ^ a b Cohen J (19 de junio de 2020). "Las vacunas antipandémicas están a punto de afrontar la prueba real" . Ciencia . 368 (6497): 1295–96. Código Bibliográfico : 2020Sci ... 368.1295C . doi : 10.1126 / science.368.6497.1295 . PMID 32554572 .
- ↑ a b Dubé E, Laberge C, Guay M, Bramadat P, Roy R, Bettinger J (1 de agosto de 2013). "Vacunación de vacunas: una visión general" . Vacunas e inmunoterapias humanas . 9 (8): 1763–73. doi : 10.4161 / hv.24657 . ISSN 2164-554X . PMC 3906279 . PMID 23584253 .
- ^ Howard J, Stracqualursi V (18 de junio de 2020). "Fauci advierte que el 'sesgo anticientífico' es un problema en Estados Unidos" . CNN. Archivado desde el original el 21 de junio de 2020 . Consultado el 21 de junio de 2020 .
- ^ "Vacunas: el procedimiento de autorización de emergencia" . Agencia Europea de Medicamentos. 2020. Archivado desde el original el 24 de septiembre de 2020 . Consultado el 21 de agosto de 2020 .
- ^ Byrne, Jane (19 de octubre de 2020). "Vacuna Moderna COVID-19 en proceso de revisión continua en Canadá, UE" . BioPharma-Reporter.com, William Reed Business Media Ltd . Consultado el 25 de noviembre de 2020 .
- ^ Dangerfield, Katie (20 de noviembre de 2020). "Pfizer solicita el uso de emergencia de la vacuna contra el coronavirus en EE. UU. ¿Y en Canadá?" . Noticias globales . Consultado el 25 de noviembre de 2020 .
- ^ "G20 lanza iniciativa de herramientas de salud necesarias para combatir el coronavirus" . El globo y el correo . 25 de abril de 2020.
- ^ "Acceso al acelerador de herramientas COVID-19 (ACT)" (PDF) . Organización Mundial de la Salud (OMS). 24 de abril de 2020.
- ^ "El ACT-Accelerator: preguntas más frecuentes (FAQ)" . Organización Mundial de la Salud (OMS). 2020 . Consultado el 16 de diciembre de 2020 .
- ^ "Actualización sobre el ensayo de solidaridad de la OMS - Acelerando una vacuna COVID-19 segura y eficaz" . Organización Mundial de la Salud (OMS). 27 de abril de 2020. Archivado desde el original el 30 de abril de 2020 . Consultado el 2 de mayo de 2020 .
Es vital que evaluemos tantas vacunas como sea posible, ya que no podemos predecir cuántas resultarán viables. Para aumentar las posibilidades de éxito (dado el alto nivel de desgaste durante el desarrollo de la vacuna), debemos probar todas las vacunas candidatas hasta que fallen. [La] OMS está trabajando para asegurar que todos ellos tengan la oportunidad de ser evaluados en la etapa inicial de desarrollo. Los resultados de la eficacia de cada vacuna se esperan dentro de tres a seis meses y esta evidencia, combinada con datos sobre seguridad, informará las decisiones sobre si se puede utilizar en una escala más amplia.
- ^ Abedi M (23 de marzo de 2020). "Canadá gastará 192 millones de dólares en el desarrollo de la vacuna COVID-19" . Noticias globales . Archivado desde el original el 9 de abril de 2020 . Consultado el 24 de marzo de 2020 .
- ^ "Respuesta de investigación del gobierno de Canadá a COVID-19" . Gobierno de Canadá. 23 de abril de 2020. Archivado desde el original el 13 de mayo de 2020 . Consultado el 4 de mayo de 2020 .
- ^ Takada N, Satake M (2 de mayo de 2020). "EE.UU. y China desatan carteras en carrera por la vacuna contra el coronavirus" . Revista asiática Nikkei . Archivado desde el original el 10 de mayo de 2020 . Consultado el 3 de mayo de 2020 .
- ^ Morriss E (22 de abril de 2020). "El gobierno lanza un grupo de trabajo sobre la vacuna contra el coronavirus cuando comienzan los ensayos clínicos en humanos" . Pharmafield. Archivado desde el original el 17 de junio de 2020 . Consultado el 3 de mayo de 2020 .
- ^ Kuznia R, Polglase K, Mezzofiore G (1 de mayo de 2020). "En busca de una vacuna, Estados Unidos hace una 'gran apuesta' en una empresa con tecnología no probada" . CNN. Archivado desde el original el 13 de mayo de 2020 . Consultado el 2 de mayo de 2020 .
- ^ Cohen J (15 de mayo de 2020). "El esfuerzo de la vacuna 'Warp Speed' de Estados Unidos sale de las sombras" . Ciencia . 368 (6492): 692–93. Código Bibliográfico : 2020Sci ... 368..692C . doi : 10.1126 / science.368.6492.692 . ISSN 0036-8075 . PMID 32409451 .
- ^ Justin Sink, Jordan Fabian, Riley Griffin (15 de mayo de 2020). "Trump presenta líderes de 'Warp Speed' para acelerar la vacuna COVID-19" . Bloomberg. Archivado desde el original el 21 de mayo de 2020 . Consultado el 15 de mayo de 2020 .CS1 maint: uses authors parameter (link)
- ^ "Cronología de la Organización Mundial de la Salud - COVID-19" . Organización Mundial de la Salud. 27 de abril de 2020. Archivado desde el original el 29 de abril de 2020 . Consultado el 2 de mayo de 2020 .
- ^ a b c Thanh Le T, Andreadakis Z, Kumar A, Gómez Román R, Tollefsen S, Saville M, et al. (9 de abril de 2020). "El panorama del desarrollo de la vacuna COVID-19" . Nature Reviews Descubrimiento de medicamentos . 19 (5): 305–06. doi : 10.1038 / d41573-020-00073-5 . ISSN 1474-1776 . PMID 32273591 .
- ^ a b Gates B (febrero de 2020). "Respondiendo a Covid-19: ¿Una pandemia única en un siglo?" . La Revista de Medicina de Nueva Inglaterra . 382 (18): 1677–79. doi : 10.1056 / nejmp2003762 . PMID 32109012 .
- ^ Fauci AS, Lane HC, Redfield RR (marzo de 2020). "Covid-19: Navegando por lo inexplorado" . La Revista de Medicina de Nueva Inglaterra . 382 (13): 1268–69. doi : 10.1056 / nejme2002387 . PMC 7121221 . PMID 32109011 .
- ^ a b Le TT, Cramer JP, Chen R, Mayhew S (4 de septiembre de 2020). "Evolución del panorama de desarrollo de la vacuna COVID-19" . Nature Reviews Descubrimiento de medicamentos . 19 (10): 667–68. doi : 10.1038 / d41573-020-00151-8 . ISSN 1474-1776 . PMID 32887942 . S2CID 221503034 .
- ^ Weintraub R, Yadav P, Berkley S (2 de abril de 2020). "Una vacuna COVID-19 necesitará una distribución global equitativa" . Harvard Business Review . ISSN 0017-8012 . Archivado desde el original el 9 de junio de 2020 . Consultado el 9 de junio de 2020 .
- ^ "La pandemia de COVID-19 revela los riesgos de depender del sector privado para las vacunas que salvan vidas, dice el experto" . Radio CBC . 8 de mayo de 2020. Archivado desde el original el 13 de mayo de 2020 . Consultado el 8 de junio de 2020 .
- ^ Ahmed DD (4 de junio de 2020). "El acuerdo de Oxford, AstraZeneca COVID-19 refuerza la 'soberanía de las vacunas ' " . Stat . Archivado desde el original el 12 de junio de 2020 . Consultado el 8 de junio de 2020 .
- ^ Grenfell R, Drew T (14 de febrero de 2020). "He aquí por qué la OMS dice que faltan 18 meses para una vacuna contra el coronavirus" . Business Insider . Consultado el 11 de noviembre de 2020 .
- ^ "Actualización sobre el ensayo de solidaridad de la OMS - Acelerando una vacuna COVID-19 segura y eficaz" . Organización Mundial de la Salud. 27 de abril de 2020. Archivado desde el original el 30 de abril de 2020 . Consultado el 2 de mayo de 2020 .
Es vital que evaluemos tantas vacunas como sea posible, ya que no podemos predecir cuántas resultarán viables. Para aumentar las posibilidades de éxito (dado el alto nivel de desgaste durante el desarrollo de la vacuna), debemos probar todas las vacunas candidatas hasta que fallen. [La] OMS está trabajando para asegurar que todos ellos tengan la oportunidad de ser evaluados en la etapa inicial de desarrollo. Los resultados de la eficacia de cada vacuna se esperan dentro de tres a seis meses y esta evidencia, combinada con datos sobre seguridad, informará las decisiones sobre si se puede utilizar en una escala más amplia.
- ^ Yamey G, Schäferhoff M, Hatchett R, Pate M, Zhao F, McDade KK (mayo de 2020). "Garantizar el acceso mundial a las vacunas COVID-19" . Lancet . 395 (10234): 1405–06. doi : 10.1016 / S0140-6736 (20) 30763-7 . PMC 7271264 . PMID 32243778 .
CEPI estima que el desarrollo de hasta tres vacunas en los próximos 12 a 18 meses requerirá una inversión de al menos
2.000
millones
de
dólares estadounidenses. Esta estimación incluye
ensayos clínicos de
fase
1 de ocho candidatos a vacunas, progresión de hasta seis candidatos a través de la fase
2 y
3 ensayos, cumplimiento de los requisitos reglamentarios y de calidad para al menos tres vacunas y mejora de la capacidad de fabricación mundial de tres vacunas.
- ^ "La OMS 'apoyó el uso de emergencia de China' de las vacunas experimentales Covid-19" . Poste matutino del sur de China . 25 de septiembre de 2020. Archivado desde el original el 26 de septiembre de 2020 . Consultado el 26 de septiembre de 2020 .
- ^ Kramer AE (19 de septiembre de 2020). "Rusia es lenta para administrar la vacuna contra el virus a pesar de la aprobación del Kremlin" . The New York Times . ISSN 0362-4331 . Archivado desde el original el 27 de septiembre de 2020 . Consultado el 28 de septiembre de 2020 .
- ^ "Pfizer y BioNTech para presentar hoy una solicitud de autorización de uso de emergencia a la FDA de los Estados Unidos para la vacuna COVID-19" . Pfizer (Comunicado de prensa). 20 de noviembre de 2020 . Consultado el 20 de noviembre de 2020 .
- ^ Parque A (20 de noviembre de 2020). "Exclusivo: el director ejecutivo de Pfizer analiza la presentación de la primera solicitud de autorización de la vacuna COVID-19 a la FDA" . Tiempo . Consultado el 20 de noviembre de 2020 .
- ^ "Información para profesionales de la salud sobre la vacuna Pfizer / BioNTech COVID-19" . Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) . 8 de diciembre de 2020 . Consultado el 13 de diciembre de 2020 .
- ^ "Condiciones de autorización para la vacuna Pfizer / BioNTech COVID-19" . Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) . 3 de diciembre de 2020 . Consultado el 19 de diciembre de 2020 .
- ^ "El regulador de medicamentos del Reino Unido da la aprobación para la primera vacuna COVID-19 del Reino Unido" . Agencia Reguladora de Medicamentos y Productos Sanitarios, Gobierno del Reino Unido. 2 de diciembre de 2020 . Consultado el 2 de diciembre de 2020 .
- ^ Mueller, Benjamin (2 de diciembre de 2020). "Reino Unido aprueba la vacuna contra el coronavirus de Pfizer, la primera en Occidente" . The New York Times . Consultado el 2 de diciembre de 2020 .
- ^ Roberts, Michelle (2 de diciembre de 2020). "Vacuna Covid Pfizer aprobada para su uso la próxima semana en el Reino Unido" . BBC . Consultado el 2 de diciembre de 2020 .
- ^ "Preguntas y respuestas: vacunación COVID-19 en la UE" . Comisión Europea . 21 de diciembre de 2020 . Consultado el 21 de diciembre de 2020 .
- ^ "Bahrein segundo en el mundo en aprobar la vacuna Pfizer / BioNTech Covid-19" . Agencia de Noticias de Bahrein. 4 de diciembre de 2020 . Consultado el 9 de diciembre de 2020 .
- ^ "Emiratos Árabes Unidos: Ministerio de salud anuncia 86 por ciento de eficacia de la vacuna" . Gulf News . Consultado el 9 de diciembre de 2020 .
- ^ Thomas K, LaFraniere S, Weiland N, Goodnough A, Haberman M (12 de diciembre de 2020). "La FDA aprueba la vacuna Pfizer y millones de dosis se enviarán de inmediato" . The New York Times . Consultado el 12 de diciembre de 2020 .
- ^ "La FDA toma medidas adicionales en la lucha contra COVID-19 al emitir una autorización de uso de emergencia para la segunda vacuna COVID-19" . EE.UU. Administración de Drogas y Alimentos (FDA) (Nota de prensa) . Consultado el 18 de diciembre de 2020 .
- ^ Oliver SE, Gargano JW, Marin M, Wallace M, Curran KG, Chamberland M, et al. (Diciembre de 2020). "Recomendación provisional del Comité Asesor sobre Prácticas de Inmunización para el uso de la vacuna COVID-19 Moderna - Estados Unidos, diciembre de 2020" (PDF) . MMWR. Informe Semanal de Morbilidad y Mortalidad . 69 (5152): 1653–1656. doi : 10.15585 / mmwr.mm695152e1 . PMID 33382675 . S2CID 229945697 .
- ^ Lovelace Jr B (19 de diciembre de 2020). "La FDA aprueba la segunda vacuna Covid para uso de emergencia, ya que autoriza la distribución de Moderna en los Estados Unidos" . CNBC . Consultado el 19 de diciembre de 2020 .
- ^ a b c d e f Thanh Le T, Cramer JP, Chen R, Mayhew S (4 de septiembre de 2020). "Evolución del panorama de desarrollo de la vacuna COVID-19" . Nature Reviews Descubrimiento de medicamentos . 19 (10): 667–68. doi : 10.1038 / d41573-020-00151-8 . ISSN 1474-1776 . PMID 32887942 . S2CID 221503034 .
- ^ Krammer F (octubre de 2020). "Vacunas contra el SARS-CoV-2 en desarrollo" . Naturaleza . 586 (7830): 516–27. Código Bib : 2020Natur.586..516K . doi : 10.1038 / s41586-020-2798-3 . PMID 32967006 . S2CID 221887746 .
- ^ Park KS, Sun X, Aikins ME, Moon JJ (diciembre de 2020). "Sistemas de entrega de vacunas COVID-19 no virales" . Revisiones avanzadas de entrega de medicamentos . 169 : 137–51. doi : 10.1016 / j.addr.2020.12.008 . PMC 7744276 . PMID 33340620 .
- ^ Kowalski PS, Rudra A, Miao L, Anderson DG (abril de 2019). "Entrega del mensajero: avances en tecnologías para la entrega de ARNm terapéutico" . Mol Ther . 27 (4): 710-28. doi : 10.1016 / j.ymthe.2019.02.012 . PMC 6453548 . PMID 30846391 .
- ^ Verbeke R, Lentacker I, De Smedt SC, Dewitte H (octubre de 2019). "Tres décadas de desarrollo de la vacuna de ARN mensajero" . Nano hoy . 28 : 100766. doi : 10.1016 / j.nantod.2019.100766 .
- ^ "Recomendaciones de la vacuna COVID-19 ACIP" . Centros para el Control y la Prevención de Enfermedades (CDC) . Consultado el 18 de febrero de 2021 .
- ^ "Vacunas seguras COVID-19 para europeos" . Comisión Europea - Comisión Europea . Consultado el 19 de febrero de 2021 .
- ^ a b c d "Resumen de la decisión reglamentaria: vacuna Pfizer-BioNTech COVID-19" . Health Canada, Gobierno de Canadá. 9 de diciembre de 2020 . Consultado el 9 de diciembre de 2020 .
- ^ a b "Estudio para describir la seguridad, tolerabilidad, inmunogenicidad y eficacia de los candidatos a la vacuna de ARN contra COVID-19 en adultos sanos" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 30 de abril de 2020. NCT04368728. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ a b "Un ensayo de escalada de dosis de dos partes de fase I / II en varios sitios que investiga la seguridad e inmunogenicidad de cuatro vacunas profilácticas de ARN del SARS-CoV-2 contra COVID-19 utilizando diferentes regímenes de dosificación en adultos sanos" . Registro de ensayos clínicos de la UE . Unión Europea. 14 de abril de 2020. EudraCT 2020-001038-36. Archivado desde el original el 22 de abril de 2020 . Consultado el 22 de abril de 2020 .
- ^ a b "Un estudio para evaluar la eficacia, seguridad e inmunogenicidad de la vacuna mRNA-1273 en adultos mayores de 18 años para prevenir COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 14 de julio de 2020. NCT04470427. Archivado desde el original el 11 de octubre de 2020 . Consultado el 27 de julio de 2020 .
- ^ a b Palca J (27 de julio de 2020). "El candidato a vacuna COVID-19 se dirige a pruebas generalizadas en EE . UU." NPR. Archivado desde el original el 11 de octubre de 2020 . Consultado el 27 de julio de 2020 .
- ^ a b "EMA comienza a renovar la revisión de la vacuna COVID-19 de CureVac (CVnCoV)" . Agencia Europea de Medicamentos (EMA) (Comunicado de prensa). 1 de diciembre de 2020 . Consultado el 12 de febrero de 2021 .
- ^ a b "¿Qué son las vacunas basadas en vectores virales y cómo podrían usarse contra COVID-19?" . GAVI. 2020 . Consultado el 26 de enero de 2021 .
- ^ a b c "Investigación de una vacuna contra COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 26 de mayo de 2020. NCT04400838. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ a b "Un estudio de fase 2/3 para determinar la eficacia, seguridad e inmunogenicidad de la vacuna candidata contra la enfermedad por coronavirus (COVID-19) ChAdOx1 nCoV-19" . Registro de ensayos clínicos de la UE . Unión Europea. 21 de abril de 2020. EudraCT 2020-001228-32. Archivado desde el original el 5 de octubre de 2020 . Consultado el 3 de agosto de 2020 .
- ^ a b O'Reilly P (26 de mayo de 2020). "Un estudio de fase III para investigar una vacuna contra COVID-19" . ISRCTN . doi : 10.1186 / ISRCTN89951424 . ISRCTN89951424.
- ^ Córum, Jonathan; Zimmer, Carl (8 de enero de 2021). "Cómo funciona la vacuna de Gamaleya" . The New York Times . Consultado el 27 de enero de 2021 .
- ^ a b "Un estudio de Ad26.COV2.S en adultos" . ClinicalTrials.gov . 4 de agosto de 2020. Archivado desde el original el 16 de septiembre de 2020 . Consultado el 23 de agosto de 2020 .
- ^ a b "Un estudio de Ad26.COV2.S para la prevención de COVID-19 mediado por SARS-CoV-2 en participantes adultos" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de EE. UU. Archivado desde el original el 26 de septiembre de 2020.
- ^ Johnson, Carolyn; McGinley, Laura. "Johnson & Johnson busca la autorización de emergencia de la FDA para la vacuna contra el coronavirus de inyección única" . The Washington Post .
- ^ "No es solo Johnson & Johnson: China tiene una vacuna COVID-19 de dosis única que es 65% efectiva" . Fortuna . Consultado el 28 de febrero de 2021 .
- ^ Petrovsky N, Aguilar JC (28 de septiembre de 2004). "Coadyuvantes de vacunas: estado actual y tendencias futuras". Inmunología y Biología Celular . 82 (5): 488–96. doi : 10.1111 / j.0818-9641.2004.01272.x . ISSN 0818-9641 . PMID 15479434 . S2CID 154670 .
- ^ a b c "Estudio de seguridad e inmunogenicidad de la vacuna inactivada para la prevención de la infección por SARS-CoV-2 (COVID-19) (Renqiu)" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 12 de mayo de 2020. NCT04383574. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ a b "Ensayo clínico de eficacia y seguridad de la vacuna COVID-19 (inactivada) adsorbida de Sinovac en profesionales de la salud (PROFISCOV)" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 2 de julio de 2020. NCT04456595. Archivado desde el original el 11 de octubre de 2020 . Consultado el 3 de agosto de 2020 .
- ^ a b PT. Bio Farma (10 de agosto de 2020). "Un estudio de fase III, ciego al observador, aleatorizado, controlado con placebo de la eficacia, seguridad e inmunogenicidad de la vacuna inactivada del SARS-COV-2 en adultos sanos de 18 a 59 años en Indonesia" . Registri Penyakit Indonesia . Consultado el 15 de agosto de 2020 .
- ^ a b c Chen W, Al Kaabi N (18 de julio de 2020). "Un ensayo clínico de fase III para la vacuna inactivada de la neumonía por coronavirus nuevo (COVID-19) (células Vero)" . Registro chino de ensayos clínicos . Consultado el 15 de agosto de 2020 .
- ^ https://www.reuters.com/article/us-health-coronavirus-russia-vaccine-idUSKBN2AK07H
- ^ a b "Vacuna VLA2001 COVID-19" . Vacunas de precisión . 31 de diciembre de 2020 . Consultado el 11 de enero de 2021 .
- ^ a b "Estudio de determinación de dosis para evaluar la seguridad, la tolerabilidad y la inmunogenicidad de un candidato de vacuna contra el virus Sars-Cov-2 adyuvante inactivado contra Covid-19 en adultos sanos" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de EE. UU. 30 de diciembre de 2020 . Consultado el 11 de enero de 2021 .
- ^ "Módulo 2 - Vacunas de subunidad" . Conceptos básicos de seguridad de las vacunas de la OMS .
- ^ a b c d "Estudio de la seguridad, reactogenicidad e inmunogenicidad de la vacuna" EpiVacCorona "para la prevención de COVID-19 (EpiVacCorona)" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 22 de septiembre de 2020. NCT04368988 . Consultado el 16 de noviembre de 2020 .
- ^ a b "Evaluación de la seguridad e inmunogenicidad de una vacuna de nanopartículas de SARS-CoV-2 rS (COVID-19) con / sin adyuvante Matrix-M" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 30 de abril de 2020. NCT04368988. Archivado desde el original el 14 de julio de 2020 . Consultado el 14 de julio de 2020 .
- ^ a b "Un estudio sobre la seguridad, tolerabilidad y respuesta inmune de la vacuna Sclamp (COVID-19) SARS-CoV-2 en adultos sanos" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 3 de agosto de 2020. NCT04495933. Archivado desde el original el 11 de octubre de 2020 . Consultado el 4 de agosto de 2020 .
- ^ a b "Vacuna UQ-CSL V451" . precisionvaccinations.com . Consultado el 11 de diciembre de 2020 .
- ^ a b "Un estudio clínico prospectivo, aleatorizado, adaptativo, de fase I / II para evaluar la seguridad y la inmunogenicidad de la vacuna candidata a vacuna del nuevo virus corona-2019-nCov de M / s Cadila Healthcare Limited por vía intradérmica en sujetos sanos" . ctri.nic.in . Registro de ensayos clínicos de la India . 15 de diciembre de 2020. CTRI / 2020/07/026352. Archivado desde el original el 22 de noviembre de 2020.
- ^ a b "Seguridad, tolerabilidad e inmunogenicidad de INO-4800 para COVID-19 en voluntarios sanos" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 7 de abril de 2020. NCT04336410. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ a b "IVI, INOVIO y KNIH para asociarse con CEPI en un ensayo clínico de fase I / II de la vacuna de ADN COVID-19 de INOVIO en Corea del Sur" . Instituto Internacional de Vacunas. 16 de abril de 2020 . Consultado el 23 de abril de 2020 .
- ^ a b "Estudio de la vacuna de ADN COVID-19 (AG0301-COVID19)" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 9 de julio de 2020. NCT04463472. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ a b "Estudio de seguridad e inmunogenicidad de GX-19, una vacuna de ADN preventiva COVID-19 en adultos sanos" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 24 de junio de 2020. NCT04445389. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ a b "Genexine de Corea del Sur comienza el ensayo en humanos de la vacuna contra el coronavirus" . Reuters. 19 de junio de 2020. Archivado desde el original el 11 de octubre de 2020 . Consultado el 25 de junio de 2020 .
- ^ a b "Seguridad e inmunidad de la vacuna Covid-19 aAPC" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 9 de marzo de 2020. NCT04299724. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ a b "Inmunidad y seguridad de la vacuna minigen sintética Covid-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 19 de febrero de 2020. NCT04276896. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ a b c "Estudio Fase I / II aleatorizado, multicéntrico, controlado con placebo, de escalado de dosis para evaluar la seguridad, inmunogenicidad y eficacia potencial de una vacuna rVSV-SARS-CoV-2-S (IIBR-100) en adultos " . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 1 de noviembre de 2020. NCT04608305.
- ^ Johnson, Carolyn Y .; Mufson, Steven. "¿Pueden las viejas vacunas del botiquín de la ciencia prevenir el coronavirus?" . The Washington Post . ISSN 0190-8286 . Consultado el 31 de diciembre de 2020 .
- ^ "Vacunación de Bacille Calmette-Guérin (BCG) y COVID-19" . Organización Mundial de la Salud (OMS). 12 de abril de 2020. Archivado desde el original el 30 de abril de 2020 . Consultado el 1 de mayo de 2020 .
- ^ "Cómo se miden la efectividad y la eficacia de la vacuna contra la gripe" . Centros para el Control y la Prevención de Enfermedades, Centro Nacional de Inmunización y Enfermedades Respiratorias, Departamento de Salud y Servicios Humanos de EE. UU. 29 de enero de 2016. Archivado desde el original el 7 de mayo de 2020 . Consultado el 6 de mayo de 2020 .
- ^ "Principios de epidemiología, sección 8: conceptos de aparición de enfermedades" . Centros para el Control y la Prevención de Enfermedades, Centro de Vigilancia, Epidemiología y Servicios de Laboratorio, Departamento de Salud y Servicios Humanos de EE. UU. 18 de mayo de 2012. Archivado desde el original el 6 de abril de 2020 . Consultado el 6 de mayo de 2020 .
- ^ a b Pallmann P, Bedding AW, Choodari-Oskooei B, Dimairo M, Flight L, Hampson LV, et al. (Febrero de 2018). "Diseños adaptativos en ensayos clínicos: por qué usarlos y cómo ejecutarlos y reportarlos" . Medicina BMC . 16 (1): 29. doi : 10.1186 / s12916-018-1017-7 . PMC 5830330 . PMID 29490655 .
- ^ "Diseños adaptativos para ensayos clínicos de fármacos y productos biológicos: orientación para la industria" (PDF) . EE.UU. Administración de Drogas y Alimentos (FDA). 1 de noviembre de 2019. Archivado desde el original el 13 de diciembre de 2019 . Consultado el 3 de abril de 2020 .
- ^ "Un ensayo aleatorizado internacional de vacunas candidatas contra COVID-19: Esquema del ensayo de vacuna de solidaridad" (PDF) . Organización Mundial de la Salud (OMS). 9 de abril de 2020. Archivado (PDF) desde el original el 12 de mayo de 2020 . Consultado el 9 de mayo de 2020 .
- ^ Farge, Emma; Revill, John (5 de enero de 2021). "La OMS recomienda dos dosis de la vacuna Pfizer COVID-19 en un plazo de 21 a 28 días" . Reuters . Ginebra . Consultado el 5 de marzo de 2021 .
- ^ Keaten, Jamey (8 de enero de 2021). "QUIÉN: En medio de la escasez de suministros, las dosis de vacuna pueden tener un intervalo de 6 semanas" . Prensa asociada . Ginebra . Consultado el 6 de marzo de 2021 .
- ^ "Vacuna COVID: las inyecciones modernas pueden tener 6 semanas de diferencia, dice la OMS" . Deutsche Welle . 26 de enero de 2021 . Consultado el 6 de marzo de 2021 .
- ^ "Actualización del coronavirus (COVID-19): la FDA permite un almacenamiento y condiciones de transporte más flexibles para la vacuna Pfizer-BioNTech COVID-19" (Comunicado de prensa). Administración de Alimentos y Medicamentos (FDA). 25 de febrero de 2021 . Consultado el 5 de marzo de 2021 .
- ^ a b "Hoja de datos de EUA de la vacuna Pfizer-BioNTech COVID-19 para proveedores de atención médica" (PDF) . Pfizer. 25 de febrero de 2021 . Consultado el 25 de febrero de 2021 .
- ^ "Pfizer y BioNTech concluyen el estudio de fase 3 del candidato a vacuna COVID-19, que cumple con todos los criterios de valoración de eficacia primarios" (Comunicado de prensa). Pfizer. 18 de noviembre de 2020.
- ^ Polack F, Thomas S, Kitchin N, Absalon J, Gurtman A, Lockhart S, et al. (Diciembre de 2020). "Seguridad y eficacia de la vacuna BNT162b2 mRNA Covid-19" . Revista de Medicina de Nueva Inglaterra . 383 (27): 2603-15. doi : 10.1056 / NEJMoa2034577 . PMC 7745181 . PMID 33301246 .
- ^ Revisión de la FDA sobre la eficacia y seguridad de la solicitud de autorización de uso de emergencia de la vacuna Pfizer-BioNTech COVID-19 (PDF) . EE.UU. Administración de Drogas y Alimentos (FDA) (Informe). 10 de diciembre de 2020 . Consultado el 11 de diciembre de 2020 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ Erman M (18 de noviembre de 2020). "Pfizer finaliza el ensayo de COVID-19 con una eficacia del 95%, para solicitar la autorización de uso de emergencia" . Reuters . Consultado el 18 de noviembre de 2020 .
- ↑ a b c Zimmer, Carl (20 de noviembre de 2020). "2 empresas dicen que sus vacunas tienen un 95% de efectividad. ¿Qué significa eso? Se podría suponer que 95 de cada 100 personas vacunadas estarán protegidas contra Covid-19. Pero no es así como funcionan las matemáticas" . The New York Times . Consultado el 21 de noviembre de 2020 .
- ^ "Albania para iniciar la inmunización COVID-19 con la vacuna Pfizer en enero - informe" . Seenews .
- ^ "ANDORRA COVID-19" . gobernar.ad . Consultado el 19 de febrero de 2021 .
- ^ "Coronavirus en la Argentina: La ANMAT aprobo el uso de emergencia de la vacuna Pfizer" . La Nación (en español) . Consultado el 23 de diciembre de 2020 .
- ^ Overheid, Aruba (7 de enero de 2021). "Actualización de la vacuna COVID-19" . gobierno.aw . Consultado el 19 de febrero de 2021 .
- ^ "Bahrein se convierte en el segundo país en aprobar la vacuna Pfizer COVID-19" . Al Jazeera . Consultado el 5 de diciembre de 2020 .
- ^ a b c "Autorizaciones de medicamentos y vacunas para COVID-19: Lista de solicitudes recibidas" . Health Canada, Gobierno de Canadá. 9 de diciembre de 2020 . Consultado el 9 de diciembre de 2020 .
- ^ "Vacuna Pfizer aprobada para la región, pero el Ministerio de Salud quiere más información" . Noticias de Trinidad y Tobago . 6 de enero de 2021 . Consultado el 24 de febrero de 2021 .
- ^ "Chile aprueba la vacuna Pfizer-BioNTech Covid-19 para uso de emergencia" . Los tiempos del estrecho . 17 de diciembre de 2020 . Consultado el 17 de diciembre de 2020 .
- ^ "Regulador de Colombia aprueba la vacuna Pfizer-BioNTech para uso de emergencia" . Reuters . 6 de enero de 2021 . Consultado el 6 de enero de 2021 .
- ^ "Costa Rica autoriza la vacuna contra el coronavirus de Pfizer-BioNTech" . The Tico Times . 16 de diciembre de 2020 . Consultado el 16 de diciembre de 2020 .
- ^ "ARCSA autoriza ingreso al país de vacuna Pfizer-BionTech para el Covid-19 - Agencia Nacional de Regulación, Control y Vigilancia Sanitaria" (en español) . Consultado el 17 de diciembre de 2020 .
- ^ "Aprobado el uso de la vacuna" . Gobierno de Hong Kong. 25 de enero de 2021 . Consultado el 15 de febrero de 2021 .
- ^ "Irak otorga aprobación de emergencia para la vacuna Pfizer COVID-19" . MSN . Consultado el 27 de diciembre de 2020 .
- ^ "Ministro de salud israelí 'complacido' como la FDA aprueba la vacuna Pfizer COVID-19" . The Jerusalem Post . Consultado el 28 de diciembre de 2020 .
- ^ "Jordan aprueba la vacuna Pfizer-BioNTech Covid" . Francia 24.15 de diciembre de 2020 . Consultado el 15 de diciembre de 2020 .
- ^ "Kuwait autoriza el uso de emergencia de la vacuna Pfizer-BioNTech COVID-19" . Noticias árabes . 13 de diciembre de 2020 . Consultado el 15 de diciembre de 2020 .
- ^ "Liechtenstein - rastreador de vacunas COVID19" . covid19.trackvaccines.org . Consultado el 19 de febrero de 2021 .
- ^ "México aprueba la vacuna Pfizer para uso de emergencia como Covid surge" . Bloomberg. 12 de diciembre de 2020 . Consultado el 12 de diciembre de 2020 .
- ^ "México autoriza el uso de emergencia de la vacuna contra el coronavirus de Pfizer-BioNTech" . The Economic Times . 12 de diciembre de 2020 . Consultado el 14 de enero de 2021 .
- ^ "LAS PRIMERAS VACUNAS LLEGAN A MÓNACO - Mañana comienza la campaña de vacunación COVID-19 / Actualités / Coronavirus (Covid-19) / Política y práctica / Portail du Gouvernement - Mónaco" . en.gouv.mc . Consultado el 19 de febrero de 2021 .
- ^ "Evaluación sólida antes de la aprobación de la vacuna por parte de Medsafe" . Ministerio de Salud . 3 de febrero de 2021 . Consultado el 6 de febrero de 2021 .
- ^ "Macedonia del Norte inicia las vacunas COVID-19 mientras Serbia busca destacar los esfuerzos regionales" . RadioFreeEurope / RadioLiberty . Consultado el 19 de febrero de 2021 .
- ^ "Omán emite licencia para importar vacuna Pfizer BioNTech Covid - TV" . Reuters. 15 de diciembre de 2020 . Consultado el 16 de diciembre de 2020 .
- ^ "Panamá aprueba la vacuna COVID-19 de Pfizer - Ministerio de Salud" . Yahoo! Finanzas . Consultado el 16 de diciembre de 2020 .
- ^ "PH autoriza la vacuna COVID-19 de Pfizer para uso de emergencia" . CNN Filipinas. 14 de enero de 2021 . Consultado el 14 de enero de 2021 .
- ^ "Qatar, Omán para recibir la vacuna Pfizer-BioNTech COVID-19 esta semana" . Reuters . Consultado el 24 de diciembre de 2020 .
- ^ a b c d e "Normas de salud pública (autorización de emergencia de la vacuna COVID-19), 2021" (PDF) . Gobierno de San Vicente y las Granadinas . 11 de febrero de 2021 . Consultado el 12 de febrero de 2021 .
- ^ "Singapur aprueba el uso de la vacuna COVID-19 de Pfizer" . NOTICIAS AP . 14 de diciembre de 2020 . Consultado el 15 de diciembre de 2020 .
- ^ "Surinam comienza la campaña de vacunación contra el coronavirus con dosis donadas" . Reuters. 23 de febrero de 2021 . Consultado el 28 de febrero de 2021 .
- ^ "Información del producto Comirnaty" (en alemán) . Consultado el 31 de enero de 2021 . [Debido a los datos clínicos incompletos en el momento de la evaluación de la solicitud de autorización, el medicamento de la Comirnaty está autorizado por un período limitado (Art. 9a Ley de Medicamentos).]
- ^ "Dubai aprueba la vacuna Pfizer-BioNTech que será gratuita" . Mujer de los Emiratos . 23 de diciembre de 2020 . Consultado el 28 de diciembre de 2020 .
- ^ Decreto del Ministerio de Salud de Ucrania sobre la aprobación de las vacunas Covishield y Comirnaty
- ^ "El regulador de medicamentos del Reino Unido da la aprobación para la primera vacuna COVID-19 del Reino Unido" . Agencia Reguladora de Medicamentos y Productos Sanitarios, Gobierno del Reino Unido. 2 de diciembre de 2020 . Consultado el 2 de diciembre de 2020 .
- ^ "Información para profesionales de la salud sobre la vacuna Pfizer / BioNTech COVID-19" . Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) . 8 de diciembre de 2020 . Consultado el 13 de diciembre de 2020 .
- ^ "Condiciones de autorización para la vacuna Pfizer / BioNTech COVID-19" . Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) . 3 de diciembre de 2020 . Consultado el 13 de diciembre de 2020 .
- ^ "Interior aplaude la inclusión de áreas insulares a través de la operación Warp Speed para recibir vacunas COVID-19" (Comunicado de prensa). Departamento del Interior de los Estados Unidos (DOI). 12 de diciembre de 2020 . Consultado el 13 de enero de 2021 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ Dorman B (6 de enero de 2021). "Asia Minute: Palau administra vacunas para mantener el país libre de COVID" . Radio pública de Hawaii . Consultado el 13 de enero de 2021 .
- ^ "La FDA toma medidas clave en la lucha contra COVID-19 al emitir una autorización de uso de emergencia para la primera vacuna COVID-19" (Comunicado de prensa). EE.UU. Administración de Drogas y Alimentos (FDA). 11 de diciembre de 2020 . Consultado el 11 de diciembre de 2020 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ McElwee, Joshua J. (11 de diciembre de 2020). "El Vaticano ofrecerá la vacuna contra el coronavirus a los residentes y al personal a principios de 2021" . Reportero Católico Nacional . Consultado el 9 de febrero de 2021 .
- ^ Menichetti, Massimiliano (11 de diciembre de 2020). "In Vaticano parte il piano vaccinale anticovid" . vatican.va (Comunicado de prensa) . Consultado el 9 de febrero de 2021 .
- ^ a b "Estado de las vacunas COVID-19 dentro del proceso de evaluación de la OMS EUL / PQ" (PDF) . Organización Mundial de la Salud (OMS).
- ^ "La OMS emite su primera validación de uso de emergencia para una vacuna COVID-19 y enfatiza la necesidad de un acceso global equitativo" . Organización Mundial de la Salud (OMS) (Comunicado de prensa). 31 de diciembre de 2020 . Consultado el 6 de enero de 2021 .
- ^ "Comirnaty" . Administración de bienes terapéuticos . 25 de enero de 2021 . Consultado el 25 de enero de 2021 .
- ^ Informe de evaluación pública australiana para BNT162b2 (ARNm) (PDF) (Informe). Administración de Productos Terapéuticos (TGA) . Consultado el 25 de enero de 2021 .
- ^ "Vacina da Pfizer é a 1ª a obter registro definitivo no Brasil" (en portugués). G1. 23 de febrero de 2021 . Consultado el 23 de febrero de 2021 .
- ^ "EPAR de la comunidad" . Agencia Europea de Medicamentos (EMA) . Consultado el 23 de diciembre de 2020 .
- ^ "Preguntas y respuestas: vacunación COVID-19 en la UE" . Comisión Europea . 21 de diciembre de 2020 . Consultado el 21 de diciembre de 2020 .
- ^ "Comirnaty" . Registro Sindical de Medicamentos . Consultado el 8 de enero de 2021 .
- ^ "COVID-19: Bóluefninu Comirnaty frá BioNTech / Pfizer hefur verið veitt skilyrt íslenskt markaðsleyfi" . Lyfjastofnun (en islandés) . Consultado el 26 de diciembre de 2020 .
- ^ "Japón aprueba la vacuna COVID-19 de Pfizer, primera para uso doméstico" . Nikkei Asia . 14 de febrero de 2021 . Consultado el 14 de febrero de 2021 .
- ^ Lim I (8 de enero de 2021). "Khairy: Malasia puede utilizar la vacuna Covid-19 de Pfizer ahora como registro condicional concedido" . El correo malayo . Consultado el 8 de enero de 2021 .
- ^ "Estado på koronavaksiner bajo godkjenning por 21.12.20" . Statens legemiddelverk (en noruego bokmål) . Consultado el 26 de diciembre de 2020 .
- ^ "Coronavirus: Arabia Saudita aprueba el uso de la vacuna Pfizer COVID-19" . Inglés Al Arabiya . 10 de diciembre de 2020 . Consultado el 10 de diciembre de 2020 .
- ^ Zimmer C, Corum J, Wee S (10 de junio de 2020). "Rastreador de vacunas contra el coronavirus" . The New York Times . Consultado el 12 de diciembre de 2020 .
- ^ "Serbia lidera la región en esperar vacunas COVID-19 en unos días" . BalkanInsight . 21 de diciembre de 2020 . Consultado el 26 de diciembre de 2020 .
- ^ "El primer envío de la vacuna Pfizer-BioNTech llega a Serbia" . Sitio web del gobierno serbio . 22 de diciembre de 2020 . Consultado el 26 de diciembre de 2020 .
- ^ Lee, Kyung-eun (27 de febrero de 2021). "Corea del Sur comienza a implementar las vacunas Pfizer en el segundo día del programa nacional de vacunación" . Noticias de Arirang . Consultado el 28 de febrero de 2021 .
- ^ Kim, Han-joo (5 de marzo de 2021). "Corea del Sur aprueba la vacuna COVID-19 de Pfizer en medio del impulso de inmunización" . Agencia de Noticias Yonhap . Consultado el 5 de marzo de 2021 .
- ^ "Un estudio abierto de la seguridad, tolerabilidad e inmunogenicidad de la vacuna" Gam-COVID-Vac "contra COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 17 de junio de 2020. NCT04436471 . Consultado el 5 de marzo de 2021 .
- ^ Jones, Ian; Roy, Polly (2 de febrero de 2021). "El candidato a vacuna Sputnik V COVID-19 parece seguro y eficaz" . The Lancet . 397 (10275): 642–643. doi : 10.1016 / S0140-6736 (21) 00191-4 . PMC 7906719 . PMID 33545098 .
- ^ Sagdiev, Rinat; Ivanova, Polina (16 de noviembre de 2020). "Rusia se centra en dosis de vacunas liofilizadas como solución de transporte" . Reuters . Moscú . Consultado el 5 de marzo de 2021 .
- ^ "Ensayo clínico de eficacia, seguridad e inmunogenicidad de la vacuna Gam-COVID-Vac contra COVID-19" . ClinicalTrials.gov . Archivado desde el original el 12 de septiembre de 2020 . Consultado el 11 de septiembre de 2020 .
- ^ Logunov DY, Dolzhikova IV, Shcheblyakov DV, Tukhvatulin AI, Zubkova OV, Dzharullaeva AS, et al. (Febrero de 2021). "Seguridad y eficacia de una vacuna COVID-19 heteróloga prime-boost heteróloga basada en vectores rAd26 y rAd5: un análisis intermedio de un ensayo de fase 3 controlado aleatorio en Rusia" . The Lancet . 397 (10275): 671–681. doi : 10.1016 / S0140-6736 (21) 00234-8 . ISSN 0140-6736 . PMC 7852454 . PMID 33545094 .
- ^ "Ensayo clínico de eficacia, seguridad e inmunogenicidad de la vacuna Gam-COVID-Vac contra COVID-19 en Bielorrusia" . ClinicalTrials.gov . Ministerio de Salud de la Federación de Rusia. 25 de septiembre de 2020 . Consultado el 18 de enero de 2021 .
- ^ Kumar, Shivani (1 de diciembre de 2020). "Sputnik-V de Rusia llega a la India para pruebas clínicas" . Tiempos del Hindustan .
- ^ "Ensayo clínico: 17 voluntarios recibieron la vacuna Sputnik V Covid-19 de Rusia en Pune" . El Indian Express . 6 de diciembre de 2020.
- ^ "Ensayo clínico de inmunogenicidad, seguridad y eficacia de la vacuna Gam-COVID-Vac contra COVID-19 en Venezuela" . ClinicalTrials.gov . Ministerio de Salud de la Federación de Rusia. 24 de noviembre de 2020 . Consultado el 18 de enero de 2021 .
- ^ "Ensayo clínico de inmunogenicidad, seguridad y eficacia de la vacuna Gam-COVID-Vac contra COVID-19 en Venezuela" . ClinicalTrials.gov . Ministerio de Salud de la Federación de Rusia. 24 de noviembre de 2020 . Consultado el 18 de enero de 2021 .
- ^ "Emiratos Árabes Unidos comienza los ensayos de la vacuna Sputnik V Covid-19 de Rusia" . Arena de ensayos clínicos . 8 de enero de 2021.
- ^ "Covid19: la Agencia Nacional de Productos Farmacéuticos registra la vacuna Sputnik V" . Servicio de prensa de Argelia . 10 de enero de 2021.
- ^ "Argentina ha registrado la vacuna Sputnik V basada en datos de ensayos clínicos rusos" (Comunicado de prensa). Centro Gamaleya . Consultado el 1 de enero de 2021 .
- ^ "Armenia aprueba la vacuna contra el coronavirus Sputnik V de Rusia - RDIF de Rusia" . Reuters. 1 de febrero de 2021 . Consultado el 1 de febrero de 2021 .
- ^ "Bahrein autoriza la vacuna Sputnik V COVID-19 para uso de emergencia - TV de Bahrein" . Reuters. 10 de febrero de 2021 . Consultado el 19 de febrero de 2021 .
- ^ "Bielorrusia registra la vacuna Sputnik V, en primer lugar fuera de Rusia - RDIF" . Reuters. 21 de diciembre de 2020 . Consultado el 22 de diciembre de 2020 .
- ^ "Ministerio de Salud de Bolivia - Bolivia y Rusia firman contrato para adquirir 5,2 millones de dosis de la vacuna Sputnik-V contra la COVID-19" . minsalud.gob.bo . Consultado el 1 de enero de 2021 .
- ^ a b "COVID-19: Egipto autoriza pinchazos del virus Sputnik V, AstraZeneca" . Gulf News . Consultado el 24 de febrero de 2021 .
- ^ "Sputnik V autorizado en Gabón" (Comunicado de prensa). Centro Gamaleya . Consultado el 17 de febrero de 2021 .
- ^ "Ghana aprueba la vacuna Sputnik V de Rusia para uso de emergencia - RDIF" . Reuters. 20 de febrero de 2021.
- ^ "Guatemala recibirá la vacuna Sputnik de Rusia en las próximas semanas" . Reuters. 24 de febrero de 2021.
- ^ "Guinea comienza a administrar la vacuna Sputnik V Covid-19 de Rusia" . Noticias de África . 31 de diciembre de 2020.
- ^ "La vacuna Sputnik V de Rusia amplía su alcance en América Latina" . CNN . 3 de marzo de 2021.
- ^ "Honduras aprueba el uso de la vacuna Sputnik V contra COVID-19" . Agencia de Noticias Xinhua. 25 de febrero de 2021.
- ^ "Irán aprueba la vacuna rusa contra el coronavirus Sputnik V" . Reuters. 26 de enero de 2021.
- ^ "Sputnik V autorizado en Irak" (Comunicado de prensa). PharmiWeb.com. 4 de marzo de 2021.
- ^ "Jordania aprueba la vacuna Sputnik V de Rusia para su uso contra COVID-19" (Comunicado de prensa). Reuters. 10 de marzo de 2021.
- ^ "Kazajstán comienza la vacunación masiva por el ruso Sputnik V" . 1 de febrero de 2021 . Consultado el 19 de febrero de 2021 .
- ^ "Marruecos, Kenia aprueban la vacuna contra el coronavirus ruso para su uso - RDIF" . 10 de marzo de 2021 . Consultado el 12 de marzo de 2021 .
- ^ a b "Laos declara seguras las vacunas Covid-19, más para ser inoculadas la próxima semana | The Star" . La estrella . Malasia . Consultado el 19 de febrero de 2021 .
- ^ "Líbano autoriza el uso de emergencia de la vacuna Sputnik V de Rusia" . Reuters. 5 de febrero de 2021.
- ^ "México, Alemania caliente a la vacuna contra el virus Sputnik V de Rusia" . The Jakarta Post . 3 de febrero de 2021.
- ^ "Mongolia aprueba la vacuna contra el coronavirus Sputnik V de Rusia - RDIF" . Punto Urdu. 9 de febrero de 2021.
- ^ "Montenegro y San Vicente aprueban la vacuna Sputnik V de Rusia - RDIF" . Reuters. 12 de febrero de 2021.
- ^ "Marruecos ordena un millón de dosis de la vacuna Sputnik V de Rusia" . Yabiladi. 11 de marzo de 2021.
- ^ "Myanmar registra la vacuna Sputnik V COVID-19 de Rusia" . TASS . Consultado el 19 de febrero de 2021 .
- ^ "Nicaragua aprueba la vacuna rusa COVID-19" . wsoctv. 3 de febrero de 2021.
- ^ "Vacuna Sputnik V COVID 19 de NRussia registrada en Macedonia del Norte" . TASS. 7 de marzo de 2021.
- ^ "El gobierno aprueba la vacuna rusa para 'uso de emergencia ' " . Amanecer . 24 de enero de 2021.
- ^ "Palestina se ha convertido en el primer país de Oriente Medio en registrar la vacuna Sputnik V" . RFID . 11 de enero de 2021.
- ^ "Paraguay aprueba la vacuna de Rusia Sputnik V: RDIF" . Reuters. 15 de enero de 2021 . Consultado el 15 de enero de 2021 .
- ^ a b c "Vacuna Sputnik V registrada en la República Srpska de Bosnia y Herzegovina" . TASS. 5 de febrero de 2021 . Consultado el 8 de febrero de 2021 .
- ^ Burki TK (noviembre de 2020). "La vacuna rusa para COVID-19" . La lanceta. Medicina respiratoria . 8 (11): e85 – e86. doi : 10.1016 / S2213-2600 (20) 30402-1 . PMC 7837053 . PMID 32896274 .
- ^ "San Marino compra la vacuna Sputnik:" Primeras dosis ya en los próximos días " " . Unioneonline . 20 de febrero de 2021.
- ^ "Agencija odobrila uvoz ruske vakcine Sputnjik V u Srbiju" . N1 (en serbio). 31 de diciembre de 2020.
- ^ "Sputnik V aprobado para su uso en Eslovaquia" . rdif.ru . Consultado el 1 de marzo de 2021 .
- ^ "Sri Lanka aprueba la vacuna Sputnik V de Rusia" . El hindú . 4 de marzo de 2021.
- ^ "Vacuna Sputnik V autorizada en Túnez" (Comunicado de prensa). Centro Gamaleya . Consultado el 30 de enero de 2021 .
- ^ "Emiratos Árabes Unidos aprueba la vacuna Sputnik de Rusia para uso de emergencia" . Tiempos de Khaleej . 21 de enero de 2021 . Consultado el 21 de enero de 2021 .
- ^ "Uruguay comenzará la vacunación covid 19 en abril de 2021" . India florece .
- ^ "Venezuela firma contrato para la adquisición de la vacuna rusa Sputnik V" (en español). Reuters. 29 de diciembre de 2020.
- ^ a b "Vietnam aprueba vacunas Covid-19 de Estados Unidos y Rusia para uso de emergencia" . VnExpress . Consultado el 26 de febrero de 2021 .
- ^ a b "Covid-19: Zimbabwe autoriza vacunas Sputnik V, Sinovac para uso de emergencia" . news24.com. 9 de marzo de 2021.
- ^ a b c "Angola, República del Congo y Djibouti aprueban la vacuna Sputnik V de Rusia" . Reuters. 3 de marzo de 2021.
- ^ "El regulador de drogas húngaro aprueba la vacuna Sputnik V: sitio web" . The Moscow Times . 7 de febrero de 2021.
- ^ "Sputnik V registrado en Kirguistán" . Centro Gamaleya ( Nota de prensa). 23 de febrero de 2021.
- ^ "Siria autoriza el uso de Sputnik-V" . Roya. 22 de febrero de 2021.
- ^ "Turkmenistán es el primero en Asia Central en haber registrado la vacuna" Sputnik V "" . Oriente . 18 de enero de 2021.
- ^ "Uzbekistán certifica la vacuna Sputnik de Rusia para uso masivo" . Agence France-Presse (Barron). 17 de febrero de 2021.
- ^ "AstraZeneca & Serum Institute of India firman acuerdo de licencia para 1 millón de dosis de la vacuna Oxford" . The Economic Times . Consultado el 15 de junio de 2020 .
- ^ "Vacuna Covid-19: Serum Institute se inscribe en 100 millones de dosis de vacunas para la India, países de ingresos bajos y medios" . El Financial Express . El 7 de agosto de 2020.
- ^ Walsh N, Shelley J, Duwe E, Bonnett W (27 de julio de 2020). "Las esperanzas del mundo de una vacuna contra el coronavirus pueden correr por las venas de estos trabajadores de la salud" . São Paulo : CNN . Archivado desde el original el 3 de agosto de 2020 . Consultado el 3 de agosto de 2020 .
- ^ Gallagher, James; Triggle, Nick (30 de diciembre de 2020). "Covid-19: vacuna Oxford-AstraZeneca aprobada para su uso en Reino Unido" . BBC . Consultado el 5 de marzo de 2020 .
- ^ Vacuna AstraZeneca COVID-19 (PDF) (Monografía del producto). AstraZeneca . 26 de febrero de 2021. 244627 . Consultado el 5 de marzo de 2021 .
- ^ "Un estudio multicéntrico aleatorizado, doble ciego, controlado con placebo de fase III en adultos para determinar la seguridad, eficacia e inmunogenicidad de AZD1222, una vacuna de vector de ChAdOx1 no replicante, para la prevención de COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 12 de mayo de 2020. NCT04383574. Archivado desde el original el 23 de agosto de 2020 . Consultado el 26 de agosto de 2020 .
- ^ a b Voysey M, Clemens SA, Madhi SA, Weckx LY, Folegatti PM, Aley PK, et al. (19 de febrero de 2021). "La administración de dosis única y la influencia del momento de la dosis de refuerzo en la inmunogenicidad y la eficacia de la vacuna ChAdOx1 nCoV-19 (AZD1222): un análisis conjunto de cuatro ensayos aleatorizados" . The Lancet . 397 (10277): 881–891. doi : 10.1016 / S0140-6736 (21) 00432-3 . Consultado el 10 de marzo de 2021 .
- ^ "Comienza el ensayo de la vacuna Oxford COVID-19 en Brasil" . Instituto Jenner . Archivado desde el original el 9 de septiembre de 2020 . Consultado el 26 de agosto de 2020 .
- ^ "Los ensayos finales de la vacuna Oxford COVID-19 se llevarán a cabo en estos 17 hospitales de la India" . menta . 19 de agosto de 2020.
- ^ Sediqi, Abdul Qadir (7 de febrero de 2021). "Las primeras dosis de la vacuna COVID-19 llegan a Afganistán desde la India" . Reuters . Consultado el 24 de febrero de 2021 .
- ^ "India dona 500.000 vacunas COVID a Afganistán" . Al Jazeera . Consultado el 24 de febrero de 2021 .
- ^ a b c "Información en relación con la vacunación contra la COVID-19" (PDF) . Govern d'Andorra . Consultado el 14 de marzo de 2021 .
- ^ "Regulador argentino aprueba vacuna AstraZeneca / Oxford COVID-19" . Reuters. 30 de diciembre de 2020 . Consultado el 30 de diciembre de 2020 .
- ^ "Bahrein aprueba la vacuna contra el coronavirus de Oxford / AstraZeneca producida en la India" . Saudigazette . 25 de enero de 2021 . Consultado el 30 de enero de 2021 .
- ^ "Vacuna de la Universidad de Oxford-Astrazeneca: Bangladesh lo aprueba para uso de emergencia" . The Daily Star . Consultado el 6 de enero de 2021 .
- ^ "Bangladesh aprueba la vacuna COVID-19 Oxford-AstraZeneca" . aa.com.tr . Consultado el 6 de enero de 2021 .
- ^ "La República Dominicana aprueba la vacuna de AstraZeneca contra la covid-19" . Agencia EFE (en español). 31 de diciembre de 2020.
- ^ "Ecuador aprueba el uso de la vacuna AstraZeneca para COVID-19" . Reuters . 24 de enero de 2021 . Consultado el 30 de enero de 2021 .
- ^ "El Salvador da luz verde a AstraZeneca, vacuna COVID-19 de la Universidad de Oxford" . Reuters. 30 de diciembre de 2020.
- ^ https://www.afro.who.int/news/arrival-covax-vaccines-raises-hope-gambia
- ^ "Guyana obtiene el primer lote de vacunas COVID-19; Secretaría de CARICOM para obtener 100 dosis" . 10 de febrero de 2021 . Consultado el 19 de febrero de 2021 .
- ^ "La enfermera administra la primera inyección de la vacuna AstraZeneca (ChAdOx1 nCoV-19) a Brinnet Bernarai en la Corporación del Hospital Público de Georgetown - OPS / OMS | Organización Panamericana de la Salud" . paho.org . Consultado el 19 de febrero de 2021 .
- ↑ a b Schmall E, Yasir S (3 de enero de 2021). "India aprueba la vacuna Oxford-AstraZeneca Covid-19 y 1 otra" . The New York Times . Consultado el 3 de enero de 2021 .
- ^ "BPOM Terbitkan Izin Penggunaan Darurat Vaksin Covid-19 AstraZeneca" . Kompas.com . Consultado el 10 de febrero de 2021 .
- ^ a b "Irak aprueba vacunas Sinopharm, AstraZeneca" . Big News Network.com . Consultado el 30 de enero de 2021 .
- ^ https://www.bbc.com/news/world-africa-56239136
- ^ https://www.voanews.com/covid-19-pandemic/kenya-receives-1m-vaccine-doses-will-distribute-health-workers-first
- ^ "Maldivas comienza a capacitar a los trabajadores de la salud sobre la distribución de la vacuna COVID-19 - Xinhua | English.news.cn" . Agencia de Noticias Xinhua . Consultado el 19 de febrero de 2021 .
- ^ AfricaNews (26 de enero de 2021). "Mauricio comienza a vacunar a los trabajadores sanitarios de primera línea contra el covid-19" . Africanews . Consultado el 24 de febrero de 2021 .
- ^ "México aprueba la vacuna AstraZeneca COVID-19, dice el ministro" . Reuters . 5 de enero de 2021 . Consultado el 14 de enero de 2021 .
- ^ "Myanmar lanza programa de vacunación COVID-19 a nivel nacional" . Noticias Xinhua . 27 de enero de 2021.
- ^ "Nepal aprueba la vacuna AstraZeneca COVID para uso de emergencia - declaración del gobierno" . Reuters. 15 de enero de 2021.
- ^ "Wetin sabi sobre la aprobación de NAFDAC del uso de la vacuna Oxford AstraZeneca para Nigeria" . BBC News Pidgin . Consultado el 24 de febrero de 2021 .
- ^ "Pakistán aprueba la vacuna AstraZeneca COVID-19 para uso de emergencia" . 16 de enero de 2021.
- ^ "Regulador filipino aprueba el uso de emergencia de la vacuna AstraZeneca" . Reuters . 28 de enero de 2021 . Consultado el 28 de enero de 2021 .
- ^ https://www.afro.who.int/news/rwanda-receives-covid-19-vaccines-through-covax
- ^ a b "Vacunas AstraZeneca y Moderna para ser administradas en Arabia Saudita" . Gulf News . Consultado el 19 de enero de 2021 .
- ^ https://www.reuters.com/article/health-coronavirus-serbia-vaccines-idUSL1N2KR03M
- ^ "Sri Lanka aprueba la vacuna en medio de advertencias de propagación del virus" . NOTICIAS AP . 22 de enero de 2021 . Consultado el 22 de enero de 2021 .
- ^ https://www.unicef.org/sudan/stories/covid-19-vaccination-sudan
- ^ https://www.unicef.org/press-releases/sudan-receives-first-delivery-covid-19-vaccines-over-800000-doses
- ^ "Surinam comienza la campaña de vacunación contra el coronavirus con dosis donadas" . Reuters . 23 de febrero de 2021 . Consultado el 28 de febrero de 2021 .
- ^ "Taiwán otorga autorización de emergencia para la vacuna AstraZeneca COVID-19" . Reuters. 20 de febrero de 2021 . Consultado el 13 de marzo de 2021 .
- ^ "Alimentos y medicamentos tailandeses registra la vacuna COVID-19 desarrollada por AstraZeneca" . Correo de Pattaya . 23 de enero de 2021.
- ^ https://www.togofirst.com/en/health/1602-7300-covid-19-first-vaccination-campaign-to-soon-begin
- ^ https://www.africanews.com/2021/03/10/uganda-starts-covid-19-vaccinations/
- ^ "COVID-19: vacuna AstraZeneca certificada para uso en Ucrania" . covid.unian.info . Consultado el 10 de marzo de 2021 .
- ^ "Información para profesionales de la salud sobre la vacuna COVID-19 AstraZeneca" . Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) . 30 de diciembre de 2020 . Consultado el 4 de enero de 2021 .
- ^ "Vacuna de la Universidad de Oxford / AstraZeneca autorizada por el regulador de medicamentos del Reino Unido" (Comunicado de prensa). Departamento de Salud y Asistencia Social. 30 de diciembre de 2020 . Consultado el 30 de diciembre de 2020 .
- ^ "Condiciones de autorización para la vacuna COVID-19 AstraZeneca" . Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) . 30 de diciembre de 2020 . Consultado el 4 de enero de 2021 .
- ^ "Vietnam aprueba la vacuna AstraZeneca COVID-19, acorta el Congreso del Partido Comunista" . CNA . Consultado el 5 de febrero de 2021 .
- ^ "Recomendaciones provisionales para el uso de la vacuna AZD1222 (ChAdOx1-S (recombinante)) contra COVID-19 desarrolladas por la Universidad de Oxford y AstraZeneca" . Organización Mundial de la Salud (OMS) . Consultado el 27 de febrero de 2021 .
- ^ "La vacuna AstraZeneca / Oxford Covid-19 obtiene la aprobación de emergencia de la OMS" . Forbes . Consultado el 16 de febrero de 2021 .
- ^ "Vacuna contra el coronavirus AstraZeneca aprobada para su uso en Australia por TGA" . ABC News . 16 de febrero de 2021 . Consultado el 16 de febrero de 2021 .
- ^ "TGA aprueba provisionalmente la vacuna COVID-19 de AstraZeneca" . Administración de Productos Terapéuticos (TGA) . 16 de febrero de 2021 . Consultado el 16 de febrero de 2021 .
- ^ "Brasil otorga plena aprobación a la vacuna de Oxford, pedidos Sputnik" . Francia 24 . Brasilia . Agence France-Presse . 12 de marzo de 2021 . Consultado el 13 de marzo de 2021 .
- ^ "Resumen de la decisión reglamentaria - Vacuna AstraZeneca COVID-19" . Health Canada . 26 de febrero de 2021 . Consultado el 26 de febrero de 2021 .
- ^ "Vacuna COVID-19 AstraZeneca: pendiente de decisión de la CE" . Agencia Europea de Medicamentos (EMA) . 28 de enero de 2021 . Consultado el 29 de enero de 2021 .
- ^ "EMA recomienda la vacuna COVID-19 AstraZeneca para autorización en la UE" . Agencia Europea de Medicamentos (EMA) (Comunicado de prensa). 29 de enero de 2021 . Consultado el 29 de enero de 2021 .
- ^ "Comisión Europea autoriza tercera vacuna segura y eficaz contra COVID-19" . Comisión Europea (Comunicado de prensa). 29 de enero de 2021 . Consultado el 29 de enero de 2021 .
- ^ a b "EU-Kommissionen har i dag udstedt en betinget marksføringstilladelse til AstraZeneca COVID-19- vacuna. Tilladelsen gælder i Danmark" . Lægemiddelstyrelsen (en danés) . Consultado el 12 de marzo de 2021 .
- ^ "La Agencia Islandesa de Medicamentos ha emitido una autorización de comercialización condicional para la vacuna AstraZeneca COVID-19" . covid.is . Consultado el 12 de marzo de 2021 .
- ^ a b Sipalan, Joseph; Donovan, Kirsten (3 de marzo de 2021). "Malasia aprueba el uso de las vacunas Sinovac, AstraZeneca COVID-19" . Reuters . Consultado el 7 de marzo de 2021 .
- ^ "La Comisión Europea ha aprobado ahora la vacuna AstraZeneca COVID-19. Esto significa que la vacuna está aprobada para su uso en Noruega" . vg . Consultado el 12 de marzo de 2021 .
- ^ Kim, Han-joo (10 de febrero de 2021). "Corea del Sur aprueba la vacuna COVID-19 de AstraZeneca para todos los adultos" . Agencia de Noticias Yonhap . Consultado el 10 de febrero de 2021 .
- ^ Maresca, Thomas (10 de febrero de 2021). "Corea del Sur aprueba la vacuna AstraZeneca COVID-19" . United Press International . Consultado el 10 de febrero de 2021 .
- ^ Xia, Shengli; Zhang, Yuntao; Wang, Yanxia; Wang, Hui; Yang, Yunkai; Gao, George; et al. (15 de octubre de 2020). "Seguridad e inmunogenicidad de una vacuna inactivada SARS-CoV-2, BBIBP-CorV: un ensayo de fase 1/2 aleatorizado, doble ciego, controlado con placebo" . Las enfermedades infecciosas de Lancet . 21 (1): 39–51. doi : 10.1016 / S1473-3099 (20) 30831-8 . PMC 7561304 . PMID 33069281 .
- ^ Elbahrawy, Farah; Lyu, Dong; Omar, Abeer; Che, Claire; Paton, James (9 de diciembre de 2020). "La vacuna Covid respaldada por el Estado de China tiene un 86% de eficacia, dice Emiratos Árabes Unidos" . Noticias de Bloomberg . Consultado el 5 de marzo de 2020 .
La vacuna de CNBG se puede transportar y almacenar a temperaturas refrigeradas normales.
- ^ Wee S, Qin A (30 de diciembre de 2020). "Una vacuna china Covid-19 ha demostrado ser eficaz, dice su fabricante" . The New York Times . Consultado el 30 de diciembre de 2020 .
- ^ Yang Y. "Un estudio para evaluar la eficacia, seguridad e inmunogenicidad de las vacunas inactivadas contra el SARS-CoV-2 (célula Vero) en una población sana de 18 años o más" . ClinicalTrials.gov . Archivado desde el original el 14 de septiembre de 2020 . Consultado el 15 de septiembre de 2020 .
- ^ "Ensayo clínico para evaluar la eficacia, inmunogenicidad y seguridad de la vacuna inactivada SARS-CoV-2 (COVID-19)" . ClinicalTrials.gov . Consultado el 28 de septiembre de 2020 .
- ^ "Un ensayo clínico de fase III para la vacuna inactivada de la neumonía por coronavirus nuevo (COVID-19) (células Vero)" . chictr.org.cn . Registro chino de ensayos clínicos (ChiCTR) . Consultado el 15 de diciembre de 2020 .
- ^ "Bahrein permite el uso del candidato a vacuna Sinopharm COVID-19 en trabajadores de primera línea" . MSN. Reuters . Consultado el 3 de noviembre de 2020 .
- ^ Biannchi, Walter (21 de febrero de 2021). "Argentina aprueba la vacuna Sinopharm COVID-19 para uso de emergencia" . Reuters . Consultado el 23 de febrero de 2021 .
- ^ "Bielorrusia comienza las vacunas COVID-19 con inyecciones chinas" . Belta. 15 de marzo de 2021 . Consultado el 16 de marzo de 2021 .
- ^ "Bolivia comienza la inoculación con golpes de Sinopharm | The Star" . La estrella . Malasia . Consultado el 28 de febrero de 2021 .
- ^ Rinith T (4 de febrero de 2021). "El Ministerio de Salud otorga autorización de uso de emergencia a la vacuna Sinopharm de China" . Khmer Times . Consultado el 4 de febrero de 2021 .
- ^ "Dominica: Melissa Skerrit recibe la vacuna Sinopharm COVID-19" . Noticias de WIC. 4 de marzo de 2021 . Consultado el 7 de marzo de 2021 .
- ^ "Egipto licencia la vacuna Sinopharm COVID-19 de China para uso de emergencia: ministro de salud - Xinhua | English.news.cn" . Agencia de Noticias Xinhua.
- ^ "Gabón recibe 100.000 dosis de la vacuna de Sinopharm de China" . Gabón 24.12 de marzo de 2021 . Consultado el 15 de marzo de 2021 .
- ^ "El lanzamiento de la vacuna Sinopharm comienza este fin de semana" . Noticias de Stabroek. 6 de marzo de 2021 . Consultado el 7 de marzo de 2021 .
- ^ "Hungría firma un acuerdo para la vacuna COVID-19 de China Sinopharm, primero en la UE" . Correo Nacional .
- ^ "Irán lanza la segunda fase de la campaña de inoculación masiva" . Tribuna financiera . 22 de febrero de 2021 . Consultado el 23 de febrero de 2021 .
- ^ "El primer lote de la vacuna china Sinopharm llega a Jordania" . Noticias de Roya . Consultado el 9 de enero de 2021 .
- ^ Crean, Rosabel. "China dona 50.000 dosis de la vacuna Sinopharm al Líbano | Noticias, Noticias del Líbano | THE DAILY STAR" . Estrella diaria . Consultado el 2 de marzo de 2021 .
- ^ "Macao recibe el primer lote de vacunas COVID-19" . IAG . 7 de febrero de 2021 . Consultado el 24 de febrero de 2021 .
- ^ Rasheed, Aishath Hanaan Hussain. "MFDA aprueba Pfizer, vacunas Sinopharm Covid-19 para uso de emergencia" . raajje.mv . Consultado el 16 de marzo de 2021 .
- ^ "Diputado PM y gobernador de la ciudad obtienen la primera dosis de la vacuna Sinopharm" . Agencia de Noticias MONTSAME . Consultado el 15 de marzo de 2021 .
- ^ "Covid-19: Marruecos autoriza el uso de la vacuna Sinopharm" . en.yabiladi.com .
- ^ Personal de Reuters (6 de marzo de 2021). "Mozambique espera vacunar a 16 millones contra el coronavirus en 2022" . Reuters . Consultado el 7 de marzo de 2021 .
- ^ Poudel, Arjun. "La vacuna Shinopharm de China obtiene autorización de uso de emergencia en Nepal" . Correo de Katmandú . Consultado el 19 de febrero de 2021 .
- ^ Shahzad A (19 de enero de 2021). "Pakistán aprueba la vacuna china Sinopharm COVID-19 para uso de emergencia" . Reuters.
- ^ "Perú otorga aprobación 'excepcional' para la vacuna Sinopharm COVID-19 - fuentes gubernamentales" . Reuters. 27 de enero de 2021.
- ^ Asala, Kizzi. "Senegal lanza campaña de vacunación contra COVID-19 con Sinopharm de China" . Africanews . Consultado el 23 de febrero de 2021 .
- ^ "Serbia se convierte en la primera nación europea en utilizar la vacuna Sinopharm de China" . RadioFreeEurope / RadioLiberty .
- ^ Thomas, Abdul Rashid (15 de marzo de 2021). "El presidente de Sierra Leona, Bio, lidera el camino en la toma de la vacuna COVID-19" . Telegraph de Sierra Leona . Consultado el 16 de marzo de 2021 .
- ^ Sequera, Vivian (1 de marzo de 2021). "Venezuela aprueba el uso de la vacuna contra el coronavirus de China Sinopharm" . Reuters . Consultado el 2 de marzo de 2021 .
- ^ Mutsaka, Farai (18 de febrero de 2021). "Zimbabwe comienza a administrar las vacunas Sinopharm de China" . La estrella . Consultado el 20 de febrero de 2021 .
- ^ "Bahrein aprueba la vacuna contra el coronavirus Sinopharm de China" . Industrias comerciales árabes . 13 de diciembre de 2020.
- ^ Kuo L. "China aprueba la vacuna contra el coronavirus de Sinopharm, la primera del país para uso general" . The Washington Post .
- ^ "El presidente Ramkalawan y la primera dama recibe la segunda dosis de la vacuna SinoPharm" . statehouse.gov.sc . Consultado el 5 de febrero de 2021 .
- ^ Wee S (9 de diciembre de 2020). "La vacuna china Covid-19 obtiene una pulsación clave, pero las dudas se arremolinan" . The New York Times . Consultado el 12 de diciembre de 2020 .
- ^ "Coronavirus: Emiratos Árabes Unidos autoriza el uso de emergencia de la vacuna para los trabajadores de primera línea" . El Nacional . Consultado el 24 de noviembre de 2020 .
- ^ "Sinovac dice que la vacuna COVID-19 es eficaz para prevenir la hospitalización, la muerte" . Reuters . 5 de febrero de 2021 . Consultado el 5 de marzo de 2021 .
- ^ Tan, Yvette (14 de enero de 2021). "Covid: ¿Qué sabemos sobre las vacunas contra el coronavirus de China?" . BBC . Consultado el 5 de marzo de 2020 .
- ^ AGENCIAS, SABAH DIARIO CON (25 de diciembre de 2020). "Turquía está preparada para recibir la vacuna COVID-19 'efectiva' en medio de llamados a la inoculación" . Sabah diario . Consultado el 12 de febrero de 2021 .
- ↑ a b Soeriaatmadja W (11 de enero de 2021). "Indonesia otorga la aprobación de uso de emergencia a la vacuna de Sinovac, los ensayos locales muestran una eficacia del 65%" . Los tiempos del estrecho . Consultado el 11 de enero de 2021 .
- ^ "Sinovac: los resultados de Brasil muestran que la vacuna china es 50,4% efectiva" . BBC News . 13 de enero de 2021 . Consultado el 12 de febrero de 2021 .
- ^ "Las pruebas muestran que la vacuna contra el coronavirus de Sinovac de China es segura, dice el Instituto Butantan de Brasil" . Archivado desde el original el 29 de octubre de 2020 . Consultado el 29 de octubre de 2020 .
- ^ "Chile inicia estudio clínico para vacuna COVID-19" . Archivado desde el original el 11 de octubre de 2020 . Consultado el 29 de octubre de 2020 .
- ^ "Ensayo clínico de fase III aleatorizado, doble ciego, controlado con placebo para la evaluación de la eficacia y seguridad de la vacuna contra el SARS-CoV-2 (célula Vero), inactivada" . ClinicalTrials.gov . 8 de octubre de 2020. Archivado desde el original el 20 de octubre de 2020 . Consultado el 22 de octubre de 2020 .
- ^ Aliyev J. "Azerbaiyán inicia la vacunación COVID-19" . Agencia Anadolu . Consultado el 7 de febrero de 2021 .
- ^ "Bolívia autoriza uso de vacinas Sputnik V e CoronaVac contra covid-19" . noticias.uol.com.br (en portugués) . Consultado el 6 de enero de 2021 .
- ^ McGeever J, Fonseca P (17 de enero de 2021). "Brasil autoriza el uso de emergencia de Sinovac, vacunas AstraZeneca, comienzan las inyecciones" . Reuters . Consultado el 17 de enero de 2021 .
- ^ Chanritheara, rasgado. "Camboya aprueba las vacunas AstraZeneca y Sinovac para uso de emergencia COVID-19" . Camboya . Consultado el 12 de febrero de 2021 .
- ^ "Chile aprueba el uso de emergencia de la vacuna china de Sinovac contra covid-19" . Francia 24.20 de enero de 2021 . Consultado el 30 de enero de 2021 .
- ^ Aliyev J. "Colombia aprueba el uso de emergencia de la vacuna CoronaVac" . Agencia Anadolu . Consultado el 7 de febrero de 2021 .
- ^ "Las vacunas anticovidias se agotan mientras República Dominicana espera la llegada de más dosis" . DominicanToday . Consultado el 10 de marzo de 2021 .
- ^ "Ecuador firma acuerdo con Sinovac para vacuna COVID-19 de 2 millones: ministro" . Correo Nacional . Consultado el 26 de febrero de 2021 .
- ^ "Uso de vacuna Sinovac autorizado" . Gobierno de Hong Kong. 18 de febrero de 2021 . Consultado el 19 de febrero de 2021 .
- ^ "BPOM otorga autorización de uso de emergencia para la vacuna Sinovac" . Tempo . 11 de enero de 2021 . Consultado el 11 de enero de 2021 .
- ^ a b c Liu R (6 de febrero de 2021). "China aprueba la vacuna COVID-19 de Sinovac Biotech para uso público en general" . Reuters . Consultado el 7 de febrero de 2021 .
- ↑ a b Barrera, Adriana (11 de febrero de 2021). "México aprueba las vacunas China CanSino y Sinovac COVID-19" . Reuters . Consultado el 11 de febrero de 2021 .
- ^ "CoronaVac, vacuna de alta eficacia" . Ministerio de Salud Publica Y Bienestar Social .
- ^ "Filipinas aprueba la vacuna COVID-19 de Sinovac para uso de emergencia" . Reuters. 22 de febrero de 2021.
- ^ Thepgumpanat, Panarat (22 de febrero de 2021). "Tailandia permite el uso de emergencia de la vacuna COVID-19 de Sinovac" . Reuters . Consultado el 23 de febrero de 2021 .
- ^ "Túnez aprovavacino cinese Sinovac" (en italiano). Agenzia Nazionale Stampa Associata (en italiano). 5 de marzo de 2021 . Consultado el 7 de marzo de 2021 .
- ^ "Turquía comenzará a inyectar la vacuna COVID-19 este fin de semana" . Anadolu . 11 de enero de 2021 . Consultado el 11 de enero de 2021 .
- ^ Zinets, Natalia (9 de marzo de 2021). "Ucrania aprueba la vacuna Sinovac COVID-19 de China" . Reuters . Consultado el 10 de marzo de 2021 .
- ^ "Estudio de seguridad e inmunogenicidad de la vacuna 2019-nCoV (mRNA-1273) para la profilaxis de la infección por SARS-CoV-2 (COVID-19)" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 16 de marzo de 2020. NCT04283461 . Consultado el 5 de marzo de 2021 .
- ^ "Los expertos de la OMS emiten recomendaciones sobre la vacuna Moderna COVID-19" . Reuters . Ginebra . 26 de enero de 2021 . Consultado el 5 de marzo de 2021 .
- ^ Hoja de datos para proveedores de atención médica que administran vacunas (hoja de datos). Administración de Alimentos y Medicamentos . Diciembre de 2020 . Consultado el 5 de marzo de 2021 .
- ^ "Resultados provisionales prometedores del ensayo clínico de la vacuna NIH-Moderna COVID-19" . Institutos Nacionales de Salud (NIH) . 15 de noviembre de 2020.
- ^ Baden L, Essink B, Kotloff K, Frey S, Novak R, Diemert D, et al. (Diciembre de 2020). "Eficacia y seguridad de la vacuna mRNA-1273 SARS-CoV-2" . Revista de Medicina de Nueva Inglaterra . 384 (5): 403–416. doi : 10.1056 / NEJMoa2035389 . PMC 7787219 . PMID 33378609 .
- ^ "Resumen de la decisión reglamentaria - Moderna vacuna COVID-19" . Health Canada, Gobierno de Canadá. 23 de diciembre de 2020 . Consultado el 23 de diciembre de 2020 .
- ^ "Ministerio de salud israelí autoriza la vacuna COVID-19 Moderna para su uso en Israel" . modernatx.com. 4 de enero de 2021 . Consultado el 4 de enero de 2021 .
- ^ "Singapur se convierte en el primero en Asia en aprobar la vacuna COVID-19 de Moderna" . Reuters . 3 de febrero de 2021 . Consultado el 3 de febrero de 2021 .
- ^ "Swissmedic otorga autorización para la vacuna COVID-19 de Moderna" (Comunicado de prensa). Agencia Suiza de Productos Terapéuticos (Swissmedic) . 12 de enero de 2020 . Consultado el 12 de enero de 2020 .
- ^ "Información para profesionales de la salud sobre la vacuna COVID-19 Moderna" . Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) . 8 de enero de 2021 . Consultado el 8 de enero de 2021 .
- ^ "Condiciones de autorización para la vacuna COVID-19 Moderna" . Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) . 8 de enero de 2021 . Consultado el 9 de enero de 2021 .
- ^ "La FDA toma medidas adicionales en la lucha contra COVID-19 al emitir una autorización de uso de emergencia para la segunda vacuna COVID-19" . EE.UU. Administración de Drogas y Alimentos (FDA) (Nota de prensa) . Consultado el 18 de diciembre de 2020 .
- ^ Oliver SE, Gargano JW, Marin M, Wallace M, Curran KG, Chamberland M, et al. (Diciembre de 2020). "Recomendación provisional del Comité Asesor sobre Prácticas de Inmunización para el uso de la vacuna COVID-19 Moderna - Estados Unidos, diciembre de 2020" (PDF) . MMWR. Informe Semanal de Morbilidad y Mortalidad . 69 (5152): 1653–56. doi : 10.15585 / mmwr.mm695152e1 . PMID 33382675 . S2CID 229945697 .
- ^ "COVID-19 Vaccine Moderna EPAR" . Agencia Europea de Medicamentos (EMA) . Consultado el 20 de enero de 2021 .
- ^ "La Comisión Europea autoriza la segunda vacuna segura y eficaz contra COVID-19" . Comisión Europea (Comunicado de prensa) . Consultado el 6 de enero de 2021 .
- ^ "EMA recomienda COVID-19 Vaccine Moderna para autorización en la UE" (Comunicado de prensa). Agencia Europea de Medicamentos. 6 de enero de 2021 . Consultado el 6 de enero de 2021 .
- ^ "Moderna vacuna COVID-19" . Registro Sindical de Medicamentos . Consultado el 14 de enero de 2021 .
- ^ a b "Endnu en la vacuna mod COVID-19 er godkendt af EU-Kommissionen" . Lægemiddelstyrelsen (en danés) . Consultado el 7 de enero de 2021 .
- ^ "COVID-19: Bóluefninu COVID-19 Vaccine Moderna frá hefur verið veitt skilyrt íslenskt markaðsleyfi" . Lyfjastofnun (en islandés) . Consultado el 7 de enero de 2021 .
- ^ "Estado på koronavaksiner bajo godkjenning el 6 de enero de 2021" . Statens legemiddelverk (en noruego bokmål) . Consultado el 7 de enero de 2021 .
- ^ Janssen Ad26.COV2.S Vacuna para la prevención de COVID-19 (Informe). Administración de Alimentos y Medicamentos . 26 de febrero de 2021. p. 6 . Consultado el 6 de marzo de 2021 .
La vacuna, conocida como Ad26.COV2.S, es una vacuna vectorizada de adenovirus tipo 26 (Ad26) de replicación incompetente que codifica una variante estabilizada de la proteína S del SARS-CoV-2.
- ↑ a b Ledford H (29 de enero de 2021). "La vacuna COVID de una sola inyección de J&J ofrece la esperanza de una protección más rápida" . Naturaleza . doi : 10.1038 / d41586-021-00119-7 . PMID 33526898 .
- ^ "Johnson & Johnson anuncia que el candidato a vacuna Janssen COVID-19 de un solo disparo alcanzó los criterios de valoración primarios en el análisis provisional de su ensayo ENSEMBLE de fase 3" (comunicado de prensa). Johnson y Johnson. 29 de enero de 2021 . Consultado el 29 de enero de 2021 .
- ^ "Bahrein primero en aprobar la vacuna Johnson & Johnson COVID-19 para uso de emergencia" . Reuters . 25 de febrero de 2021 . Consultado el 25 de febrero de 2021 .
- ^ "Bahrein se convierte en la primera nación en conceder el uso de emergencia de tiro de J&J" . ABC News . 25 de febrero de 2021 . Consultado el 25 de febrero de 2021 .
- ^ "La vacuna Johnson & Johnson COVID-19 se convierte en la cuarta en recibir la aprobación de Health Canada | CBC News" . Corporación Canadiense de Radiodifusión . Consultado el 5 de marzo de 2021 .
- ^ https://www.jnj.com/johnson-johnson-single-shot-covid-19-vaccine-granted-conditional-marketing-authorization-by-european-commission
- ^ "Coronavirus: Sudáfrica lanza programa de vacunación" . BBC News . 17 de febrero de 2021 . Consultado el 19 de febrero de 2021 .
- ^ "La FDA emite autorización de uso de emergencia para la tercera vacuna COVID-19" . EE.UU. Administración de Drogas y Alimentos (FDA) (Nota de prensa). 27 de febrero de 2021 . Consultado el 27 de febrero de 2021 .
- ^ https://www.fda.gov/media/146303/download
- ^ "La OMS aprueba la vacuna COVID-19 de J&J para la lista de emergencias" . Channel News Asia. 13 de marzo de 2021 . Consultado el 13 de marzo de 2021 .
- ^ "Comisión Europea autoriza cuarta vacuna segura y eficaz contra COVID-19" . Comisión Europea (Comunicado de prensa). 11 de marzo de 2021.
- ^ a b "EU-Kommissionen har i dag udstedt en betinget marksføringstilladelse til Johnson & Johnsons COVID-19- vacuna. Tilladelsen gælder i Danmark" . Lægemiddelstyrelsen (en danés) . Consultado el 12 de marzo de 2021 .
- ^ "La Agencia Islandesa de Medicamentos ha emitido una autorización de comercialización condicional" . covid.is . Consultado el 12 de marzo de 2021 .
- ^ "La Comisión Europea ha aprobado ahora la vacuna Johnson & Johnson. Esto significa que la vacuna está aprobada para su uso en la UE y Noruega" . vg . Consultado el 12 de marzo de 2021 .
- ^ Zhu FC, Guan XH, Li YH, Huang JY, Jiang T, Hou LH, et al. (Agosto de 2020). "Inmunogenicidad y seguridad de una vacuna COVID-19 con vectores de adenovirus de tipo 5 recombinante en adultos sanos de 18 años o más: un ensayo de fase 2 aleatorizado, doble ciego, controlado con placebo" . Lancet . 396 (10249): 479–88. doi : 10.1016 / s0140-6736 (20) 31605-6 . ISSN 0140-6736 . PMC 7836858 . PMID 32702299 . Resumen de laicos .
- ^ a b c d Peshimam, Gibran; Farooq, Umar (8 de febrero de 2021). "La vacuna COVID-19 de CanSinoBIO tiene una efectividad del 65,7% en los ensayos mundiales, dice un funcionario de Pakistán" . Reuters . Islamabad . Consultado el 5 de marzo de 2021 .
su régimen de dosis única y el requisito de almacenamiento normal en el frigorífico podrían convertirlo en una opción favorable para muchos países
- ^ "Ensayo clínico de vacuna recombinante de coronavirus nuevo (vector de adenovirus tipo 5) contra COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 13 de noviembre de 2020. NCT04540419 . Consultado el 17 de noviembre de 2020 .
- ^ Lazcano P (15 de noviembre de 2020). "Así funcionan las cuatro vacunas que se probarán en Chile" . La Tercera . Consultado el 15 de diciembre de 2020 .
- ^ Martinez AI (3 de noviembre de 2020). "CanSino Biologics entrega la vacuna COVID-19 a México para un ensayo de última etapa" . Reuters . Consultado el 4 de noviembre de 2020 .
- ^ Ng E (28 de octubre de 2020). "CanSino de China prueba la vacuna Covid-19 en naciones con 'alta carga de enfermedad'" . Poste matutino del sur de China . Consultado el 4 de noviembre de 2020 .
- ^ Nafisa E (9 de agosto de 2020). "CanSino para iniciar el ensayo de fase III de la vacuna COVID-19 en Arabia Saudita" . Reuters . Consultado el 4 de noviembre de 2020 .
- ^ Gou J. "Ensayo de fase III de una vacuna COVID-19 del vector de adenovirus en adultos de 18 años o más" . ClinicalTrials.gov . Archivado desde el original el 18 de septiembre de 2020 . Consultado el 17 de septiembre de 2020 .
- ^ Shahzad, Asif (12 de febrero de 2021). "Pakistán aprueba la vacuna china CanSinoBIO COVID para uso de emergencia" . Reuters . Consultado el 12 de febrero de 2021 .
- ^ "China aprueba dos vacunas nacionales COVID-19 más para uso público" . Reuters. 25 de febrero de 2021 . Consultado el 16 de marzo de 2021 .
- ^ "Vacuna de SARS-CoV-2 inactivada de virión completo (BBV152) para COVID-19 en voluntarios sanos" . ClinicalTrials.gov . NCT04471519.
- ^ a b "Covishield y Covaxin: lo que sabemos sobre las vacunas Covid-19 de la India" . BBC . 4 de marzo de 2021 . Consultado el 5 de marzo de 2020 .
Las dos dosis se administran con cuatro semanas de diferencia.
La vacuna se puede almacenar entre 2 ° C y 8 ° C.
- ^ "Un ensayo clínico de eficacia y seguridad de una vacuna COVID-19 en investigación (BBV152) en voluntarios adultos" . ClinicalTrials.gov . NCT04641481 . Consultado el 26 de noviembre de 2020 .
- ^ "Bharat Biotech recluta a 23.000 voluntarios para el ensayo clínico de fase 3 de Covaxin" . NDTV.com . 28 de diciembre de 2020 . Consultado el 3 de enero de 2021 .
- ^ "Covaxin mostró una eficacia provisional del 81%: Bharat Biotech en los resultados de la fase 3" . Business Standard India . 3 de marzo de 2021.
- ^ "Irán emite permiso para uso de emergencia para otras tres vacunas COVID-19: oficial" . IRNA Inglés . 17 de febrero de 2021.
- ^ Manral, Karan (4 de marzo de 2021). "Zimbabwe aprueba Covaxin, el primero en África en aprobar la vacuna Covid-19 fabricada en India" . Tiempos del Hindustan . Consultado el 6 de marzo de 2021 .
- ^ Benedyczak, Jakub (12 de febrero de 2021). Problemas de Rusia en la carrera de vacunas (Boletín). Instituto Polaco de Asuntos Internacionales . Consultado el 6 de marzo de 2021 .
el Sputnik V y EpiVacCorona se pueden transportar y almacenar a temperaturas de +2 a + 8 ° C
- ^ "La vacuna rusa EpiVacCorona no tiene efectos adversos" . Noticias de Oreanda . 13 de enero de 2021.
- ^ "О регистрации вакцины ФБУН ГНЦ ВБ" Вектор "Роспотребнадзора" ЭпиВакКорона " " . Rospotrebnadzor (en ruso). 14 de octubre de 2020.
- ^ "Comenzaron los ensayos de post-registro de la vacuna EpiVacCorona de Rusia" . La carta farmacéutica. 18 de noviembre de 2020.
- ^ "Turkmenistán registra vacunas para la prevención de enfermedades infecciosas" . Turkmenistán hoy . 29 de enero de 2021.
- ^ "La vacuna rusa" EpiVacCorona "se registró en Turkmenistán" . EN24 . 29 de enero de 2021.
- ^ a b "Un ensayo clínico de fase III para determinar la seguridad y eficacia de ZF2001 para la prevención de COVID-19" . ClinicalTrials.gov .
- ^ "La vacuna CAS COVID-19 de China induce una respuesta inmune en pruebas de etapa intermedia" . Reuters . Pekín . 23 de diciembre de 2020 . Consultado el 8 de marzo de 2021 .
- ^ Pinghui Z (20 de noviembre de 2020). "Quinta candidata a vacuna china Covid-19 lista para entrar en ensayos de fase 3" . Poste matutino del sur de China . Consultado el 26 de diciembre de 2020 .
- ^ Ying TP (7 de diciembre de 2020). "MYEG para realizar un ensayo clínico de fase 3 para la vacuna Covid-19 de China en Msia" . Nuevos tiempos del estrecho . Consultado el 28 de diciembre de 2020 .
- ^ Liu, Roxanne (15 de marzo de 2021). "La vacuna COVID-19 de China IMCAS obtuvo la aprobación de uso de emergencia en China" . Reuters . Consultado el 15 de marzo de 2021 .
- ^ Mamatkulov, Mukhammadsharif (1 de marzo de 2021). "Uzbekistán aprueba la vacuna COVID-19 desarrollada en China" . Reuters . Consultado el 2 de marzo de 2021 .
- ^ "Uzbekistán certifica vacuna china para luchar contra COVID-19" . China Daily . 2 de marzo de 2021 . Consultado el 8 de marzo de 2021 .
- ^ "Reunión informativa con el viceprimer ministro Tatyana Golikova, el ministro de salud Mikhail Murashko y el jefe de Rospotrebnadzor Anna Popova" . Gobierno de Rusia. 18 de enero de 2021 . Consultado el 20 de febrero de 2021 .
- ^ Ryumin, Alexander (20 de febrero de 2021). "Rusia registra su tercera vacuna COVID-19 CoviVac" . TASS . Moscú . Consultado el 6 de marzo de 2021 .
- ↑ a b Ivanova, Polina (8 de febrero de 2021). "Rusia aprueba su tercera vacuna COVID-19, CoviVac" . Reuters . Moscú . Consultado el 5 de marzo de 2021 .
La inyección de CoviVac se administra en dos dosis, con un intervalo de 14 días.
Se transporta y almacena a temperaturas normales del refrigerador, de 2 a 8 grados Celsius (35,6 a 46,4 Fahrenheit), dijo la viceprimera ministra Tatiana Golikova en una sesión informativa del gobierno en enero.
- ^ "Rusia aprueba su tercera vacuna COVID-19, CoviVac" . Reuters. 20 de febrero de 2021.
- ^ "Rastreador de vacunas COVID-19 (Elija la pestaña de vacunas, aplique filtros para ver los datos seleccionados)" . Instituto Milken. 8 de diciembre de 2020 . Consultado el 11 de diciembre de 2020 . Resumen de laicos .
- ^ "Proyecto de panorama de las vacunas candidatas COVID 19" . Organización Mundial de la Salud (OMS). 10 de diciembre de 2020 . Consultado el 11 de diciembre de 2020 .
- ^ Wadman M (noviembre de 2020). "El tiro largo" . Ciencia . 370 (6517): 649–653. Código Bibliográfico : 2020Sci ... 370..649W . doi : 10.1126 / science.370.6517.649 . PMID 33154120 .
- ^ Wadman M (28 de diciembre de 2020). "Novavax lanza un ensayo fundamental en Estados Unidos de la vacuna COVID-19 de caballo oscuro después de retrasos en la fabricación" . Ciencia . doi : 10.1126 / science.abg3441 .
- ^ Parekh N (24 de julio de 2020). "Novavax: una fábrica de proteínas SARS-CoV-2 para vencer a COVID-19" . Archivado desde el original el 22 de noviembre de 2020 . Consultado el 24 de julio de 2020 .
- ^ Chung YH, Beiss V, Fiering SN, Steinmetz NF (octubre de 2020). "Pioneros de la vacuna COVID-19 y su diseño de nanotecnología" . ACS Nano . 14 (10): 12522–12537. doi : 10.1021 / acsnano.0c07197 . PMC 7553041 . PMID 33034449 .
- ^ Medhi R, Srinoi P, Ngo N, Tran HV, Lee TR (25 de septiembre de 2020). "Estrategias basadas en nanopartículas para combatir COVID-19" . Nano materiales aplicados por ACS . 3 (9): 8557–8580. doi : 10.1021 / acsanm.0c01978 . PMC 7482545 .
- ^ "Un estudio sobre la eficacia, la respuesta inmune y la seguridad de una vacuna COVID-19 en adultos en el Reino Unido" . ClinicalTrials.gov . Consultado el 22 de noviembre de 2020 .
- ^ "Un estudio sobre la eficacia, la respuesta inmune y la seguridad de una vacuna COVID-19 en adultos con riesgo de SARS-CoV-2" . ClinicalTrials.gov . Consultado el 30 de diciembre de 2020 .
- ^ Keech C, Albert G, Cho I, Robertson A, Reed P, Neal S, et al. (Septiembre de 2020). "Ensayo de fase 1-2 de una vacuna de nanopartículas de proteína de pico recombinante de SARS-CoV-2" . La Revista de Medicina de Nueva Inglaterra . 383 (24): 2320–32. doi : 10.1056 / NEJMoa2026920 . PMC 7494251 . PMID 32877576 .
- ^ https://www.bloomberg.com/news/articles/2021-02-02/trudeau-signs-deal-to-make-novavax-covid-19-vaccine-in-canada
- ^ "EMA comienza a renovar la revisión de la vacuna COVID-19 de Novavax (NVX-CoV2373)" . Agencia Europea de Medicamentos (EMA) (Comunicado de prensa). 1 de diciembre de 2020 . Consultado el 12 de febrero de 2021 .
- ^ "Ucrania asegura 12 millones de dosis de vacuna AstraZeneca, Novavax COVID-19" . Reuters . 5 de febrero de 2021 . Consultado el 24 de febrero de 2021 .
- ^ "COVID-19: Ucrania puso en marcha el programa de vacunación contra el coronavirus" . euronews . 8 de febrero de 2021 . Consultado el 24 de febrero de 2021 .
- ↑ Held, Sergio (4 de marzo de 2021). "La vacuna candidata cubana Soberana 02 SARS-CoV-2 pasa a ensayos de fase III" . Bioworld . Consultado el 10 de marzo de 2021 .
- ^ "SOBERANA 02-FaseIII" . Registro Público Cubano de Ensayos Clínicos. RPCEC00000354.
- ^ "SOBERANA 02" . Registro Público Cubano de Ensayos Clínicos. 27 de octubre de 2020 . Consultado el 22 de enero de 2021 .
- ^ "SOBERANA 02A" . Registro Público Cubano de Ensayos Clínicos. 17 de diciembre de 2020 . Consultado el 22 de enero de 2021 .
- ^ "COVID-19" . CureVac . Consultado el 21 de diciembre de 2020 .
- ^ "COVID-19: un estudio clínico multicéntrico, aleatorizado, cegado por el observador, controlado con placebo, de fase 2b / 3 que evalúa la eficacia y seguridad de la vacuna de ARNm de SARS-CoV-2 en investigación CVnCoV en adultos de 18 años de edad y mayores" . Registro de ensayos clínicos de la UE . 19 de noviembre de 2020. 2020-003998-22 . Consultado el 19 de diciembre de 2020 .
- ^ "Un estudio para evaluar la seguridad, reactogenicidad e inmunogenicidad de la vacuna CVnCoV en adultos sanos" . ClinicalTrials.gov . 26 de junio de 2020. NCT04449276. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ "Un estudio de confirmación de dosis para evaluar la seguridad, reactogenicidad e inmunogenicidad de la vacuna CVnCoV en adultos sanos" . ClinicalTrials.gov . 17 de agosto de 2020. NCT04515147. Archivado desde el original el 23 de agosto de 2020 . Consultado el 28 de agosto de 2020 .
- ^ "Estudio de seguridad e inmunogenicidad de una vacuna inactivada contra el SARS-CoV-2 para prevenir contra COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 2 de junio de 2020. NCT04412538. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ "El estudio de eficacia, seguridad e inmunogenicidad de la vacuna inactivada contra el SARS-CoV-2 para prevenir contra COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos. NCT04659239 . Consultado el 10 de marzo de 2021 .
- ^ Yergaliyeva, Aidana (20 de diciembre de 2020). "Kazajstán comienza a vacunar a 3.000 voluntarios con QazCovid-in de fabricación propia" . The Astana Times . Consultado el 2 de marzo de 2021 .
- ^ a b "Inmunogenicidad, eficacia y seguridad de la vacuna QazCovid-in® COVID-19 - Vista de texto completo - ClinicalTrials.gov" . Clinicaltrials.gov .
- ^ "Reactogenicidad, seguridad e inmunogenicidad de la vacuna QazCovid-in® COVID-19 - Vista de texto completo - ClinicalTrials.gov" . Clinicaltrials.gov .
- ^ "Coronavirus | Zydus Cadila obtiene el visto bueno de DCGI para iniciar ensayos clínicos de fase 3 para la vacuna COVID-19" . El hindú . 3 de enero de 2021.
- ^ a b Thacker T. "Zydus Cadila para probar ZyCoV-D en 30.000 pacientes en ensayos de fase 3" . The Economic Times . Consultado el 16 de diciembre de 2020 .
- ^ "DBT-BIRAC apoyó al candidato de vacuna de ADN desarrollado de forma autóctona por Zydus Cadila, aprobado para ensayos clínicos de fase III" (Comunicado de prensa). Oficina de Información de Prensa . 3 de enero de 2021.
- ^ Rawat K, Kumari P, Saha L (febrero de 2021). "Vacuna COVID-19: una actualización reciente en las vacunas en línea, su diseño y estrategias de desarrollo" . Revista europea de farmacología . 892 : 173751. doi : 10.1016 / j.ejphar.2020.173751 . ISSN 1879-0712 . PMC 7685956 . PMID 33245898 .
- ^ "GSK, Medicago lanza ensayos clínicos fase 2/3 de la vacuna COVID-19 derivada de plantas" . PMLive . 13 de noviembre de 2020 . Consultado el 16 de noviembre de 2020 .
- ^ Chander V (14 de julio de 2020). "Medicago de Canadá comienza los ensayos en humanos de la vacuna COVID-19 a base de plantas" . Correo Nacional . Reuters. Archivado desde el original el 1 de noviembre de 2020 . Consultado el 14 de julio de 2020 .
- ^ Medicago (18 de noviembre de 2020). "Estudio de fase 2/3 aleatorizado, ciego, controlado con placebo para evaluar la seguridad, eficacia e inmunogenicidad de una vacuna COVID-19 de partículas recombinantes similares al coronavirus en adultos de 18 años de edad o mayores" . Ensayos clínicos . Consultado el 26 de noviembre de 2020 .
- ^ "SCB-2019 como vacuna COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 28 de mayo de 2020. NCT04405908. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ "Clover Biopharmaceuticals comienza ensayo de vacuna de fase I Covid-19" . Arena de ensayos clínicos. 20 de junio de 2020. Archivado desde el original el 11 de octubre de 2020 . Consultado el 25 de junio de 2020 .
- ^ "Acerca de nosotros" . Biofarmacéuticos Clover . Archivado desde el original el 11 de octubre de 2020 . Consultado el 1 de agosto de 2020 .
- ^ "Un estudio controlado de fase 2/3 de la vacuna de proteína S trimérica de SARS-CoV-2 recombinante adyuvante (SCB-2019) para la prevención de COVID-19 (SCB-2019)" . Biblioteca Nacional de Medicina de los Estados Unidos. NCT04672395 . Consultado el 10 de marzo de 2021 .
- ^ "Un estudio para evaluar la vacuna MVC-COV1901 contra COVID-19 en adultos (COVID-19)" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 11 de marzo de 2021 .
- ^ "Un estudio para evaluar la seguridad e inmunogenicidad de MVC-COV1901 contra COVID-19" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 11 de marzo de 2021 .
- ^ "A medida que Israel se vuelve loco por las vacunas, ¿la versión local perderá su oportunidad?" . Los tiempos de Israel . 29 de diciembre de 2020 . Consultado el 1 de enero de 2021 .
- ^ a b "VN inicia la inyección de la vacuna COVID-19 de cosecha propia en un ensayo en humanos de primera etapa" . Noticias de Vietnam . 17 de diciembre de 2020.
- ^ "Proyecto de panorama y rastreador de vacunas candidatas COVID-19" . QUIEN . 26 de febrero de 2021.
- ^ "¿Cuánto cuesta la primera vacuna COVID-19 fabricada en Vietnam?" . Voz de Vietnam . 11 de diciembre de 2020.
- ^ Chi Le, Anh Thu (26 de febrero de 2021). "Vietnam entra en la segunda fase de los ensayos de la vacuna Covid-19" . VnExpress .
- ^ "Seguridad, inmunogenicidad y eficacia de INO-4800 para COVID-19 en adultos sanos seronegativos con alto riesgo de exposición al SARS-CoV-2" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 12 de marzo de 2021 .
- ^ "Seguridad, tolerabilidad e inmunogenicidad de INO-4800 seguida de electroporación en voluntarios sanos para COVID19" . Clinicaltrials.gov . Biblioteca Nacional de Estados Unidos de Medincine . Consultado el 12 de marzo de 2021 .
- ^ "Estudio de la vacuna de ADN COVID-19 (AG0302-COVID19)" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 11 de marzo de 2021 .
- ^ "Acerca de AnGes - Introducción" . Anges, Inc . Archivado desde el original el 11 de octubre de 2020 . Consultado el 1 de agosto de 2020 .
- ^ "Estudio de fase II / III de la vacuna de ADN COVID-19 (AG0302-COVID19)" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 11 de marzo de 2021 .
- ^ "Estudio de formulaciones de vacunas de proteína recombinante contra COVID-19 en adultos sanos de 18 años y mayores" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 11 de marzo de 2021 .
- ^ "Estudio de la vacuna de proteína recombinante con adyuvante contra COVID-19 en adultos de 18 años de edad y mayores (VAT00002)" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 11 de marzo de 2021 .
- ^ "CTI y Arcturus Therapeutics anuncian el inicio de la dosificación del candidato a vacuna de ARNm COVID-19 STARR ™, LUNAR-COV19 (ARCT-021) en un estudio de fase 1/2" . Asociación de Bioindustria del Reino Unido. 13 de agosto de 2020. Archivado desde el original el 11 de octubre de 2020 . Consultado el 23 de agosto de 2020 .
- ^ "Estudio de dosis ascendente de la vacuna ARCT-021 de investigación SARS-CoV-2 en sujetos adultos sanos" . Clinicaltrials.gov . Archivado desde el original el 11 de octubre de 2020 . Consultado el 23 de agosto de 2020 .
- ^ "Estudio de extensión de etiqueta abierta para evaluar la seguridad y la inmunogenicidad a largo plazo de ARCT-021" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 13 de marzo de 2021 .
- ^ "Un ensayo que evalúa la seguridad y los efectos de una vacuna de ARN ARCT-021 en adultos sanos" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 10 de marzo de 2021 .
- ^ "Seguridad, tolerabilidad e inmunogenicidad del candidato a vacuna COVID-19 (VBI-2902a)" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 15 de marzo de 2021 .
- ^ "Estudio de seguridad e inmunogenicidad de GX-19N, una vacuna de ADN preventiva COVID-19 en adultos sanos" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 16 de marzo de 2021 .
- ^ "La vacuna Covid-19 del consorcio Genexine adquiere la aprobación para los ensayos clínicos en Corea" . 11 de junio de 2020 . Consultado el 1 de agosto de 2020 .
- ^ "Inicio de un estudio clínico japonés de TAK-919, candidato a vacuna COVID-19 de Moderna" . Takeda. 21 de enero de 2021 . Consultado el 11 de marzo de 2021 .
- ^ "Un estudio de TAK-919 en adultos japoneses sanos (COVID-19)" . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 11 de marzo de 2021 .
- ^ "Takeda proporciona actualizaciones sobre los ensayos clínicos de fase 1/2 de los candidatos a la vacuna COVID-19 de Novavax y Moderna en Japón" . Takeda. 24 de febrero de 2021 . Consultado el 11 de marzo de 2021 .
- ^ "Un estudio de TAK-019 en adultos japoneses sanos (COVID-19)" . Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 10 de marzo de 2021 .
- ^ a b "Acerca de nosotros" . Instituto Médico Genoinmune de Shenzhen. Archivado desde el original el 11 de octubre de 2020 . Consultado el 1 de agosto de 2020 .
- ^ Ward D, McCormack S (22 de mayo de 2020). "Ensayo clínico para evaluar la seguridad de una vacuna contra el coronavirus en hombres y mujeres sanos" . ISRCTN . doi : 10.1186 / ISRCTN17072692 . ISRCTN17072692.
- ^ "Vacuna GRAd-COV2 contra COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 7 de enero de 2021. NCT04528641.
- ^ "ReiThera anuncia que su candidata a vacuna GRAd-COV2 COVID-19 es bien tolerada e induce claras respuestas inmunitarias en sujetos sanos de 18 a 55 años" . ReiThera Srl . Yahoo! Finanzas. 24 de noviembre de 2020 . Consultado el 12 de enero de 2021 .
- ^ "Seguro de la nueva vacuna ReiThera, pico de respuesta a las 4 semanas" . ANSA . 5 de enero de 2021.
- ^ "Vacuna monovalente recombinante COVID19 (COVAX19)" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 1 de julio de 2020. NCT04453852. Archivado desde el original el 11 de octubre de 2020 . Consultado el 14 de julio de 2020 .
- ^ "Vaxine" . Archivado desde el original el 11 de octubre de 2020 . Consultado el 1 de agosto de 2020 .
- ^ "Un ensayo clínico de fase I para evaluar la seguridad, la tolerancia y la inmunogenicidad preliminar de diferentes dosis de una vacuna de ARNm del SARS-CoV-2 en la población de 18 a 59 años y 60 años y más" . Registro chino de ensayos clínicos . 24 de junio de 2020. ChiCTR2000034112. Archivado desde el original el 11 de octubre de 2020 . Consultado el 6 de julio de 2020 .
- ^ "Introducción de la empresa" . Biotecnología Walvax . Archivado desde el original el 11 de octubre de 2020 . Consultado el 1 de agosto de 2020 .
- ^ "Candidato a vacuna de ARNm indígena respaldado por DBT obtiene el visto bueno del controlador de medicamentos para iniciar ensayos clínicos en humanos" (Comunicado de prensa). Oficina de Información de Prensa . Consultado el 13 de enero de 2021 .
- ^ "Vacunas de ARNm - HGC019" . Gennova Biopharmaceuticals Limited . Consultado el 13 de enero de 2021 .
- ^ Raghavan P (15 de diciembre de 2020). "Gennova, con sede en Pune, comenzará los ensayos en humanos de su vacuna Covid 'pronto ' " . El Indian Express .
- ^ "Una fase I aleatorizada prospectiva de etiqueta abierta seguida sin problemas por un estudio de fase II para evaluar la seguridad, reactogenicidad e inmunogenicidad de la nueva vacuna Covid-19 de Biological E que contiene el dominio de unión al receptor del SARS-CoV-2 para la protección contra la enfermedad Covid-19 cuando se administra por vía intramuscular en un programa de dos dosis (0, 28D) a voluntarios sanos " . ctri.nic.in . Registro de ensayos clínicos de la India . 13 de enero de 2021. CTRI / 2020/11/029032. Archivado desde el original el 12 de noviembre de 2020.
- ^ "CEPI se asocia con Biological E Limited para avanzar en el desarrollo y fabricación de candidata a vacuna COVID-19" . cepi.net . CEPI . Consultado el 5 de marzo de 2021 .
- ^ Chui M (16 de noviembre de 2020). "La vacuna biológica E. Limited y Baylor COVID-19 comienza el ensayo clínico en la India" . Facultad de Medicina de Baylor .
- ^ Leo L (16 de noviembre de 2020). "Biological E inicia ensayos humanos de la vacuna" . Menta .
- ^ a b "Vacuna Bangavax: permiso solicitado para ensayo clínico" . The Daily Star . 18 de enero de 2021.
- ^ "Bangladesh se une a la carrera mundial de la vacuna COVID-19 con Bongavax para ensayo clínico" . arabnews.com . Noticias árabes . 8 de enero de 2021.
- ^ "Globe Biotech solicita la aprobación para ejecutar el ensayo clínico de la vacuna COVID" . bdnews24.com . Bdnews24.com . 17 de enero de 2021.
- ^ "Globe Biotech busca aprobación para ensayos de vacunas" . Nueva Era . 17 de enero de 2021.
- ^ a b "La vacuna contra el coronavirus fabricada en Canadá inicia ensayos clínicos en humanos" . Corporación Canadiense de Radiodifusión. 26 de enero de 2021.
- ^ a b "La vacuna VIDO COVID-19 pasa a las pruebas clínicas de fase 1" . globalnews.ca . 10 de febrero de 2021.
- ^ "Seguridad e inmunogenicidad de COVI-VAC, una vacuna viva atenuada contra COVID-19" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos.
- ^ "Un estudio de la seguridad y la respuesta inmune a dosis variables de una vacuna contra COVID-19 en adultos sanos" . Clinicaltrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos.
- ^ "COVIran Barakat: Irán lanza ensayos en humanos de su vacuna COVID" . aljazeera . 29 de diciembre de 2019.
- ^ a b "Seguridad e inmunogenicidad de una vacuna intranasal contra el SARS-CoV-2 (BBV154) para COVID-19" . ClinicalTrials.gov . Biblioteca Nacional de Medicina de los Estados Unidos . 5 de febrero de 2021. NCT04751682. Archivado desde el original el 24 de febrero de 2021 . Consultado el 5 de febrero de 2021 .
- ^ "Vacuna intranasal para Covid-19 | Bharat Biotech" . www.bharatbiotech.com . Consultado el 5 de marzo de 2021 .
- ^ "Ensayo de rango de dosis para evaluar la seguridad e inmunogenicidad de V590 (vacuna COVID-19) en adultos sanos (V590-001)" . ClinicalTrials.gov . 30 de septiembre de 2020 . Consultado el 26 de enero de 2021 .
- ^ "Un estudio para evaluar la seguridad, la tolerabilidad y la inmunogenicidad de V591 (vacuna COVID-19) en participantes sanos (V591-001)" . ClinicalTrials.gov . 4 de agosto de 2020 . Consultado el 26 de enero de 2021 .
- ^ "Comienza la inscripción de participantes para el ensayo de fase I del candidato a vacuna IAVI-Merck COVID-19" . IAVI . Consultado el 14 de marzo de 2021 .
- ^ "Vacuna V591 SARS-CoV-2" . www.precisionvaccinations.com . Consultado el 14 de marzo de 2021 .
- ^ "Merck suspende el desarrollo de candidatos a la vacuna SARS-CoV-2 / COVID-19; continúa el desarrollo de dos candidatos terapéuticos en investigación" . Merck (Comunicado de prensa). 25 de enero de 2021 . Consultado el 25 de enero de 2021 .
- ^ "Documento informativo de la FDA: vacuna Pfizer-BioNTech COVID-19" (PDF) . Administración de Drogas y Alimentos de los Estados Unidos. 10 de diciembre de 2020 . Consultado el 1 de enero de 2021 .
- ^ Branswell, Helen (2 de febrero de 2021). "Comparación de tres vacunas Covid-19: Pfizer, Moderna, J&J" . Stat . Consultado el 28 de febrero de 2021 .
- ^ Randolph HE, Barreiro LB (mayo de 2020). "Inmunidad colectiva: comprensión de COVID-19" . La inmunidad . 52 (5): 737–41. doi : 10.1016 / j.immuni.2020.04.012 . PMC 7236739 . PMID 32433946 .
- ^ "El límite de la FDA para la efectividad de la vacuna Covid-19 es del 50 por ciento. ¿Qué significa eso?" . NBC News . Consultado el 8 de enero de 2021 .
- ^ "EMA establece un objetivo de eficacia del 50% - con flexibilidad - para las vacunas COVID" . raps.org . Consultado el 8 de enero de 2021 .
- ^ Bartsch, Sarah; O'Shea, Kelly; Ferguson, Marie; Bottazzi, Maria; Matrimonio, Patrick; Strych, Ulrich; et al. (15 de julio de 2020). "La eficacia de la vacuna necesaria para una vacuna contra el coronavirus COVID-19 para prevenir o detener una epidemia como única intervención" . Revista estadounidense de medicina preventiva . 59 (4): 493–503. doi : 10.1016 / j.amepre.2020.06.011 . ISSN 0749-3797 . PMC 7361120 . PMID 32778354 . Consultado el 6 de marzo de 2021 .
- ^ Dean, Natalie; Madewell, Zachary (5 de marzo de 2021). "Comprensión del espectro de medidas de eficacia de la vacuna" . La opinión de BMJ . Consultado el 10 de marzo de 2021 .
- ^ "Vacuna Moderna COVID-19 - inyección cx-024414, suspensión" . DailyMed . Institutos Nacionales de Salud de EE. UU . Consultado el 20 de diciembre de 2020 .
- ^ "Vacuna Pfizer-BioNTech COVID-19 - inyección de ARN ingrediente bnt-162b2, suspensión" . DailyMed . Institutos Nacionales de Salud de EE. UU . Consultado el 14 de diciembre de 2020 .
- ^ Logunov DY, Dolzhikova IV, Shcheblyakov DV, Tukhvatulin AI, Zubkova OV, Dzharullaeva AS, et al. (Febrero de 2021). "Seguridad y eficacia de una vacuna COVID-19 heteróloga prime-boost heteróloga basada en vectores rAd26 y rAd5: un análisis intermedio de un ensayo de fase 3 controlado aleatorio en Rusia" . The Lancet . 397 (10275): 671–681. doi : 10.1016 / S0140-6736 (21) 00234-8 . ISSN 0140-6736 . PMC 7852454 . PMID 33545094 .
- ^ Wadman M, Cohen J (28 de enero de 2021). "La vacuna Novavax ofrece una eficacia del 89% contra COVID-19 en el Reino Unido, pero es menos potente en Sudáfrica" . Ciencia . doi : 10.1126 / science.abg8101 .
- ^ "La vacuna Novavax COVID-19 demuestra una eficacia del 89,3% en el ensayo de fase 3 del Reino Unido | Novavax Inc. - Sitio de IR" . ir.novavax.com . Consultado el 3 de marzo de 2021 .
- ^ "Emiratos Árabes Unidos dice que la vacuna Sinopharm tiene un 86% de eficacia contra COVID-19" . Reuters . Dubai . 9 de diciembre de 202 . Consultado el 10 de marzo de 2021 .
- ^ Wee S, Qin A (30 de diciembre de 2020). "Una vacuna china Covid-19 ha demostrado ser eficaz, dice su fabricante" . The New York Times . Consultado el 30 de diciembre de 2020 .
- ^ "Sinovac dice que la vacuna COVID-19 es eficaz para prevenir la hospitalización, la muerte" . Reuters . 5 de febrero de 2021 . Consultado el 10 de marzo de 2021 .
- ^ "Covid Shot de Sinovac demuestra una eficacia del 78% en el ensayo de Brasil" . Bloomberg. 7 de enero de 2021 . Consultado el 7 de enero de 2021 .
- ^ "Chile aprueba la vacuna contra el coronavirus chino" . Barron . Agence France-Presse . 20 de enero de 2021 . Consultado el 10 de marzo de 2021 .
- ^ "Vacuna Janssen COVID-19 - inyección de ad26.cov2.s, suspensión" . DailyMed . Institutos Nacionales de Salud de EE. UU . Consultado el 15 de marzo de 2021 .
- ^ "Covaxin de Bharat Biotech encontró 81% efectivo en ensayos de fase 3 provisionales" . menta . 3 de marzo de 2021.
- ^ "Bharat Biotech anuncia los resultados de la fase 3 de COVAXIN: la primera vacuna COVID-19 de la India demuestra una eficacia clínica provisional del 81%" (PDF) (Comunicado de prensa). Hyderabad : Bharat Biotech . 3 de marzo de 2021 . Consultado el 10 de marzo de 2021 .
- ^ a b Comisionado, Oficina del (23 de febrero de 2021). "Actualización del coronavirus (COVID-19): la FDA emite políticas para guiar a los desarrolladores de productos médicos que abordan las variantes del virus" . FDA . Consultado el 7 de marzo de 2021 .
- ↑ Mahase, Elisabeth (2 de marzo de 2021). "Covid-19: ¿Dónde estamos con las vacunas y variantes?" . BMJ . 372 : n597. doi : 10.1136 / bmj.n597 . ISSN 1756-1833 . PMID 33653708 . S2CID 232093175 .
- ^ "Dentro de la variante de coronavirus B.1.1.7" . The New York Times . 18 de enero de 2021 . Consultado el 29 de enero de 2021 .
- ↑ Muik, Alexander; Wallisch, Ann-Kathrin; Sänger, Bianca; Swanson, Kena A .; Mühl, Julia; Chen, Wei; Cai, Hui; Maurus, Daniel; Sarkar, Ritu; Türeci, Özlem; Dormitzer, Philip R. (29 de enero de 2021). "Neutralización del pseudovirus del linaje B.1.1.7 del SARS-CoV-2 por sueros humanos provocados por la vacuna BNT162b2" . Ciencia : eabg6105. doi : 10.1126 / science.abg6105 . ISSN 0036-8075 . PMID 33514629 .
- ^ Emary, Katherine RW; Golubchik, Tanya; Aley, Parvinder K .; Ariani, Cristina V .; Angus, Brian John; Bibi, Sagida; Blane, Beth; Bonsall, David; Cicconi, Paola; Charlton, Sue; Clutterbuck, Elizabeth (2021). "Eficacia de la vacuna ChAdOx1 nCoV-19 (AZD1222) contra SARS-CoV-2 VOC 202012/01 (B.1.1.7)" . Diario electrónico SSRN . doi : 10.2139 / ssrn.3779160 . ISSN 1556-5068 .
- ^ Mahase, Elisabeth (1 de febrero de 2021). "Covid-19: la eficacia de la vacuna Novavax es del 86% contra la variante del Reino Unido y del 60% contra la variante sudafricana" . BMJ : n296. doi : 10.1136 / bmj.n296 . ISSN 1756-1833 .
- ^ Kuchler, Hannah (25 de enero de 2021). "Moderna desarrolla una nueva vacuna para hacer frente a la cepa Covid mutante" . Financial Times . Consultado el 30 de enero de 2021 .
- ^ Liu, Yang; Liu, Jianying; Xia, Hongjie; Zhang, Xianwen; Fontes-Garfias, Camila R .; Swanson, Kena A .; Cai, Hui; Sarkar, Ritu; Chen, Wei; Cutler, Mark; Cooper, David; Weaver, Scott C .; Muik, Alexander; Sahin, Ugur; Jansen, Kathrin U .; Xie, Xuping; Dormitzer, Philip R .; Shi, Pei-Yong (17 de febrero de 2021). "Actividad neutralizante del suero obtenido con BNT162b2 - Informe preliminar" . Revista de Medicina de Nueva Inglaterra . doi : 10.1056 / nejmc2102017 . PMID 33596352 . Consultado el 25 de febrero de 2021 .
- ^ "Johnson & Johnson anuncia que el candidato a vacuna Janssen COVID-19 de un solo disparo alcanzó los criterios de valoración primarios en el análisis provisional de su ensayo ENSEMBLE de fase 3" (comunicado de prensa). Johnson y Johnson. 29 de enero de 2021 . Consultado el 29 de enero de 2021 .
- ^ Francis, Derek; Andy, Bruce (6 de febrero de 2021). "Oxford / AstraZeneca COVID disparó menos eficaz contra la variante sudafricana: estudio" . Reuters . Consultado el 8 de febrero de 2021 .
- ^ "Sudáfrica detiene el jab de AstraZeneca sobre nueva cepa" . BBC News . 7 de febrero de 2021 . Consultado el 8 de febrero de 2021 .
- ^ Booth, William; Johnson, Carolyn Y. (7 de febrero de 2021). "Sudáfrica suspende el lanzamiento de la vacuna Oxford-AstraZeneca después de que los investigadores informaran de una protección 'mínima' contra la variante del coronavirus" . The Washington Post . Londres . Consultado el 8 de febrero de 2021 .
Sudáfrica suspenderá el uso de la vacuna contra el coronavirus que están desarrollando la Universidad de Oxford y AstraZeneca después de que los investigadores descubrieron que brindaba una "protección mínima" contra las infecciones leves o moderadas por coronavirus causadas por la nueva variante detectada por primera vez en ese país.
- ^ "Covid: Sudáfrica detiene el lanzamiento de la vacuna AstraZeneca sobre una nueva variante" . BBC News . 8 de febrero de 2021 . Consultado el 12 de febrero de 2021 .
- ↑ a b c Tregoning JS, Russell RF, Kinnear E (25 de enero de 2018). "Vacunas contra la influenza adyuvantes" . Vacunas e inmunoterapias humanas . 14 (3): 550–64. doi : 10.1080 / 21645515.2017.1415684 . ISSN 2164-5515 . PMC 5861793 . PMID 29232151 .
- ^ a b c d Wang J, Peng Y, Xu H, Cui Z, Williams RO (5 de agosto de 2020). "La carrera de la vacuna COVID-19: desafíos y oportunidades en la formulación de vacunas" . AAPS PharmSciTech . 21 (6): 225. doi : 10.1208 / s12249-020-01744-7 . ISSN 1530-9932 . PMC 7405756 . PMID 32761294 .
- ^ "Vacunas contra el coronavirus (COVID-19)" . Our World in Data Obtenido de agencias de salud individuales .
- ^ a b c "Rastreador de datos COVID" . Centros para el Control y la Prevención de Enfermedades .
- ^ "El Papa Francisco y Benedicto XVI reciben la segunda dosis de la vacuna COVID-19" . Agencia Católica de Noticias .
- ^ "Vacunas contra el coronavirus (COVID-19) - Estadísticas e investigación" . Nuestro mundo en datos .
- ^ a b "Actualización sobre el ensayo de solidaridad de la OMS: acelerando una vacuna COVID-19 segura y eficaz" . Organización Mundial de la Salud. 27 de abril de 2020. Archivado desde el original el 30 de abril de 2020 . Consultado el 2 de mayo de 2020 .
Es vital que evaluemos tantas vacunas como sea posible, ya que no podemos predecir cuántas resultarán viables. Para aumentar las posibilidades de éxito (dado el alto nivel de desgaste durante el desarrollo de la vacuna), debemos probar todas las vacunas candidatas hasta que fallen. [La] OMS está trabajando para asegurar que todos ellos tengan la oportunidad de ser evaluados en la etapa inicial de desarrollo. Los resultados de la eficacia de cada vacuna se esperan dentro de tres a seis meses y esta evidencia, combinada con datos sobre seguridad, informará las decisiones sobre si se puede utilizar en una escala más amplia.
- ^ a b Gates B (30 de abril de 2020). "Explicación de la carrera de la vacuna: lo que necesita saber sobre la vacuna COVID-19" . Las notas de Gates. Archivado desde el original el 14 de mayo de 2020 . Consultado el 2 de mayo de 2020 .
- ^ a b Gates B (febrero de 2020). "Respondiendo a Covid-19: ¿Una pandemia única en un siglo?" . La Revista de Medicina de Nueva Inglaterra . 382 (18): 1677–79. doi : 10.1056 / nejmp2003762 . PMID 32109012 .
- ^ Weintraub R, Yadav P, Berkley S (2 de abril de 2020). "Una vacuna COVID-19 necesitará una distribución global equitativa" . Harvard Business Review . ISSN 0017-8012 . Archivado desde el original el 9 de junio de 2020 . Consultado el 9 de junio de 2020 .
- ↑ a b c Steenhuysen J, Eisler P, Martell A, Nebehay S (27 de abril de 2020). "Informe especial: países, empresas arriesgan miles de millones en la carrera por la vacuna contra el coronavirus" . Reuters. Archivado desde el original el 15 de mayo de 2020 . Consultado el 2 de mayo de 2020 .
- ^ Gartner A, Roberts L (3 de mayo de 2020). "¿Qué tan cerca estamos de una vacuna contra el coronavirus? Últimas noticias sobre los ensayos en el Reino Unido" . El telégrafo . ISSN 0307-1235 . Archivado desde el original el 4 de mayo de 2020 . Consultado el 3 de mayo de 2020 .
- ^ a b Thanh Le T, Andreadakis Z, Kumar A, Gómez Román R, Tollefsen S, Saville M, et al. (9 de abril de 2020). "El panorama del desarrollo de la vacuna COVID-19" . Nature Reviews Descubrimiento de medicamentos . 19 (5): 305–06. doi : 10.1038 / d41573-020-00073-5 . ISSN 1474-1776 . PMID 32273591 .
- ^ Le TT, Cramer JP, Chen R, Mayhew S (4 de septiembre de 2020). "Evolución del panorama de desarrollo de la vacuna COVID-19" . Nature Reviews Descubrimiento de medicamentos . 19 (10): 667–68. doi : 10.1038 / d41573-020-00151-8 . ISSN 1474-1776 . PMID 32887942 . S2CID 221503034 .
- ^ a b Yamey G, Schäferhoff M, Hatchett R, Pate M, Zhao F, McDade KK (mayo de 2020). "Garantizar el acceso mundial a las vacunas COVID-19" . Lancet . 395 (10234): 1405–06. doi : 10.1016 / S0140-6736 (20) 30763-7 . PMC 7271264 . PMID 32243778 .
CEPI estima que el desarrollo de hasta tres vacunas en los próximos 12 a 18 meses requerirá una inversión de al menos
2.000
millones
de
dólares estadounidenses. Esta estimación incluye
ensayos clínicos de
fase
1 de ocho candidatos a vacunas, progresión de hasta seis candidatos a través de la fase
2 y
3 ensayos, cumplimiento de los requisitos reglamentarios y de calidad para al menos tres vacunas y mejora de la capacidad de fabricación mundial de tres vacunas.
- ^ "Un ensayo aleatorizado internacional de vacunas candidatas contra COVID-19: Esquema del ensayo de vacuna de solidaridad" (PDF) . Organización Mundial de la Salud. 9 de abril de 2020. Archivado (PDF) desde el original el 12 de mayo de 2020 . Consultado el 9 de mayo de 2020 .
- ^ a b "COVAX: Garantizar el acceso equitativo global a las vacunas COVID-19" . GAVI. 2020. Archivado desde el original el 25 de septiembre de 2020 . Consultado el 28 de agosto de 2020 .
- ^ "Plan de I + D: una hoja de ruta de investigación global coordinada - 2019 nuevo coronavirus" (PDF) . Organización Mundial de la Salud. 1 de marzo de 2020. Archivado (PDF) desde el original el 15 de mayo de 2020 . Consultado el 10 de mayo de 2020 .
- ^ a b Azar A (4 de febrero de 2020). "Aviso de declaración en virtud de la Ley de preparación pública y preparación para emergencias para contramedidas médicas contra COVID-19" . Archivado desde el original el 25 de abril de 2020 . Consultado el 22 de abril de 2020 .
- ^ "Preguntas y respuestas: autorización de comercialización condicional de vacunas COVID-19 en la UE" . Comisión Europea. 11 de diciembre de 2020. Pregunta: ¿Cuál es la diferencia de responsabilidad entre la autorización de comercialización condicional de la UE y las autorizaciones de uso de emergencia? . Consultado el 29 de diciembre de 2020 .
- ^ Haahr, Thomas (7 de septiembre de 2020). "COVID-19: los eurodiputados quieren vacunas seguras, total transparencia y responsabilidad para las empresas" . Parlamento Europeo . La Sra. Gallina hizo hincapié en que las negociaciones con las empresas habían sido difíciles, pero subrayó que las empresas que desarrollan y fabrican vacunas COVID-19 serían responsables de acuerdo con las leyes vigentes y, si algo sale mal, podrían ser llevadas a los tribunales. Esto también se aplica a la compensación por defectos ocultos . Consultado el 29 de diciembre de 2020 .
- ^ So AD, Woo J (diciembre de 2020). "Reserva de vacunas de la enfermedad del coronavirus 2019 para el acceso global: análisis transversal" . BMJ . 371 : m4750. doi : 10.1136 / bmj.m4750 . ISSN 1756-1833 . PMC 7735431 . PMID 33323376 .
- ^ Adhanom Ghebreyesus, Tedros (18 de enero de 2021). "Palabras de apertura del Director General de la OMS en la 148ª reunión del Consejo Ejecutivo" . Organización Mundial de la Salud . Consultado el 25 de enero de 2021 .
- ^ "Bahrein aprueba el uso de la vacuna COVID-19 china" . ABC News . Consultado el 13 de diciembre de 2020 .
- ^ "Emiratos Árabes Unidos dice que la vacuna Sinopharm tiene un 86% de eficacia contra COVID-19" . Reuters . Consultado el 9 de diciembre de 2020 .
- ^ Holmes, Oliver (16 de febrero de 2021). "Israel bloqueó la entrada de las vacunas Covid en Gaza, dicen los palestinos" . The Guardian . Consultado el 17 de febrero de 2021 .
- ^ Rasgon, Adam (4 de febrero de 2021). "El éxito de las vacunas de Israel desata un debate sobre las desigualdades palestinas" . The New York Times . Consultado el 17 de febrero de 2021 .
- ^ Horton, Chris (17 de febrero de 2021). "Taiwán preocupada por China puede haber bloqueado la compra de vacunas" . Bloomberg . Consultado el 17 de febrero de 2021 .
- ^ "Jugar a la política con la pobreza: estrategia de vacuna COVID-19 de Sisi" . Fundación Carnegie para la Paz Internacional . Consultado el 25 de febrero de 2021 .
- ^ Strazewski, Len (9 de febrero de 2021). "Dr. Fauci: Variantes revelan la vacunación COVID-19 como trabajo global" . Asociación Médica Estadounidense . Consultado el 4 de marzo de 2021 .
- ^ Bergmark, Edward; Wierson, Arick (26 de febrero de 2021). "Opinión: sin un plan de vacuna global, las variantes del coronavirus podrían provocar un número incalculable de muertes" . CNN . Consultado el 4 de marzo de 2021 .
- ^ Lim, Paul (11 de marzo de 2021). "Los países ricos bloquean el impulso de las naciones en desarrollo para renunciar a los derechos de patente de la vacuna COVID" . www.euractiv.com . Consultado el 13 de marzo de 2021 .
- ^ "Diez problemas de salud que abordará la OMS este año" . Organización Mundial de la Salud (OMS). 2019. Archivado desde el original el 11 de noviembre de 2019 . Consultado el 26 de mayo de 2020 .
- ^ Malik AA, McFadden SM, Elharake J, Omer SB (2020). "Determinantes de la aceptación de la vacuna COVID-19 en los Estados Unidos" . EClinicalMedicine, la lanceta . 26 : 100495. doi : 10.1016 / j.eclinm.2020.100495 . ISSN 2589-5370 . PMC 7423333 . PMID 32838242 .
- ^ "Más en EE.UU. abrazar las vacunas contra la covid, muestra Pew Poll" . The New York Times . 5 de marzo de 2021 . Consultado el 8 de marzo de 2021 .
- ^ Funk, Cary (5 de marzo de 2021). "Una proporción cada vez mayor de estadounidenses dicen que planean recibir una vacuna COVID-19, o que ya la tienen" (PDF) . Pew Research Center Science & Society . Consultado el 8 de marzo de 2021 . Resumen de laicos .
- ^ Bekiempis, Victoria (21 de diciembre de 2020). " ' Estoy listo': Joe Biden recibe la vacuna contra el coronavirus en vivo por televisión" . The Guardian . Consultado el 26 de diciembre de 2020 .
- ^ Aratani, Lauren (18 de diciembre de 2020). "Mike Pence recibe la vacuna Covid-19 en la televisión en vivo: 'No sentí nada ' " . The Guardian . Consultado el 26 de diciembre de 2020 .
- ^ Gabbatt, Adam (3 de diciembre de 2020). "Obama, Clinton y Bush se comprometen a llevar la vacuna Covid a la televisión para mostrar su seguridad" . The Guardian . Consultado el 26 de diciembre de 2020 .
Otras lecturas
- Funk CD, Laferrière C, Ardakani A (2020). "Una instantánea de la carrera mundial de vacunas dirigidas al SARS-CoV-2 y la pandemia de COVID-19" . Front Pharmacol . 11 : 937. doi : 10.3389 / fphar.2020.00937 . PMC 7317023 . PMID 32636754 .
- Desarrollo y obtención de licencias de vacunas para prevenir el COVID-19: orientación para la industria (informe). Administración de Drogas y Alimentos de los Estados Unidos . Junio de 2020.
- Khandekar, Gauri, Otero-Iglesias Miguel (1 de marzo de 2021). "Cómo aumentar rápidamente la producción mundial de vacunas" Politico .
- Ramsay M, ed. (2020). "Capítulo 14a: COVID-19" . Inmunización contra enfermedades infecciosas . Salud Pública de Inglaterra.
- Levine, Hallie (23 de septiembre de 2020). "Las 5 etapas del desarrollo de la vacuna COVID-19: lo que necesita saber sobre cómo funciona un ensayo clínico" . Johnson y Johnson.
- Ware, Gemma (18 de febrero de 2021). "Cómo las leyes de patentes se interponen en el camino del lanzamiento mundial de la vacuna contra el coronavirus" The Conversation .
- Zimmer C, Sheikh K, Weiland N (20 de mayo de 2020). "Una nueva entrada en la carrera por una vacuna contra el coronavirus: esperanza" . The New York Times .
Protocolos de vacunación
- "Protocolo mRNA-1273-P301" (PDF) . Moderna .
- "Protocolo C4591001 PF-07302048 (Vacunas COVID-19 basadas en ARN BNT162)" (PDF) . Pfizer .
- "Protocolo AZD1222 - D8110C00001" (PDF) . AstraZeneca .
- "Protocolo VAC31518COV3001; Fase 3 (ENSEMBLE)" (PDF) . Vacunas y prevención de Janssen .
- "Protocolo VAC31518COV3009; Fase 3 (ENSEMBLE 2)" (PDF) . Vacunas y prevención de Janssen .
enlaces externos
| Wikiquote tiene citas relacionadas con: vacuna COVID-19 |
- "El panorama de la vacuna candidata a COVID-19" . Organización Mundial de la Salud (OMS) .
- Rastreador de vacunas COVID-19 . Enfoque regulatorio
- "Rastreador de medicamentos y vacunas Covid-19 de STAT" . Stat .
- "Vacunas COVID-19: desarrollo, evaluación, aprobación y seguimiento" . Agencia Europea de Medicamentos .
- "Desarrollo de vacunas - 101" . Administración de Drogas y Alimentos de los Estados Unidos .
- "Variantes y mutaciones del coronavirus" . The New York Times .
- MIT Lecture 10: Kizzmekia Corbett, Vaccines " en YouTube