| Atresia esofágica | |
|---|---|
| Otros nombres | Atresia esofágica |
 | |
| Tipos anatómicos comunes de atresia esofágica a) Atresia esofágica con fístula traqueoesofágica distal (86%), C. macroscópica b) Atresia esofágica aislada sin fístula traqueoesofágica (7%), A. macroscópica c) Fístula traqueoesofágica tipo H (4%), E. bruta [1] | |
| Especialidad | Pediatría |
La atresia esofágica es una afección médica congénita ( defecto de nacimiento ) que afecta el tracto digestivo . Hace que el esófago termine en una bolsa de extremo ciego en lugar de conectarse normalmente al estómago . Comprende una variedad de defectos anatómicos congénitos que son causados por un desarrollo embriológico anormal del esófago. Se caracteriza anatómicamente por una obstrucción congénita del esófago con interrupción de la continuidad de la pared esofágica. [ aclaración necesaria ]
Signos y síntomas
Este defecto congénito surge en la cuarta semana fetal, cuando la tráquea y el esófago deben comenzar a separarse.
Puede asociarse con trastornos del tabique traqueoesofágico . [2]
Complicaciones
Cualquier intento de alimentación podría causar neumonía por aspiración, ya que la leche se acumula en la bolsa ciega y se desborda hacia la tráquea y los pulmones. Además, una fístula entre la parte inferior del esófago y la tráquea puede permitir que el ácido del estómago fluya hacia los pulmones y cause daño. Debido a estos peligros, la afección debe tratarse lo antes posible después del nacimiento. [ cita requerida ]
Defectos congénitos asociados
Pueden coexistir otros defectos de nacimiento, particularmente en el corazón , pero a veces también en el ano, la columna vertebral o los riñones. Esto se conoce como asociación VACTERL debido a la participación de la columna vertebral, anorrectal, cardíaca, traqueal, esofágica, renal y de las extremidades. Se asocia con polihidramnios en el tercer trimestre. [ cita requerida ]
Diagnóstico
Esta condición puede ser visible, después de aproximadamente 26 semanas, en una ecografía . En la USG prenatal, el hallazgo de un estómago pequeño o ausente en el contexto de polihidramnios se consideró un síntoma potencial de atresia esofágica. Sin embargo, estos hallazgos tienen un valor predictivo positivo bajo. El signo de la bolsa en la parte superior del cuello es otro signo que ayuda en el diagnóstico prenatal de atresia esofágica y puede detectarse poco después del nacimiento, ya que el bebé afectado no podrá tragar su propia saliva . [ cita requerida ]
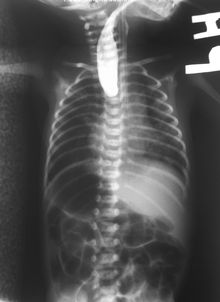
En una radiografía simple, no se verá un tubo de alimentación que atraviese el esófago y permanezca enrollado en la bolsa esofágica superior. [3]
Clasificación
Esta afección toma varias formas diferentes, a menudo involucrando una o más fístulas que conectan la tráquea con el esófago ( fístula traqueoesofágica ).
| Bruto [4] | Vogt [5] | Ladd [6] | Nombre (s) | Descripción | Frecuencia [1] |
|---|---|---|---|---|---|
| - | Tipo 1 | - | Agenesia esofágica | Ausencia completa muy rara del esófago, no incluida en la clasificación de Gross o Ladd | N / A |
| Escribe un | Tipo 2 | I | Atresia esofágica de "brecha larga", "pura" o "aislada" | Se caracteriza por la presencia de un “espacio” entre las dos bolsas ciegas esofágicas sin presencia de fístula. | 7% |
| Tipo B | Tipo 3A | II | Atresia esofágica con FTE proximal (fístula traqueoesofágica) | La bolsa esofágica superior se conecta de forma anormal a la tráquea. La bolsa esofágica inferior termina a ciegas. | 2-3% |
| Tipo C | Tipo 3B | III, IV | Atresia esofágica con TEF distal (fístula traqueoesofágica) | La bolsa esofágica inferior se conecta de forma anormal a la tráquea. La bolsa esofágica superior termina a ciegas. | 86% |
| Tipo D | Tipo 3C | V | Atresia esofágica con FTE proximal y distal (dos fístulas traqueoesofágicas) | Tanto la bolsa esofágica superior como la inferior establecen una conexión anormal con la tráquea en dos lugares separados y aislados. | <1% |
| Tipo E | Tipo 4 | - | TEF (fístula traqueoesofágica) ÚNICAMENTE sin atresia esofágica, tipo H | Esófago completamente intacto y capaz de sus funciones normales, sin embargo, existe una conexión anormal entre el esófago y la tráquea. No incluido en la clasificación de Ladd | 4% |
Tratamiento
Opciones de tratamiento
Los tratamientos para la afección varían según su gravedad. El tratamiento más inmediato y eficaz en la mayoría de los casos es una reparación quirúrgica para cerrar la (s) fístula (s) y volver a conectar los dos extremos del esófago entre sí. Aunque esto generalmente se hace a través de una incisión entre las costillas del lado derecho del bebé, en algunos centros se utiliza una técnica que utiliza tres pequeñas incisiones (toracoscopia). [ cita requerida ]
En una minoría de casos, la brecha entre los segmentos esofágicos superior e inferior puede ser demasiado larga para salvarla. En estas situaciones, los abordajes quirúrgicos tradicionales incluyen gastrostomía seguida de flexión gástrica, transposición colónica y transposición del yeyuno. [7] La flexión gástrica ha sido el enfoque preferido en muchos centros especializados, incluidos Great Ormond Street (Londres) y Mott Children's Hospital (Ann Arbor). [8] La gastrostomía, o sonda G, permite la alimentación por sonda al estómago a través de la pared abdominal. A menudo, también se realizará una esofagostomía cervical para permitir que la saliva que se ingiere drene por un orificio en el cuello. Meses o años después, el esófago puede repararse, a veces mediante el uso de un segmento de intestino que se eleva al tórax, interponiéndose entre los segmentos superior e inferior del esófago. [ cita requerida ]
Sin embargo, en algunos de estos casos denominados de brecha larga, se puede utilizar un tratamiento quirúrgico avanzado desarrollado por el Dr. John Foker, [9] para alargar y luego unir los segmentos esofágicos cortos. Usando la técnica de Foker, los cirujanos colocan suturas de tracción en los diminutos extremos del esófago y aumentan la tensión en estas suturas diariamente hasta que los extremos estén lo suficientemente cerca como para coserlos. El resultado es un esófago que funciona normalmente, prácticamente indistinguible de uno congénitamente bien formado. Desafortunadamente, los resultados han sido algo difíciles de replicar por otros cirujanos y la necesidad de múltiples operaciones ha moderado el entusiasmo por este enfoque. El tratamiento óptimo en los casos de atresia esofágica de intervalo largo sigue siendo controvertido. [10]
El método de compresión magnética es otro método para reparar la atresia esofágica de espacio largo. Este método no requiere reemplazar la sección faltante con injertos del intestino u otras partes del cuerpo. El uso de fuerza electromagnética para atraer juntos los extremos superior e inferior del esófago se intentó por primera vez en la década de 1970 mediante el uso de gránulos de acero atraídos entre sí mediante la aplicación de electroimanes externos al paciente. En la década de 2000 , el grupo de Mario Zaritzky y otros desarrollaron un refinamiento adicional . El método más nuevo utiliza imanes permanentes y un globo.
- Los imanes se insertan en la bolsa superior a través de la boca o la nariz del bebé, y la inferior a través del orificio de la sonda de alimentación por gastrotomía (que habría tenido que hacerse de todos modos para alimentar al bebé, por lo que no requiere ninguna cirugía adicional).
- La distancia entre los imanes se controla mediante un globo en la bolsa superior, entre el extremo de la bolsa y el imán. Esto también controla la fuerza entre los imanes para que no sea lo suficientemente fuerte como para causar daños.
- Una vez que los extremos del esófago se han estirado lo suficiente para tocarse, el imán superior se reemplaza por uno sin globo y la atracción magnética más fuerte hace que los extremos se fusionen ( anastomosis ). [11] [12] [13] [14]
En abril de 2015, Annalise Dapo se convirtió en la primera paciente en los Estados Unidos a la que se le corrigió la atresia esofágica con imanes. [11] [15]
Complicaciones del tratamiento
Las complicaciones postoperatorias pueden incluir una fuga en el sitio de cierre del esófago. A veces, se desarrollará una estenosis o un punto estrecho en el esófago, lo que dificultará la deglución. La estenosis esofágica generalmente se puede dilatar con instrumentos médicos. En la edad adulta, la mayoría de los niños con este trastorno tendrán problemas para tragar, acidez o ambos. La desmotilidad esofágica ocurre en 75-100% de los pacientes. Después de la reparación esofágica ( anastomosis ), la flacidez relativa de la antigua bolsa proximal (bolsa ciega, arriba) junto con la dismotilidad esofágica pueden causar acumulación de líquido durante la alimentación. Debido a la proximidad, el hinchamiento de la bolsa puede causar oclusión traqueal. Sigue una hipoxia severa ("episodios de muerte") y, a menudo, puede ser necesaria la intervención médica.
La traqueomalacia, un reblandecimiento de la tráquea, generalmente por encima de la carina ( carina de la tráquea ), pero a veces también extenso en el árbol bronquial inferior, es otra posible complicación grave. Se encuentran disponibles una variedad de tratamientos para la traqueomalacia asociada con la atresia esofágica. Si no es grave, la afección se puede tratar con expectativa, ya que la tráquea generalmente se endurecerá a medida que el bebé madura hasta el primer año de vida. Cuando solo la tráquea por encima de la carina está comprometida, una de las intervenciones "más simples" es la aortopexia.en el que el bucle aórtico está unido a la parte posterior del esternón, aliviando así mecánicamente la presión de la tráquea ablandada. Una intervención aún más sencilla es la colocación de un stent. Sin embargo, la proliferación de células epiteliales y la posible incorporación del stent en la tráquea pueden hacer que la extracción posterior sea peligrosa. [ cita requerida ]
La incidencia de asma, bronquitis, hiperreactividad bronquial e infecciones recurrentes en adolescentes y adultos sobrevivientes de atresia esofágica supera con creces la de sus pares sanos. [16] Durante la primera década de la reparación quirúrgica de la EA, hasta el 20% de los pacientes sucumbieron a la neumonía . A partir de ahí, la neumonía se ha mantenido como una de las principales complicaciones pulmonares y motivo de reingreso tras la reparación de la EA. [16] [17] Los factores de riesgo de neumonía dentro de los primeros cinco años de vida incluyen otras infecciones respiratorias agudas y una gran cantidad de dilataciones esofágicas. [18]
Epidemiología
Ocurre en aproximadamente 1 de cada 3000 nacidos vivos . [1]
La atresia esofágica congénita (EA) representa una falla del esófago para desarrollarse como un pasaje continuo. En cambio, termina como una bolsa ciega. La fístula traqueoesofágica ( FTE ) representa una abertura anormal entre la tráquea y el esófago. EA y TEF pueden ocurrir por separado o juntos. La EA y la FTE se diagnostican en la UCI al nacer y se tratan de inmediato. [ cita requerida ]
Se sospecha la presencia de EA en un lactante con salivación excesiva (babeo) y en un recién nacido con babeo que suele ir acompañado de asfixia, tos y estornudos. Cuando se alimentan, estos bebés tragan normalmente, pero comienzan a toser y luchar cuando el líquido regresa por la nariz y la boca. El bebé puede volverse cianótico (volverse azulado debido a la falta de oxígeno) y puede dejar de respirar a medida que el exceso de líquido de la bolsa ciega es aspirado (succionado) hacia la tráquea. La cianosis es el resultado del laringoespasmo (un mecanismo de protección que tiene el cuerpo para evitar la aspiración hacia la tráquea). Con el tiempo se desarrollará dificultad respiratoria. [ cita requerida ]
Si se nota alguno de los signos / síntomas anteriores, se introduce un catéter suavemente en el esófago para comprobar la resistencia. Si se observa resistencia, se realizarán otros estudios para confirmar el diagnóstico. Se puede insertar un catéter y se verá de color blanco en una película de rayos X normal para demostrar el final de la bolsa ciega. A veces, se coloca una pequeña cantidad de bario (líquido similar a la tiza) por la boca para diagnosticar los problemas. [ cita requerida ]
El tratamiento de EA y TEF es una cirugía para reparar el defecto. Si se sospecha EA o TEF, se interrumpen todas las alimentaciones orales y se inician los líquidos intravenosos. Se colocará al bebé para ayudar a drenar las secreciones y disminuir la probabilidad de aspiración. Los bebés con EA a veces pueden tener otros problemas. Se realizarán estudios para observar el corazón, la columna vertebral y los riñones. La cirugía para reparar la EA es esencial ya que el bebé no podrá alimentarse y es muy probable que desarrolle neumonía. Una vez que el bebé está en condiciones para la cirugía, se hace una incisión en el costado del pecho. Por lo general, el esófago se puede coser. Después de la cirugía, el bebé puede ser hospitalizado durante un período de tiempo variable. El cuidado de cada bebé es individualizado. Es muy común verlo en un recién nacido con ano imperforado . [cita requerida ]
Referencias
- ↑ a b c Spitz L (mayo de 2007). "Atresia esofágica" . Revista Orphanet de Enfermedades Raras . 2 : 24. doi : 10.1186 / 1750-1172-2-24 . PMC 1884133 . PMID 17498283 .
- ^ Clark DC (febrero de 1999). "Atresia esofágica y fístula traqueoesofágica" . Médico de familia estadounidense . 59 (4): 910–6, 919–20. PMID 10068713 .
- ^ Higano NS, Bates AJ, Tkach JA, Fleck RJ, Lim FY, Woods JC, Kingma PS (febrero de 2018). "Visualización pre y postoperatoria de atresia esofágica neonatal / fístula traqueoesofágica mediante resonancia magnética" . Revista de informes de casos de cirugía pediátrica . 29 : 5-8. doi : 10.1016 / j.epsc.2017.10.001 . PMC 5794017 . PMID 29399473 .
- ^ RE bruto (1953). La cirugía de la infancia y la niñez . Filadelfia: WB Saunders.
- ^ Vogt EC (noviembre de 1929). "Atresia esofágica congénita". Revista estadounidense de roentgenología . 22 : 463–465.
- ^ Ladd WE (1944). "El tratamiento quirúrgico de la atresia esofágica y fístulas traqueoesofágicas". La Revista de Medicina de Nueva Inglaterra . 230 (21): 625–637. doi : 10.1056 / nejm194405252302101 .
- ^ "Programa de tratamiento de atresia esofágica" . Hospital de Niños de Boston. Archivado desde el original el 4 de junio de 2011 . Consultado el 1 de junio de 2012 .
- ^ Hirschl RB, Yardeni D, Oldham K, Sherman N, Siplovich L, Gross E, et al. (Octubre de 2002). "Transposición gástrica para reemplazo esofágico en niños: experiencia con 41 casos consecutivos con especial énfasis en atresia esofágica" . Annals of Surgery . 236 (4): 531–9, discusión 539-41. doi : 10.1097 / 00000658-200210000-00016 . PMC 1422608 . PMID 12368682 .
- ^ "Atresia esofágica - síntomas, pruebas, tratamiento Foker" . Hospital de Niños de Boston. Archivado desde el original el 11 de julio de 2012 . Consultado el 1 de junio de 2012 .
- ^ Kunisaki SM, Foker JE (junio de 2012). "Avances quirúrgicos en el feto y neonato: atresia esofágica". Clínicas de Perinatología . 39 (2): 349–61. doi : 10.1016 / j.clp.2012.04.007 . PMID 22682384 .
- ↑ a b Mims B (10 de abril de 2015). "El procedimiento pionero de WakeMed corrige el raro trastorno del bebé" . WRAL.com . Raleigh-Durham: Capitol Broadcasting.
- ^ "Dr Zaritzky Pioneers opción no quirúrgica para bebés con atresia esofágica" . Departamento de Radiología . Universidad de Chicago. 13 de abril de 2015. Archivado desde el original el 14 de abril de 2015.
- ^ Oehlerking A, Meredith JD, Smith IC, Nadeau PM, Gomez T, Trimble ZA, Mooney DP, Trumper DL (junio de 2011). "Un tratamiento magnético no quirúrgico controlado hidráulicamente para la atresia esofágica de espacio largo" (PDF) . Revista de dispositivos médicos . 5 (2): 027511. doi : 10.1115 / 1.3589828 . Archivado desde el original (PDF) el 2 de abril de 2015.
- ^ Lovvorn III HN, Baron CM, Danko ME, Novotny NM, Bucher BT, Johnston KK, Zaritzky MF (2014). "Reparación por etapas de atresia esofágica: aproximación de bolsa y anastomosis magnética basada en catéter" . Revista de informes de casos de cirugía pediátrica . 2 (4): 170-175. doi : 10.1016 / j.epsc.2014.03.004 .
- ^ "El nuevo procedimiento no invasivo para bebés de WakeMed es el primero de su tipo en EE. UU." WTVD-TV . Raleigh-Durham. 10 de abril de 2015.
- ↑ a b Sistonen S, Malmberg P, Malmström K, Haahtela T, Sarna S, Rintala RJ, Pakarinen MP (noviembre de 2010). "Atresia esofágica reparada: morbilidad respiratoria y función pulmonar en adultos" . The European Respiratory Journal . 36 (5): 1106–12. doi : 10.1183 / 09031936.00153209 . PMID 20351029 .
- ^ Louhimo I, Lindahl H (1983). "Atresia esofágica: resultados primarios de 500 pacientes tratados consecutivamente". J Pediatr Surg . 18 (3): 217–229. doi : 10.1016 / s0022-3468 (83) 80089-x . PMID 6875767 .
- ^ Nurminen P, Koivusalo A, Hukkinen M, Pakarinen M (diciembre de 2019). "Neumonía después de la reparación de la incidencia de atresia esofágica y principales factores de riesgo". Revista europea de cirugía pediátrica . 29 (6): 504–509. doi : 10.1055 / s-0038-1675775 . hdl : 10138/300624 . PMID 30469161 .
Lectura adicional
- Harmon CM, Coran AG (1998). "Anomalías congénitas del esófago". Cirugía pediátrica (5ª ed.). St Louis, KY: División de Ciencias de la Salud de Elsevier Science. ISBN 0-8151-6518-8.
Enlaces externos
- Entrada de GenReview / NIH / UW sobre la atresia esofágica / descripción general de la fístula traqueoesofágica
| Clasificación | D
|
|---|---|
| Recursos externos |
|


