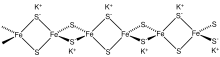
Clúster de hierro-azufre
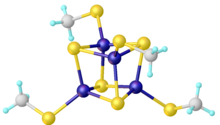
Los grupos de hierro-azufre (o grupos de hierro-azufre en la ortografía británica ) son conjuntos moleculares de hierro y sulfuro . Se discuten con mayor frecuencia en el contexto del papel biológico de las proteínas hierro-azufre , que son omnipresentes. [2] Se conocen muchos grupos de Fe-S en el área de la química organometálica y como precursores de análogos sintéticos de los grupos biológicos (ver Figura). Se cree que el último antepasado común universal tenía muchos grupos de hierro y azufre. [3]
Racimos organometálicos
Los grupos organometálicos de Fe – S incluyen los sulfidocarbonilos con la fórmula Fe 2 S 2 (CO) 6 , H 2 Fe 3 S (CO) 9 y Fe 3 S 2 (CO) 9 . También se conocen compuestos que incorporan ligandos de ciclopentadienilo, tales como (C 5 H 5 ) 4 Fe 4 S 4 . [4]
Materiales inorgánicos
Agrupaciones biológicas de Fe – S
Los cúmulos de hierro y azufre se encuentran en muchos sistemas biológicos, a menudo como componentes de proteínas de transferencia de electrones . Las proteínas ferredoxina son los grupos de Fe-S más comunes en la naturaleza. Cuentan con centros 2Fe – 2S o 4Fe – 4S. Ocurren en todas las ramas de la vida. [5]
Los grupos de Fe-S pueden clasificarse según su estequiometría de Fe: S [2Fe-2S], [4Fe-3S], [3Fe-4S] y [4Fe-4S]. [6] Los grupos [4Fe – 4S] se presentan en dos formas: ferredoxinas normales y proteínas de hierro de alto potencial (HiPIP). Ambos adoptan estructuras cuboidales, pero utilizan diferentes estados de oxidación. Se encuentran en todas las formas de vida. [7]
El par redox relevante en todas las proteínas Fe-S es Fe (II) / Fe (III). [7]
Se han sintetizado muchos grupos en el laboratorio con la fórmula [Fe 4 S 4 (SR) 4 ] 2− , que son conocidos por muchos sustituyentes R y con muchos cationes. Se han preparado variaciones que incluyen los cubanos incompletos [Fe 3 S 4 (SR) 3 ] 3− . [8]
Las proteínas de Rieske contienen grupos de Fe-S que se coordinan como una estructura 2Fe-2S y se pueden encontrar en el complejo III del citocromo bc1 unido a la membrana en las mitocondrias de eucariotas y bacterias. También forman parte de las proteínas del cloroplasto , como el complejo citocromo b 6 f en los organismos fotosintéticos. Estos organismos fotosintéticos incluyen plantas, algas verdes y cianobacterias , el precursor bacteriano de los cloroplastos. Ambos son parte de la cadena de transporte de electrones de sus respectivos organismos, lo cual es un paso crucial en la recolección de energía para muchos organismos. [9]
En algunos casos, los clústeres de Fe-S son redox inactivos, pero se propone que tengan funciones estructurales. Los ejemplos incluyen endonucleasa III y MutY. [5] [10]
Ver también
Referencias
- ^ Axel Kern, Christian Näther, Felix Studt, Felix Tuczek (2004). "Aplicación de un campo de fuerza universal a clústeres mixtos de Fe / Mo-S / Se Cubane y Heterocubane. 1. Sustitución de azufre por selenio en la serie [Fe4X4 (YCH3) 4] 2-; X = S / Se e Y = S / Se ". Inorg. Chem . 43 (16): 5003–5010. doi : 10.1021 / ic030347d . PMID 15285677 .Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )
- ^ SJ Lippard, JM Berg "Principios de la química bioinorgánica" Libros de ciencia de la universidad: Mill Valley, CA; 1994. ISBN 0-935702-73-3 .
- ^ Weiss, Madeline C., et al. "La fisiología y el hábitat del último ancestro común universal". Nature microbiology 1.9 (2016): 1-8.
- ^ Ogino, H., Inomata, S., Tobita, H. (1998). "Racimos abiológicos de hierro y azufre". Chem. Rev . 98 (6): 2093–2122. doi : 10.1021 / cr940081f . PMID 11848961 . Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )
- ↑ a b Johnson, DC, Dean, DR, Smith, AD, Johnson, MK (2005). "Estructura, función y formación de racimos biológicos hierro-azufre". Revisión anual de bioquímica . 74 : 247-281. doi : 10.1146 / annurev.biochem.74.082803.133518 . PMID 15952888 . Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )
- ^ Lill, Roland (2015). "Emisión de proteína hierro-azufre" . Biochimica et Biophysica Acta . 1853 (6): 1251-1252. doi : 10.1016 / j.bbamcr.2015.03.001 . PMC 5501863 . PMID 25746719 .
- ↑ a b Fisher, N (1998). "Transferencia de electrones intramolecular en [4Fe – 4S)]". The EMBO Journal : 849–858.
- ^ Rao, PV; Holm, RH (2004). "Análogos sintéticos de los sitios activos de proteínas de azufre de hierro". Chem. Rev . 104 (2): 527─559. doi : 10.1021 / Cr020615 + . PMID 14871134 . Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )
- ^ QUÍMICA INORGÁNICA BIOLÓGICA: estructura y reactividad . [Sl]: LIBROS DE CIENCIAS UNIVERSITARIAS. 2018. ISBN 978-1938787966. OCLC 1048090793 .
- ^ Guan, Y .; Manuel, RC; Arvai, AS; Parikh, SS; Mol, CD; Miller, JH; Lloyd, S .; Tainer, JA (diciembre de 1998). "MutY núcleo catalítico, estructuras de adenina mutantes y unidas definen la especificidad de la superfamilia de enzimas de reparación de ADN". Biología estructural de la naturaleza . 5 (12): 1058–1064. doi : 10.1038 / 4168 . ISSN 1072-8368 . PMID 9846876 . S2CID 22085836 .
enlaces externos
- Química de racimo
- Compuestos de hierro
- Compuestos de azufre