 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido (1 R , 2 S , 3 r , 4 R , 5 S , 6 s ) -Ciclohexano-1,2,3,4,5,6-hexol | |
| Otros nombres cis -1,2,3,5- trans -4,6-ciclohexanohexol Ciclohexanohexol Factor antialopecia de ratón Nucita Phaseomannita Phaseomannitol Factor de ojo antipantalla de rata Escilita (para el isómero escilo -inositol) Vitamina B 8 | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.027.295 |
| KEGG | |
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 6 H 12 O 6 | |
| Masa molar | 180,16 g / mol |
| Densidad | 1,752 g / cm 3 |
| Punto de fusion | 225 a 227 ° C (437 a 441 ° F; 498 a 500 K) |
| Farmacología | |
| A11HA07 ( OMS ) | |
| Riesgos | |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | 143 ° C (289 ° F; 416 K) |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
Inositol , o más precisamente myo -inositol , es un carbocíclico de azúcar que es abundante en el cerebro y otros tejidos de mamíferos; Interviene en la transducción de señales celulares en respuesta a una variedad de hormonas , neurotransmisores y factores de crecimiento y participa en la osmorregulación . [2] Es un alcohol de azúcar con la mitad del dulzor de la sacarosa (azúcar de mesa). Se produce naturalmente en humanos a partir de glucosa.. Un riñón humano produce alrededor de dos gramos por día. Otros tejidos también lo sintetizan, y la concentración más alta se encuentra en el cerebro, donde desempeña un papel importante al hacer que otros neurotransmisores y algunas hormonas esteroides se unan a sus receptores. [3] El inositol se promueve como un suplemento dietético en el tratamiento del síndrome de ovario poliquístico ( SOP ). Sin embargo, solo hay evidencia de muy baja calidad sobre su eficacia para aumentar la fertilidad en mujeres con SOP. [4]
Visión general
myo- inositol juega un papel importante como base estructural para una serie de mensajeros secundarios en las células eucariotas , los diversos fosfatos de inositol . Además, el inositol sirve como un componente importante de los lípidos estructurales fosfatidilinositol (PI) y sus diversos fosfatos, los lípidos fosfatidilinositol fosfato (PIP).
El inositol o sus fosfatos y lípidos asociados se encuentran en muchos alimentos, en particular frutas, especialmente melón y naranjas . [5] En las plantas, el hexafosfato de inositol, el ácido fítico o sus sales, los fitatos, sirven como depósitos de fosfato en las semillas, por ejemplo, en nueces y frijoles. [6] El ácido fítico también se encuentra en cereales con alto contenido de salvado . Sin embargo, el fitato no está directamente biodisponible para los humanos en la dieta, ya que no es digerible. Algunas técnicas de preparación de alimentos descomponen parcialmente los fitatos para cambiar esto. Sin embargo, el inositol en forma de glicerofosfolípidos , como se encuentra en ciertas sustancias derivadas de plantas comolecitinas , se absorbe bien y es relativamente biodisponible.
El myo- inositol (libre de fosfato) alguna vez se consideró un miembro del complejo de vitamina B , llamado Vitamina B 8 en este contexto. Sin embargo, debido a que el cuerpo humano la produce a partir de la glucosa , no es un nutriente esencial . [7]
Isómeros y estructura
El isómero myo -inositol es un compuesto meso , y por lo tanto ópticamente inactivo , porque tiene un plano de simetría . Por esta razón, meso -inositol es un nombre obsoleto para este compuesto. Además de myo -inositol, los otros estereoisómeros de origen natural son escilo -, muco -, D - quiro -, y neo -inositol , a pesar de que se producen en cantidades mínimas en la naturaleza. Los otros isómeros posibles son L - quiro -, alo -, epi - y cis -inositol. Como lo indican sus nombres, L - y D - quiro inositol son el único par de enantiómeros de inositol , pero son enantiómeros entre sí, no de myo -inositol. [8]
myo - scyllo - muco - chiro - neo - allo - epi - cis -
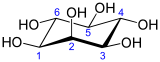
En su conformación más estable , el isómero myo -inositol asume la conformación de silla , que mueve el número máximo de hidroxilos a la posición ecuatorial, donde están más alejados entre sí. En esta conformación, el isómero myo natural tiene una estructura en la que cinco de los seis hidroxilos (el primero, tercero, cuarto, quinto y sexto) son ecuatoriales , mientras que el segundo grupo hidroxilo es axial . [9]
Biosíntesis
myo- inositol se sintetiza a partir de glucosa 6-fosfato (G6P) en dos pasos. Primero, la G6P es isomerizada por una enzima inositol-3-fosfato sintasa (por ejemplo, ISYNA1 ) a mio -inositol 1-fosfato, que luego es desfosforilado por una enzima inositol monofosfatasa (por ejemplo, IMPA1 ) para dar mio -inositol libre . En los seres humanos, la mayor parte del inositol se sintetiza en los riñones, seguidos de los testículos, por lo general en cantidades de unos pocos gramos por día. [2] a nivel periférico, el myo -inositol se convierte en D - chiro-inositol por una epimerasa específica. La actividad de esta epimerasa depende de la insulina. Cabe destacar que sólo una pequeña cantidad de myo -inositol se convierte en D - chiro -inositol y la conversión es irreversible. [10]
El inositol, el fosfatidilinositol y algunos de sus mono y polifosfatos funcionan como mensajeros secundarios en varias vías de transducción de señales intracelulares . Están involucrados en una serie de procesos biológicos, que incluyen:
- Transducción de señales de insulina [11]
- Ensamblaje del citoesqueleto
- Guía nerviosa ( epsin )
- Control de la concentración de calcio intracelular (Ca 2+ ) [12]
- Mantenimiento del potencial de la membrana celular [13]
- Desglose de grasas [14]
- Expresión genética [15] [16]
En una familia importante de vías, el 4,5-bisfosfato de fosfatidilinositol (PIP 2 ) se almacena en las membranas celulares hasta que es liberado por cualquiera de varias proteínas de señalización y se transforma en varios mensajeros secundarios, por ejemplo, diacilglicerol y trifosfato de inositol . [17]
Ácido fítico en plantas
El hexafosfato de inositol, también llamado ácido fítico o IP6, es la principal forma de almacenamiento de fósforo en muchos tejidos vegetales , especialmente en salvado y semillas . [18] El fósforo y el inositol en forma de fitato generalmente no están biodisponibles para los animales no rumiantes porque estos animales carecen de la enzima digestiva fitasa necesaria para eliminar los grupos fosfato. Los rumiantes pueden digerir fácilmente el fitato debido a la fitasa producida por los microorganismos del rumen . [19] Además, el ácido fítico también quela importantes minerales como calcio , magnesio , hierro y zinc , haciéndolos inabsorbibles y contribuyendo a las deficiencias minerales en personas cuyas dietas dependen en gran medida del salvado y las semillas para su ingesta de minerales, como ocurre en los países en desarrollo . [20] [21]
El inositol penta- (IP5), tetra- (IP4) y trifosfato (IP3) también se denominan "fitatos".
Uso en la fabricación de explosivos.
En la reunión de 1936 de la American Chemical Society , el profesor Edward Bartow de la Universidad de Iowa presentó un medio comercialmente viable para extraer grandes cantidades de inositol del ácido fítico presente naturalmente en el maíz de desecho. Como posible uso de la sustancia química, sugirió "nitrato de inositol" como una alternativa más estable a la nitroglicerina . [22] Hoy en día, el nitrato de inositol se utiliza para gelatinizar la nitrocelulosa , por lo que se puede encontrar en muchos explosivos modernos y propulsores sólidos de cohetes. [23]
Contra la sal de la carretera
Cuando las plantas están expuestas a concentraciones crecientes de sal de carretera , las células vegetales se vuelven disfuncionales y sufren apoptosis , lo que conduce a un crecimiento inhibido. El pretratamiento con inositol podría revertir estos efectos. [24]
Investigación y aplicaciones clínicas
Se han estudiado grandes dosis de inositol para el tratamiento de la depresión , pero se necesitan más estudios para determinar si este es un tratamiento eficaz. [25]
Se ha descubierto que el inositol tiene efectos moderados en pacientes con trastorno de pánico o trastorno obsesivo-compulsivo . [26] [27]
El inositol no debe administrarse de forma rutinaria para el tratamiento de bebés prematuros que tienen o están en riesgo de síndrome de dificultad respiratoria infantil (SDR). [28] Cabe destacar que el mioinositol ayuda a prevenir los defectos del tubo neural con una eficacia particular en combinación con el ácido fólico . [29]
El inositol se considera un tratamiento seguro y eficaz para el síndrome de ovario poliquístico (SOP). Actúa aumentando la sensibilidad a la insulina, lo que ayuda a mejorar la función ovárica y reduce el hiperandrogenismo . [30] También se ha demostrado que reduce el riesgo de enfermedad metabólica en personas con síndrome de ovario poliquístico. [31] Además, gracias a su función como segundo mensajero de la FSH, el mioinositol es eficaz para restaurar la proporción FSH / LH y la regularización del ciclo menstrual. [32] El papel del myo- inositol como segundo mensajero de la FSH conduce a una correcta maduración del folículo ovárico y, en consecuencia, a una mayor calidad de los ovocitos. Mejorar la calidad de los ovocitos en mujeres con o sin SOP,El myo -inositol se puede considerar como un posible enfoque para aumentar las posibilidades de éxito en las tecnologías de reproducción asistida. [33] [34] Por el contrario, D - quiro inositol puede deteriorar la calidad de los ovocitos en una forma dependiente de la dosis. [35] El alto nivel de DCI parece estar relacionado con niveles elevados de insulina recuperados en aproximadamente el 70% de las mujeres con SOP. [36] En este sentido, la insulina estimula la conversión irreversible de myo -inositol en D - chiro -inositol provocando una reducción drástica de myo -inositol. myo-La depleción de inositol es particularmente dañina para los folículos ováricos porque está involucrada en la señalización de FSH, que se ve afectada debido a la depleción de mio -inositol. [10] La evidencia reciente informa una mejora más rápida de los parámetros metabólicos y hormonales cuando estos dos isómeros se administran en su proporción fisiológica. La proporción plasmática de myo -inositol y D - chiro -inositol en sujetos sanos es 40: 1 de myo -y D - chiro -inositol respectivamente. [37] El uso de la proporción 40: 1 muestra la misma eficacia de myo-inositol solo pero en un tiempo más corto. Además, la relación fisiológica no afecta la calidad de los ovocitos. [38]
El uso de inositoles en el SOP está cobrando mayor importancia y se reporta una eficacia superior al 70% con un fuerte perfil de seguridad. Por otro lado, alrededor del 30% de los pacientes podrían mostrarse resistentes al inositol. [39] Nuevas pruebas sobre la etiopatogenia del SOP describen una alteración en la especie y la cantidad de cada cepa que caracteriza la flora gastrointestinal normal. Esta alteración podría conducir a un bajo grado crónico de inflamación y malabsorción. [40] Una posible solución podría estar representada por la combinación de mio -inositol y α-lactoalbúmina . Esta combinación muestra un efecto sinérgico en el aumento de la absorción de mioinositol. [41] Un estudio reciente informó que el myoLa combinación de -inositol y α-lactoalbúmina puede aumentar el contenido plasmático de mio -inositol en pacientes resistentes al inositol con una mejora relativa de los parámetros hormonales y metabólicos. [42]
A pesar de su efecto antinutriente, el ácido fítico tiene un uso potencial en endodoncia, odontología adhesiva, preventiva y regenerativa, y para mejorar las características y el rendimiento de los materiales dentales. [43]
Utilizar como agente de corte
El inositol se ha utilizado como adulterante o agente cortante para muchas drogas ilegales, como cocaína , metanfetamina y, a veces , heroína , [44] probablemente debido a su solubilidad, textura en polvo o dulzor reducido (50%) en comparación con azúcares más comunes.
El inositol también se utiliza como soporte cinematográfico sustituto de la cocaína en el cine . [45]
Fuentes nutricionales
El myo- inositol está presente de forma natural en una variedad de alimentos, aunque las tablas de composición de los alimentos no siempre distinguen entre la lecitina , la forma lipídica relativamente biodisponible y la forma fitato / fosfato biodisponible. [5] Los alimentos que contienen las concentraciones más altas de mioinositol y sus compuestos incluyen frutas, frijoles, granos y nueces. [5] Las frutas en particular, especialmente las naranjas y el melón, contienen las mayores cantidades de mioinositol . [46] También está presente en frijoles, nueces y granos, sin embargo, estos contienen grandes cantidades de myo -inositol en forma de fitato, que no está biodisponible sin la transformación por fitasa.enzimas. Bacillus subtilis , el microorganismo que produce el alimento fermentado natto , produce enzimas fitasa que pueden convertir el ácido fítico en una forma más biodisponible de polifosfato de inositol en el intestino. [47] Además, las especies de Bacteroides en el intestino secretan vesículas que contienen una enzima activa que convierte la molécula de fitato en fósforo biodisponible y polifosfato de inositol, que es una molécula de señalización importante en el cuerpo humano. [48]
myo- inositol también se puede encontrar como ingrediente en bebidas energéticas , [49] ya sea junto con o como un sustituto de la glucosa, [50] aparentemente para aumentar los niveles de serotonina y el estado de alerta. [51]
En los seres humanos, el mioinositol se produce de forma natural a partir de glucosa-6-fosfato a través de la desfosforilación enzimática. [46]
Referencias
- ^ Índice de Merck (11ª ed.). pag. 4883.
- ^ a b Parthasarathy, LK; Seelan, RS; Tobias, C .; Casanova, MF; Parthasarathy, Enfermera registrada (2006). Inositol 3-fosfato sintasa de mamíferos: su papel en la biosíntesis del inositol cerebral y su uso clínico como agente psicoactivo . Bioquímica subcelular. 39 . págs. 293–314. doi : 10.1007 / 0-387-27600-9_12 . ISBN 978-0-387-27599-4. PMID 17121280 .
- ^ Croze, ML; Soulage, CO (octubre de 2013). "Papel potencial e intereses terapéuticos del myo -inositol en enfermedades metabólicas". Biochimie . 95 (10): 1811–1827. doi : 10.1016 / j.biochi.2013.05.011 . PMID 23764390 .
- ^ Showell, MG; Mackenzie-Proctor, R .; Jordan, V .; Hodgson, R .; Farquhar, C. (2018). "Inositol para mujeres subfértiles con síndrome de ovario poliquístico" . La base de datos Cochrane de revisiones sistemáticas . 2018 (12): CD012378. doi : 10.1002 / 14651858.CD012378.pub2 . PMC 6516980 . PMID 30570133 .
- ^ a b c Clements, RS; Darnell, B. (septiembre de 1980). " Contenido de myo- inositol de alimentos comunes: desarrollo de una dieta alta en mio -inositol". La Revista Estadounidense de Nutrición Clínica . 33 (9): 1954-1967. doi : 10.1093 / ajcn / 33.9.1954 . PMID 7416064 . S2CID 4442333 .
- ^ "Ácido fítico" . www.phytochemicals.info . Archivado desde el original el 6 de agosto de 2017 . Consultado el 2 de octubre de 2017 .
- ^ Reynolds, JEF (1993). Martindale: La farmacopea adicional . 30 . Pensilvania: Distribuidores de libros de Rittenhouse. pag. 1379. ISBN 978-0-85369-300-0.
Un isómero de la glucosa que tradicionalmente se ha considerado una vitamina B, aunque tiene un estado incierto como vitamina y no se ha identificado un síndrome de deficiencia en el hombre.
- ^ Majumder, AL; Biswas, BB (3 de octubre de 2006). Biología de inositoles y fosfoinosítidos . Springer Science & Business Media. ISBN 9780387276007.
- ^ Brady, S .; Siegel, G .; Albers, RW; Precio, D. (2005). Neuroquímica básica: aspectos moleculares, celulares y médicos . Prensa académica. pag. 348. ISBN 9780080472072.
- ↑ a b Carlomagno, G .; Unfer, V .; Roseff, S. (2011). "El D - quiro paradoja inositol en el ovario". Fertilidad y esterilidad . 95 (8): 2515–6. doi : 10.1016 / j.fertnstert.2011.05.027 . PMID 21641593 .
- ^ Larner, J. (2002). " D - chiro -inositol - su papel funcional en la acción de la insulina y su déficit en la resistencia a la insulina" . Revista Internacional de Investigación Experimental en Diabetes . 3 (1): 47–60. doi : 10.1080 / 15604280212528 . PMC 2478565 . PMID 11900279 .
- ^ Gerasimenko, JV; Flowerdew, SE; Voronina, SG; Sukhomlin, TK; Tepikin, AV; Petersen, OH; Gerasimenko, OV (diciembre de 2006). "Los ácidos biliares inducen la liberación de Ca 2+ tanto del retículo endoplásmico como de las reservas de calcio intracelular ácido mediante la activación de los receptores de trifosfato de inositol y de los receptores de rianodina" . La revista de química biológica . 281 (52): 40154–40163. doi : 10.1074 / jbc.M606402200 . PMID 17074764 .
- ↑ Kukuljan, M .; Vergara, L .; Stojilković, SS (febrero de 1997). "Modulación de la cinética de oscilaciones de [Ca 2+ ] i inducidas por inositol 1,4,5-trifosfato por entrada de calcio en gonadotrofos pituitarios" . Revista biofísica . 72 (2 Pt 1): 698–707. Código bibliográfico : 1997BpJ .... 72..698K . doi : 10.1016 / S0006-3495 (97) 78706-X . PMC 1185595 . PMID 9017197 .
- ^ Rapiejko, PJ; Northup, JK; Evans, T .; Brown, JE; Malbon, CC (noviembre de 1986). "Proteínas G de las células grasas. Papel en la regulación hormonal del 1,4,5-trifosfato de inositol intracelular" . La revista bioquímica . 240 (1): 35–40. doi : 10.1042 / bj2400035 . PMC 1147372 . PMID 3103610 .
- ^ Shen, X .; Xiao, H .; Ranallo, R .; Wu, W.-H .; Wu, C. (enero de 2003). "Modulación de complejos remodeladores de cromatina dependientes de ATP por polifosfatos de inositol" . Ciencia . 299 (5603): 112-114. Código Bibliográfico : 2003Sci ... 299..112S . doi : 10.1126 / science.1078068 . PMID 12434013 . S2CID 8381889 .
- ^ Steger, DJ; Haswell, ES; Miller, AL; Wente, SR; O'Shea, EK (enero de 2003). "Regulación de la remodelación de la cromatina por polifosfatos de inositol" . Ciencia . 299 (5603): 114-116. Código Bibliográfico : 2003Sci ... 299..114S . doi : 10.1126 / science.1078062 . PMC 1458531 . PMID 12434012 .
- ^ Mathews, CK; Van Holde, KE; Ahern, KG (2000). Bioquímica (3ª ed.). San Francisco, CA: Benjamin Cummings. pag. 855. ISBN 978-0805330663. OCLC 42290721 .
- ^ "Ácido fítico" . www.phytochemicals.info . Archivado desde el original el 7 de marzo de 2018 . Consultado el 2 de mayo de 2018 .
- ^ Klopfenstein, TJ; Angel, R .; Cromwell, G .; Erickson, GE; Fox, DG; Parsons, C .; Satter, LD; Sutton, AL; Baker, DH (julio de 2002). "Modificación de la dieta animal para disminuir el potencial de contaminación por nitrógeno y fósforo" . Consejo de Ciencia y Tecnología Agrícola . 21 . Archivado desde el original el 11 de junio de 2011.
- ^ Hurrell, RF (septiembre de 2003). "Influencia de las fuentes de proteínas vegetales en la biodisponibilidad de oligoelementos y minerales" . La Revista de Nutrición . 133 (9): 2973S – 2977S. doi : 10.1093 / jn / 133.9.2973S . PMID 12949395 .
- ^ Comité de Protección de Alimentos; Junta de Alimentos y Nutrición; Consejo Nacional de Investigaciones (1973). "Fitatos" . Sustancias tóxicas presentes de forma natural en los alimentos . Academia Nacional de Ciencias. págs. 363–371 . ISBN 978-0-309-02117-3.
- ^ Laurence, WL (17 de abril de 1936). "El subproducto del maíz produce explosivos" . The New York Times . pag. 7. Archivado desde el original el 12 de mayo de 2013.
- ^ Ledgard, J. (2007). El Manual Preparatorio de Explosivos . pag. 366. ISBN 9780615142906.
- ^ Chatterjee, J .; Majumder, AL (septiembre de 2010). "Anomalías inducidas por la sal en las células mitóticas de la punta de la raíz de Allium cepa : prevención mediante pretratamiento con inositol". Protoplasma . 245 (1–4): 165–172. doi : 10.1007 / s00709-010-0170-4 . PMID 20559853 . S2CID 9128286 .
- ^ Taylor, MJ; Wilder, H .; Bhagwagar, Z .; Geddes, J. (2004). "Inositol para trastornos depresivos" . La base de datos Cochrane de revisiones sistemáticas (2): CD004049. doi : 10.1002 / 14651858.CD004049.pub2 . PMC 6984679 . PMID 15106232 .
- ^ Benjamin, J. (julio de 1995). "Ensayo cruzado, doble ciego, controlado con placebo del tratamiento con inositol para el trastorno de pánico". Soy J Psiquiatría . 152 (7): 1084–6. doi : 10.1176 / ajp.152.7.1084 . PMID 7793450 .
- ^ Fux, J. (1996). "Tratamiento con inositol del trastorno obsesivo compulsivo". Soy J Psiquiatría . 153 (9): 1219–21. doi : 10.1176 / ajp.153.9.1219 . PMID 8780431 .
- ^ Howlett, Alexandra; Ohlsson, Arne; Plakkal, Nishad (8 de julio de 2019). "Inositol en lactantes prematuros con riesgo o con síndrome de dificultad respiratoria" . La base de datos Cochrane de revisiones sistemáticas . 7 : CD000366. doi : 10.1002 / 14651858.CD000366.pub4 . ISSN 1469-493X . PMC 6613728 . PMID 31283839 .
- ↑ Cavalli, P .; Ronda, E. (2017). "Myoinositol: el puente (PONTI) para alcanzar un embarazo saludable" . Revista Internacional de Endocrinología . 2017 : 5846286. doi : 10.1155 / 2017/5846286 . PMC 5274721 . PMID 28243254 .
- ↑ Monastra, G .; Unfer, V .; Harrath, AH; Bizzarri, M. (enero de 2017). "La combinación del tratamiento con myo -inositol y D - chiro -inositol (40: 1) es eficaz para restaurar la función ovárica y el equilibrio metabólico en pacientes con SOP". Endocrinología Ginecológica . 33 (1): 1–9. doi : 10.1080 / 09513590.2016.1247797 . PMID 27898267 . S2CID 24836559 .
- ↑ Nordio, M .; Proietti, E. (mayo de 2012). "La terapia combinada con myo -inositol y D - chiro -inositol reduce el riesgo de enfermedad metabólica en pacientes con PCOS con sobrepeso en comparación con la suplementación de myo -inositol solo". Revista europea de ciencias médicas y farmacológicas . 16 (5): 575–581. PMID 22774396 .
- ^ Unfer, V .; et al. (2012). "Efectos de myo -inositol en mujeres con SOP: una revisión sistemática de ensayos controlados aleatorios". Endocrinología Ginecológica . 28 (7): 509-15. doi : 10.3109 / 09513590.2011.650660 . PMID 22296306 . S2CID 24582338 .
- ↑ Ciotta, L .; et al. (2011). "Efectos de la suplementación con myo -inositol sobre la calidad de los ovocitos en pacientes con SOP: un ensayo doble ciego". Revista europea de ciencias médicas y farmacológicas . 15 (5): 509-14. PMID 21744744 .
- ^ Papaleo, E .; et al. (2009). "Contribución de myo -inositol a la reproducción". Revista europea de obstetricia y ginecología y biología reproductiva . 147 (2): 120–3. doi : 10.1016 / j.ejogrb.2009.09.008 . PMID 19800728 .
- ^ Isabella, R .; Raffone, E. (2012). "¿Tiene necesidad de ovario D - quiro inositol?" . Revista de investigación ovárica . 5 (1): 14. doi : 10.1186 / 1757-2215-5-14 . PMC 3447676 . PMID 22587479 .
- ^ Moghetti, P. (2016). "Resistencia a la insulina y síndrome de ovario poliquístico". Diseño Farmacéutico Actual . 22 (36): 5526–5534. doi : 10.2174 / 1381612822666160720155855 . PMID 27510482 .
- ^ Facchinetti, F .; et al. (2015). "Los resultados de la Conferencia Internacional de Consenso de mio inositol y D - quiro inositol en Obstetricia y Ginecología: la relación entre el síndrome metabólico y síndrome de ovario poliquístico". Revista europea de obstetricia y ginecología y biología reproductiva . 195 : 72–6. doi : 10.1016 / j.ejogrb.2015.09.024 . PMID 26479434 .
- ↑ Colazingari, S .; et al. (2013). "La terapia combinada de mio inositol más D - quiro inositol, en lugar de D - quiro inositol, es capaz de mejorar los resultados de FIV: resultados de un ensayo controlado aleatorio". Archivos de Ginecología y Obstetricia . 288 (6): 1405-11. doi : 10.1007 / s00404-013-2855-3 . PMID 23708322 . S2CID 45611717 .
- ↑ Kamenov, Z .; et al. (2015). "Inducción de la ovulación con myo -inositol solo y en combinación con citrato de clomifeno en pacientes con síndrome de ovario poliquístico con resistencia a la insulina". Endocrinología Ginecológica . 31 (2): 131–5. doi : 10.3109 / 09513590.2014.964640 . PMID 25259724 . S2CID 24469378 .
- ^ González, F. (2012). "Inflamación en el síndrome de ovario poliquístico: sustento de la resistencia a la insulina y la disfunción ovárica" . Esteroides . 77 (4): 300–5. doi : 10.1016 / j.steroids.2011.12.003 . PMC 3309040 . PMID 22178787 .
- ↑ Monastra, G .; et al. (2018). " Efecto de la alfa- lactoalbúmina sobre la absorción intestinal de mio -inositol: in vivo e in vitro". Entrega actual de medicamentos . 15 (9): 1305-1311. doi : 10.2174 / 1567201815666180509102641 . PMID 29745333 .
- ^ Oliva, MM; et al. (2018). "Efectos de myo -inositol más alfa- lactoalbúmina en mujeres con SOP resistente a mio -inositol" . Revista de investigación ovárica . 11 (1): 38. doi : 10.1186 / s13048-018-0411-2 . PMC 5944130 . PMID 29747700 .
- ^ Nassar M, Nassar R, Maki H, Al-Yagoob A, Hachim M, Senok A, Williams D, Hiraishi N (marzo de 2021). "Ácido fítico: propiedades y posibles aplicaciones en odontología" . Fronteras en los materiales . 8 : 29. Bibcode : 2021FrMat ... 8 ... 29N . doi : 10.3389 / fmats.2021.638909 .
- ^ "Inositol, guía nerviosa, fabricante de agente de corte" . Aditivo para piensos Tianyu. Archivado desde el original el 8 de septiembre de 2014 . Consultado el 21 de julio de 2013 .
- ↑ Golianopoulos, T. (12 de mayo de 2012). "Drogas dobles: lo que los actores realmente fumar, fumar y esnifar frente a la cámara" . Cableado . Archivado desde el original el 14 de mayo de 2012 . Consultado el 14 de mayo de 2012 .
- ↑ a b Awuchi, Chinaza (2017). "Alcoholes de azúcar: química, producción, problemas de salud e importancia nutricional del manitol, sorbitol, xilitol y eritritol" . Revista Internacional de Investigación Académica Avanzada . 5 (11): 1954-1967.
- ↑ Borgi MA, Boudebbouze S, Mkaouar H, Maguin E, Rhimi M (2015). "Fitasas de Bacillus: estado actual y perspectivas de futuro" . Bioingeniería . 5 (4): 233-236. doi : 10.1080 / 21655979.2015.1048050 . PMC 4601277 . PMID 25946551 .
- ^ Stentz R, Osborne S, Horn N, Li AW, Hautefort I, Bongaerts R, Rouyer M, Bailey P, Shears SB, Hemmings AM, Brearley CA, Carding SR (27 de febrero de 2014). "Un homólogo bacteriano de una enzima de señalización de fosfato de inositol eucariota media el diálogo entre reinos en el intestino de los mamíferos" . Informes de celda . 6 (4): 646–656. doi : 10.1016 / j.celrep.2014.01.021 . PMC 3969271 . PMID 24529702 .
- ^ Ehlers, Anke; Marakis, Georgios; Lampen, Alfonso; Hirsch-Ernst, Karen Ildico (1 de agosto de 2019). "Evaluación de riesgos de bebidas energéticas con enfoque en parámetros cardiovasculares y consumo de bebidas energéticas en Europa" . Toxicología alimentaria y química . 130 : 109-121. doi : 10.1016 / j.fct.2019.05.028 . ISSN 0278-6915 . PMID 31112702 .
- ^ DiSalvo, David. "Sabemos sobre la cafeína en las bebidas energéticas como Monster, pero ¿qué pasa con los otros ingredientes?" . Forbes . Consultado el 22 de diciembre de 2020 .
- ^ "Ingredientes de bebidas energéticas y lo que hacen" . www.caffeineinformer.com . Consultado el 22 de diciembre de 2020 .
enlaces externos
| Wikimedia Commons tiene medios relacionados con el inositol . |
- Biblioteca Nacional de Medicina de EE. UU .: Portal de información sobre medicamentos - Inositol
- Espectro de inositol MS
- Inositol unido a proteínas en el AP
- Desorden obsesivo compulsivo
- Inositol
- Biología del trastorno bipolar
- Biología del trastorno obsesivo compulsivo
- Agentes quimiopreventivos
- Tratamiento del trastorno obsesivo compulsivo
- Inhibidores de la xantina oxidasa
