ATPasa
| Adenosina trifosfatasa | ||||||||
|---|---|---|---|---|---|---|---|---|
| Identificadores | ||||||||
| CE no. | 3.6.1.3 | |||||||
| No CAS. | 9000-83-3 | |||||||
| Bases de datos | ||||||||
| IntEnz | Vista IntEnz | |||||||
| BRENDA | Entrada BRENDA | |||||||
| FÁCIL | NiceZyme vista | |||||||
| KEGG | Entrada KEGG | |||||||
| MetaCyc | camino metabólico | |||||||
| PRIAM | perfil | |||||||
| Estructuras PDB | RCSB PDB PDBe PDBsum | |||||||
| ||||||||
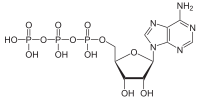
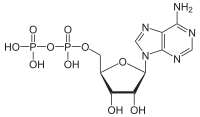
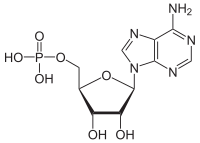
ATPasas ( CE 3.6.1.3 , A denosine 5'- T ri P hosphat ase , adenylpyrophosphatase, ATP monofosfatasa, trifosfatasa, antígeno T de SV40, hidrolasa de ATP, V complejo (transporte de electrones mitocondrial), (Ca 2 + + Mg 2+ ) -ATPasa, HCO 3 - -ATPasa, adenosina trifosfatasa) son una clase de enzimas que catalizan la descomposición de ATP en ADP y un ion fosfato libre [1] [2] [3] [4] [5] [6]o la reacción inversa. Esta reacción de desfosforilación libera energía , que la enzima (en la mayoría de los casos) aprovecha para impulsar otras reacciones químicas que de otro modo no ocurrirían. Este proceso se usa ampliamente en todas las formas de vida conocidas .
Algunas de estas enzimas son proteínas de membrana integrales (ancladas dentro de membranas biológicas ) y mueven solutos a través de la membrana, típicamente contra su gradiente de concentración. Estos se denominan ATPasas transmembrana.
Funciones
Las ATPasas transmembrana importan metabolitos necesarios para el metabolismo celular y exportan toxinas, desechos y solutos que pueden obstaculizar los procesos celulares. Un ejemplo importante es el intercambiador de sodio-potasio (o Na + / K + ATPasa ) que mantiene el potencial de la membrana celular . Y otro ejemplo es la ATPasa de hidrógeno y potasio (H + / K + ATPasa o bomba de protones gástrica) que acidifica el contenido del estómago. La ATPasa se conserva genéticamente en animales; por lo tanto, los cardenólidos, que son esteroides tóxicos producidos por plantas que actúan sobre las ATPasas, producen toxinas animales generales y eficaces que actúan de forma dependiente de la dosis. [7]
Además de los intercambiadores, otras categorías de ATPasa transmembrana incluyen cotransportadores y bombas (sin embargo, algunos intercambiadores también son bombas). Algunos de estos, como el Na + / K + ATPasa, provocan un flujo neto de carga, pero otros no. Estos se denominan transportadores "electrogénicos" y "no electrogénicos", respectivamente.
Estructura
Los motivos de Walker son un motivo de secuencia de proteínas revelador para la unión e hidrólisis de nucleótidos. Más allá de esta amplia función, los motivos de Walker se pueden encontrar en casi todas las ATPasas naturales, con la notable excepción de las tirosina quinasas . [8] Los motivos de Walker comúnmente forman una hoja Beta -vuelta- Hélice alfa que se autoorganiza como un Nido (motivo estructural de proteínas) . Se cree que esto se debe a que las ATPasas modernas evolucionaron a partir de pequeños péptidos de unión a NTP que tenían que autoorganizarse. [9]
El diseño de proteínas ha sido capaz de replicar la función de ATPasa (débilmente) sin utilizar secuencias o estructuras de ATPasa naturales. Es importante destacar que, si bien todas las ATPasas naturales tienen alguna estructura de hoja beta, la "ATPasa alternativa" diseñada carece de estructura de hoja beta, lo que demuestra que esta función esencial para la vida es posible con secuencias y estructuras que no se encuentran en la naturaleza. [10]
Mecanismo
El acoplamiento entre la hidrólisis y el transporte de ATP es más o menos una reacción química estricta, en la que se transporta un número fijo de moléculas de soluto por cada molécula de ATP que se hidroliza; por ejemplo, 3 iones Na + fuera de la célula y 2 iones K + hacia adentro por ATP hidrolizado, para el intercambiador Na + / K + .
Las ATPasas transmembrana aprovechan la energía potencial química del ATP porque realizan un trabajo mecánico : transportan solutos en una dirección opuesta a su dirección de movimiento preferida termodinámicamente , es decir, desde el lado de la membrana donde se encuentran en baja concentración hasta el lado donde están en alta concentración. Este proceso se considera transporte activo .
Por ejemplo, el bloqueo de las H + -ATPasas vesiculares aumentaría el pH dentro de las vesículas y disminuiría el pH del citoplasma.
ATP sintasas transmembrana
La ATP sintasa de las mitocondrias y los cloroplastos es una enzima anabólica que aprovecha la energía de un gradiente de protones transmembrana como fuente de energía para agregar un grupo fosfato inorgánico a una molécula de difosfato de adenosina (ADP) para formar una molécula de trifosfato de adenosina (ATP).
Esta enzima funciona cuando un protón desciende por el gradiente de concentración, lo que le da a la enzima un movimiento giratorio. Este movimiento giratorio único une ADP y P para crear ATP.
La ATP sintasa también puede funcionar a la inversa, es decir, utilizar la energía liberada por la hidrólisis de ATP para bombear protones contra su gradiente electroquímico.
Clasificación
Existen diferentes tipos de ATPasas, que pueden diferir en función (síntesis y / o hidrólisis de ATP), estructura (F-, V- y A-ATPasas contienen motores rotativos) y en el tipo de iones que transportan.
- ATPasas rotativas [11] [12]
- Las F-ATPasas (F1FO-ATPasas) en las mitocondrias , los cloroplastos y las membranas plasmáticas bacterianas son los principales productores de ATP, utilizando el gradiente de protones generado por la fosforilación oxidativa (mitocondrias) o la fotosíntesis (cloroplastos).
- Las F-ATPasas que carecen de una subunidad delta / OSCP mueven los iones de sodio en su lugar. Se propone que se llamen N-ATPasas , ya que parecen formar un grupo distinto que está más alejado de las F-ATPasas habituales que las A-ATPasas de las V-ATPasas. [13]
- Las V-ATPasas (V1VO-ATPasas) se encuentran principalmente en vacuolas eucariotas, catalizando la hidrólisis de ATP para transportar solutos y bajar el pH en orgánulos como la bomba de protones del lisosoma.
- Las A-ATPasas (A1AO-ATPasas) se encuentran en Archaea y algunas bacterias extremófilas. Están organizados como V-ATPasas, pero funcionan como F-ATPasas principalmente como ATP sintasas.
- Existen muchos homólogos que no son necesariamente rotativos. Ver ATP sintasa § Evolución .
- Las F-ATPasas (F1FO-ATPasas) en las mitocondrias , los cloroplastos y las membranas plasmáticas bacterianas son los principales productores de ATP, utilizando el gradiente de protones generado por la fosforilación oxidativa (mitocondrias) o la fotosíntesis (cloroplastos).
- Las P-ATPasas (E1E2-ATPasas) se encuentran en bacterias, hongos y en membranas plasmáticas eucariotas y orgánulos, y funcionan para transportar una variedad de iones diferentes a través de las membranas.
- Las E-ATPasas son enzimas de la superficie celular que hidrolizan una variedad de NTP, incluido el ATP extracelular. Los ejemplos incluyen ecto-ATPasas, CD39 y ecto-ATP / Dases, todos los cuales son miembros de una superfamilia " GDA1 CD39 ". [14]
- Las proteínas AAA son una familia de NTPasas de bucle P en forma de anillo .
P-ATPasa
Las P-ATPasas (algunas veces conocidas como ATPasas E1-E2) se encuentran en bacterias y también en membranas plasmáticas eucariotas y orgánulos. Su nombre se debe a que el fosfato inorgánico se adhiere por poco tiempo a los residuos de aspartato en el momento de la activación. La función de la P-ATPasa es transportar una variedad de compuestos diferentes, como iones y fosfolípidos, a través de una membrana utilizando la hidrólisis de ATP para obtener energía. Hay muchas clases diferentes de P-ATPasas, que transportan un tipo específico de ion. Las P-ATPasas pueden estar compuestas por uno o dos polipéptidos y normalmente pueden adoptar dos conformaciones principales, E1 y E2.
Genes humanos
- Transporte de Na + / K + : ATP1A1 , ATP1A2 , ATP1A3 , ATP1A4 , ATP1B1 , ATP1B2 , ATP1B3 , ATP1B4
- Transporte de Ca ++ : ATP2A1 , ATP2A2 , ATP2A3 , ATP2B1 , ATP2B2 , ATP2B3 , ATP2B4 , ATP2C1 , ATP2C2
- Transporte de Mg ++ : ATP3
- Intercambio H + / K + : ATP4A
- H + transporte, mitocondrial : ATP5A1 , ATP5B , ATP5C1 , ATP5C2 , ATP5D , ATP5E , ATP5F1 , ATP5G1 , ATP5G2 , ATP5G3 , ATP5H , ATP5I , ATP5J , ATP5J2 , ATP5L , ATP5L2 , ATP5O , ATP5S
- H + transporte, lisosomal : ATP6AP1 , ATP6AP2 , ATP6V1A , ATP6V1B1 , ATP6V1B2 , ATP6V1C1 , ATP6V1C2 , ATP6V1D , ATP6V1E1 , ATP6V1E2 , ATP6V1F , ATP6V1G1 , ATP6V1G2 , ATP6V1G3 , ATP6V1H , ATP6V0A1 , ATP6V0A2 , ATP6V0A4 , ATP6V0B , ATP6V0C , ATP6V0D1 , ATP6V0D2, ATP6V0E
- Transporte de Cu ++ : ATP7A , ATP7B
- Clase I, tipo 8: ATP8A1 , ATP8B1 , ATP8B2 , ATP8B3 , ATP8B4
- Clase II, tipo 9: ATP9A , ATP9B
- Clase V, tipo 10: ATP10A , ATP10B , ATP10D
- Clase VI, tipo 11: ATP11A , ATP11B , ATP11C
- Transporte de H + / K + , no gástrico: ATP12A
- tipo 13: ATP13A1 , ATP13A2 , ATP13A3 , ATP13A4 , ATP13A5
Ver también
- ATP sintasa
- Subunidades alfa / beta de ATP sintasa
- Proteínas AAA
- P-ATPasa
Referencias
- ^ Geider K, Hoffmann-Berling H (1981). "Proteínas que controlan la estructura helicoidal del ADN". Revisión anual de bioquímica . 50 : 233–60. doi : 10.1146 / annurev.bi.50.070181.001313 . PMID 6267987 .
- ^ Kielley WW (1961). "Miosina adenosina trifosfatasa". En Boyer PD, Lardy H, Myrbäck K (eds.). Las enzimas . 5 (2ª ed.). Nueva York: Academic Press. págs. 159-168.
- ^ Martin SS, Senior AE (noviembre de 1980). "Actividades de la adenosina trifosfatasa de membrana en el páncreas de rata". Biochimica et Biophysica Acta (BBA) - Biomembranas . 602 (2): 401–18. doi : 10.1016 / 0005-2736 (80) 90320-x . PMID 6252965 .
- ^ Njus D, Knoth J, Zallakian M (1981). "Transporte ligado a protones en gránulos de cromafina". Temas de actualidad en bioenergética . 11 : 107-147. doi : 10.1016 / B978-0-12-152511-8.50010-4 .
- ^ Riley MV, Peters MI (junio de 1981). "La localización de la actividad ATPasa sensible a aniones en el endotelio corneal". Biochimica et Biophysica Acta (BBA) - Biomembranas . 644 (2): 251–6. doi : 10.1016 / 0005-2736 (81) 90382-5 . PMID 6114746 .
- ^ Tjian R (1981). "Regulación de la transcripción viral y la replicación del ADN por el antígeno T grande de SV40". Temas de actualidad en microbiología e inmunología . 93 : 5-24. doi : 10.1007 / 978-3-642-68123-3_2 . ISBN 978-3-642-68125-7. PMID 6269805 .
- ^ Dobler S, Dalla S, Wagschal V, Agrawal AA (agosto de 2012). "Evolución convergente de toda la comunidad en la adaptación de insectos a cardenólidos tóxicos por sustituciones en la Na, K-ATPasa" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 109 (32): 13040–5. doi : 10.1073 / pnas.1202111109 . PMC 3420205 . PMID 22826239 .
- ^ Walker JE, Saraste M, Runswick MJ, Gay Nueva Jersey (1982). "Secuencias distantemente relacionadas en las subunidades alfa y beta de ATP sintasa, miosina, quinasas y otras enzimas que requieren ATP y un pliegue de unión de nucleótidos común" . EMBO J . 1 (8): 945–51. doi : 10.1002 / j.1460-2075.1982.tb01276.x . PMC 553140 . PMID 6329717 .
- ^ Romero Romero ML, Yang F, Lin YR, Toth-Petroczy A, Berezovsky IN, Goncearenco A, et al. (Diciembre de 2018). "Proteínas de bucle de fosfato simples pero funcionales" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 115 (51): E11943 – E11950. doi : 10.1073 / pnas.1812400115 . PMC 6304952 . PMID 30504143 .
- ^ Wang M, Hecht MH (agosto de 2020). "Una ATPasa completamente de novo de diseño de proteína combinatoria". Revista de la Sociedad Química Estadounidense . 142 (36): 15230-15234. doi : 10.1021 / jacs.0c02954 . PMID 32833456 .
- ^ Stewart AG, Laming EM, Sobti M, Stock D (abril de 2014). "ATPasas rotativas - máquinas moleculares dinámicas" . Opinión actual en biología estructural . 25 : 40–8. doi : 10.1016 / j.sbi.2013.11.013 . PMID 24878343 .
- ^ Kühlbrandt W, Davies KM (enero de 2016). "ATPasas rotativas: un nuevo giro a una máquina antigua". Tendencias en Ciencias Bioquímicas . 41 (1): 106-116. doi : 10.1016 / j.tibs.2015.10.006 . PMID 26671611 .
- ^ Dibrova, DV; Galperin, MI; Mulkidjanian, AY (15 de junio de 2010). "Caracterización de la N-ATPasa, una forma distinta de translocación de Na + transferida lateralmente de la ATPasa de membrana de tipo F bacteriana" . Bioinformática . 26 (12): 1473–6. doi : 10.1093 / bioinformatics / btq234 . PMC 2881411 . PMID 20472544 .
- ^ Knowles, AF (marzo de 2011). "La superfamilia GDA1_CD39: NTPDases con diversas funciones" . Señalización purinérgica . 7 (1): 21–45. doi : 10.1007 / s11302-010-9214-7 . PMC 3083126 . PMID 21484095 .
enlaces externos
| Wikimedia Commons tiene medios relacionados con adenosina trifosfatasas . |
- "ATP sintasa: una espléndida máquina molecular"
- ATPase en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- Estructuras de microscopía electrónica de ATPasas del EM Data Bank (EMDB)
- EC 3.6.1
- EC 3.6.3
- Proteínas integrales de membrana