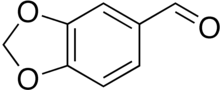
Piperonal
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido 2 H -1,3-benzodioxol-5-carbaldehído | |
| Otros nombres Heliotropina; Heliotropina; Aldehído de piperonilo; Aldehído metilen éter protocatechico; 3,4-metilendioxibenzaldehído; | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| 131691 | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.004.009 |
| Número CE |
|
| 4186 | |
| KEGG | |
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 8 H 6 O 3 | |
| Masa molar | 150,133 g · mol −1 |
| Apariencia | Cristales incoloros [1] |
| Densidad | 1,337 g / cm 3 |
| Punto de fusion | 37 ° C (99 ° F; 310 K) [1] |
| Punto de ebullición | 263 ° C (505 ° F; 536 K) [1] |
| Soluble en 500 partes [1] | |
| Riesgos | |
| Pictogramas GHS |  |
| Palabra de señal GHS | Advertencia |
| H317 | |
| P261 , P272 , P280 , P302 + 352 , P321 , P333 + 313 , P363 , P501 | |
| Dosis o concentración letal (LD, LC): | |
LD 50 ( dosis media ) | 2700 mg / kg (por vía oral en ratas) [1] |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
Piperonal , también conocido como heliotropina , es un compuesto orgánico que se encuentra comúnmente en fragancias y sabores. [2] La molécula está relacionada estructuralmente con otros aldehídos aromáticos como el benzaldehído y la vainillina .
Ocurrencia natural
Piperonal se encuentra naturalmente en varias plantas. Los ejemplos incluyen eneldo , vainilla , flores violetas y pimienta negra .
Preparación
El piperonal se puede preparar mediante la escisión oxidativa de isosafrol o utilizando una secuencia de múltiples pasos de catecol o 1,2-metilendioxibenceno . La síntesis de la última sustancia química se logra mediante una reacción de condensación con ácido glioxílico seguida de la escisión del α-hidroxiácido resultante con un agente oxidante . [2] [3] [4] La síntesis a partir de catecol requiere un paso adicional, la síntesis del éter Williamson usando diclorometano . [5]
Reacciones
El piperonal, como todos los aldehídos , puede reducirse a su alcohol (alcohol piperonílico) u oxidarse para dar su ácido (ácido piperonílico).
Piperonal se puede utilizar en la síntesis de algunos fármacos, incluidos tadalafil , [6] L-DOPA , [7] y atrasentan . [8]
Fragancia
Piperonal tiene un olor floral que se describe comúnmente como similar al de la vainillina o la cereza . Por esta razón, se usa comúnmente en fragancias y sabores artificiales . [2] El compuesto se llamó Heliotropin por las notas de "pastel de cereza" que se encuentran en la fragancia de la flor de heliotropo (aunque el químico no está presente en el verdadero aroma de la flor). [9] Los perfumistas comenzaron a usar la fragancia por primera vez a principios de la década de 1880. [10] Se usa comúnmente para agregar matices de vainilla o almendra, generalmente impartiendo aspectos balsámicos, polvorientos y florales al carácter de una fragancia. [11]
El acetato de piperonilo es un aromatizante de cereza sintético. [12]
Referencias
- ^ a b c d e Budavari, Susan, ed. (1996), The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (12a ed.), Merck, ISBN 0911910123
- ^ a b c Karl-Georg Fahlbusch, Franz-Josef Hammerschmidt, Johannes Panten, Wilhelm Pickenhagen, Dietmar Schatkowski, Kurt Bauer, Dorothea Garbe y Horst Surburg "Sabores y fragancias" en la Enciclopedia de química industrial de Ullmann, Wiley-VCH, Weinheim, 2003 . doi : 10.1002 / 14356007.a11_141
- ^ Fatiadi, Alexander y Schaffer, Robert (1974). "Un procedimiento mejorado para la síntesis de ácido DL-4-hidroxi-3-metoximandélico (DL-" Vanillyl "-ácido mandélico, VMA)" . Revista de Investigación de la Oficina Nacional de Normalización Sección A . 78A (3): 411–412. doi : 10.6028 / jres.078A.024 .
- ^ Nwaukwa, Stephen; Keehn, Philip (1982). "Escisión oxidativa de α-dioles, α-dionas, α-hidroxi-cetonas y α-hidroxi y α-cetoácidos con hipoclorito de calcio [Ca (OCl) 2 ]”. Letras de tetraedro . 23 (31): 3135–3138. doi : 10.1016 / S0040-4039 (00) 88578-0 .
- ^ Bonthrone, W. y Cornforth, J. (1969). "La metilenación de los catecoles". Revista de la Sociedad Química (9): 1202–1204. doi : 10.1039 / J39690001202 .
- ^ Gilla, G .; Anumula, RR; Aalla, S .; Vurimidi, H. y Ghanta, MR (2013). "Síntesis y caracterización de sustancias relacionadas y metabolito de tadalafil, un inhibidor de PDE-5" (PDF) . Comunicaciones orgánicas . 6 (1): 12-22.
- ^ Yamada, Shun-Ichi; Fujii, Tozo; Shioiri, Takayuki (1962). "Estudios sobre aminoácidos ópticamente activos. I. Preparación de 3- (3,4-Metilendioxifenil) -D- y -L-alanina" . Boletín químico y farmacéutico . 10 (8): 680. doi : 10.1248 / cpb.10.680 .
- ^ Winn, Martin; von Geldern, Thomas W .; Opgenorth, Terry J .; Jae, Hwan-Soo; Tasker, Andrew S .; Boyd, Steven A .; Kester, Jeffrey A .; Mantei, Robert A .; Bal, Radhika; Sorensen, Bryan K .; Wu-Wong, Jinshyun R .; Chiou, William J .; Dixon, Douglas B .; Novosad, Eugene I .; Hernández, Lisa; Marsh, Kennan C. (1996). "Ácidos 2,4-diarilpirrolidina-3-carboxílicos potentes antagonistas del receptor de endotelina selectivo ETAS. 1. Descubrimiento de A-127722". Revista de química medicinal . 39 (5): 1039–1048. doi : 10.1021 / jm9505369 . ISSN 0022-2623 .
- ^ http://www.bojensen.net/EssentialOilsEng/EssentialOils13A/EssentialOils13A.htm
- ^ La fuerza de la moda en la política y la sociedad : perspectivas globales desde la Edad Moderna hasta la época contemporánea Por Beverly Lemire ISBN 9781409404927
- ^ La entrada de la base de datos de Good Scents Company para Heliotropin
- ^ Manual de ingredientes de sabor de Fenaroli.
enlaces externos
| Wikisource tiene el texto del artículo Piperonal de la Encyclopædia Britannica de 1911 . |
- Benzaldehídos
- Benzodioxol