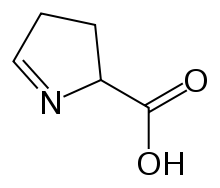
Ácido 1-pirrolin-5-carboxílico
Este artículo necesita citas adicionales para su verificación . ( enero de 2021 ) |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido Ácido 3,4-dihidro- 2H -pirrol-2-carboxílico | |
| Otros nombres Ácido 1-pirrolina-5-carboxílico Ácido δ-1-pirrolina-5-carboxílico P5C | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| KEGG | |
| Malla | Delta-1-pirrolina-5-carboxilato |
PubChem CID | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 5 H 7 NO 2 | |
| Masa molar | 113,115 g / mol |
| Acidez (p K a ) | 1,82 / 6,07 [1] |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El ácido 1-pirrolina-5-carboxílico (nombre sistemático ácido 3,4-dihidro-2H-pirrol-2-carboxílico [2] ) es un iminoácido cíclico . Su base conjugada y anión es 1-pirrolina-5-carboxilato (P5C). En solución, P5C está en equilibrio espontáneo con glutamato-5-semialdhído (GSA). [3] El estereoisómero ( S ) -1-pirrolina-5-carboxilato (también denominado L-P5C) es un metabolito intermedio en la biosíntesis y degradación de prolina y arginina . [4] [5] [6]
En la biosíntesis de prolina procariota , la enzima γ-glutamil fosfato reductasa sintetiza GSA a partir de γ-glutamil fosfato . En la mayoría de los eucariotas , la GSA se sintetiza a partir del aminoácido glutamato mediante la enzima bifuncional 1-pirrolina-5-carboxilato sintasa (P5CS). La P5CS humana está codificada por el gen ALDH18A1 . [7] [8] La enzima pirrolina-5-carboxilato reductasa convierte la P5C en prolina
En la degradación de la prolina, la enzima prolina deshidrogenasa produce P5C a partir de prolina y la enzima 1-pirrolina-5-carboxilato deshidrogenasa convierte GSA en glutamato. En muchos procariotas, la prolina deshidrogenasa y la P5C deshidrogenasa forman una enzima bifuncional que evita la liberación de P5C durante la degradación de la prolina. [9] En la degradación de la arginina, la enzima ornitina-δ-aminotransferasa media la transaminación entre ornitina y un 2-oxoácido (típicamente α-cetoglutarato) para formar P5C y un L-aminoácido (típicamente glutamato). En condiciones específicas, P5C también se puede usar para la biosíntesis de arginina mediante la reacción inversa de la ornitina-δ-aminotransferasa. [4]
Referencias
- ^ "calculado por Chemicalize de ChemAxon" .
- ^ PubChem. "Ácido 3,4-dihidro-2H-pirrol-2-carboxílico" . pubchem.ncbi.nlm.nih.gov . Consultado el 23 de enero de 2020 .
- ↑ Heacock, Anne M .; Williams, Irene H .; Frank, Leonard H .; Adams, Elijah (1 de abril de 1975). "Δ1-pirrolina-5-carboxilato y Δ1-pirrolina-3-hidroxi-5-carboxilato: cromatografía en el analizador de aminoácidos". Bioquímica analítica . 64 (2): 593–600. doi : 10.1016 / 0003-2697 (75) 90472-8 . ISSN 0003-2697 . PMID 236687 .
- ↑ a b Bertolo, Robert F .; Burrin, Douglas G. (1 de octubre de 2008). "Aspectos comparativos del metabolismo de la glutamina y la prolina tisular" . La Revista de Nutrición . 138 (10): 2032S – 2039S. doi : 10.1093 / jn / 138.10.2032S . ISSN 0022-3166 . PMID 18806120 .
- ^ Qamar, Aarzoo; Mysore, Kirankumar; Senthil-Kumar, Muthappa (2015). "Papel del metabolismo de prolina y pirrolina-5-carboxilato en la defensa de las plantas contra patógenos invasores" . Fronteras en la ciencia de las plantas . 6 . doi : 10.3389 / fpls.2015.00503 . ISSN 1664-462X . PMID 26217357 .
- ^ Invierno, Gudrun; Todd, Christopher D .; Trovato, Maurizio; Forlani, Giuseppe; Funck, Dietmar (2015). "Implicaciones fisiológicas del metabolismo de la arginina en plantas" . Fronteras en la ciencia de las plantas . 6 : 534. doi : 10.3389 / fpls.2015.00534 . ISSN 1664-462X . PMC 4520006 . PMID 26284079 .
- ^ Liu G, Maunoury C, Kamoun P, Aral B (octubre de 1996). "Asignación del gen humano que codifica la delta 1-pirrolina-5-carboxilato sintetasa (P5CS) a 10q24.3 mediante hibridación in situ". Genómica . 37 (1): 145–6. doi : 10.1006 / geno.1996.0535 . PMID 8921385 .
- ^ "Gen Entrez: familia de aldehído deshidrogenasa 18 ALDH18A1, miembro A1" .
- ^ Liu, Li-Kai; Becker, Donald F .; Tanner, John J. (15 de octubre de 2017). "Estructura, función y mecanismo de utilización de prolina A (PutA)" . Archivos de Bioquímica y Biofísica . Flavoproteínas: más allá de los paradigmas clásicos. 632 : 142-157. doi : 10.1016 / j.abb.2017.07.005 . ISSN 0003-9861 . PMC 5650515 . PMID 28712849 .
- Pirrolinas
- Ácidos carboxílicos
- Talones de bioquímica