Etóxido de titanio
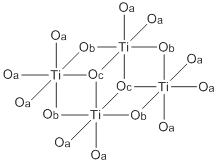 Estructura abreviada del etóxido de titanio (IV). Los ligandos de etóxido están representados por O's. Los ligandos de etóxido terminales se designan por Oa, los ligandos de doble puente por Ob y los ligandos de triple puente por Oc. | |
| Nombres | |
|---|---|
| Nombre IUPAC etanolato; titanio (4+) | |
| Nombre IUPAC sistemático tetraetanolato de titanio (4+) | |
| Otros nombres Titanato de etilo, titanato de tetraetilo | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.019.464 |
| Número CE |
|
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 32 H 80 O 16 Ti 4 | |
| Masa molar | 228,109 g / mol |
| Apariencia | líquido incoloro |
| Densidad | 1.088 |
| Punto de ebullición | 150-152 (a 10 mmHg) |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El etóxido de titanio es un compuesto químico con la fórmula Ti 4 (OCH 2 CH 3 ) 16 . Es un líquido incoloro que es soluble en disolventes orgánicos pero que se hidroliza fácilmente. Se vende comercialmente como solución incolora. Los alcóxidos de titanio (IV) y circonio (IV) se utilizan en síntesis orgánica y ciencia de materiales . Adoptan estructuras más complejas que las sugeridas por sus fórmulas empíricas. [1]
Síntesis
El etóxido de titanio se prepara tratando tetracloruro de titanio con etanol en presencia de una amina: [2]
- TiCl 4 + 4 EtOH + 4 Et 3 N → Ti (OEt) 4 + 4 Et 3 NHCl
La pureza del etóxido de titanio se evalúa habitualmente mediante espectroscopia de RMN de protón . Ti (OEt) 4 RMN 1H (90 MHz, cloroformo-d, ppm): 4,36 (cuarteto, 8H, CH 2 ), 1,27 (triplete, 12H, CH 3 ). [3]
Estructura
Ambos Ti (OEt) 4 existen principalmente como tetrámeros con un entorno de coordinación octaédrico alrededor de los centros metálicos. Hay dos tipos de centros de titanio, dependiendo del número de ligandos de alcóxido terminales y de puente. Zr (OEt) 4 es estructuralmente similar. [2] [4] La simetría virtual de la estructura del núcleo de M 4 O 16 para las estructuras del tetrámero de estos compuestos es C 2h . [5]
Compuestos relacionados
Metóxido de titanio
Al igual que el etóxido, el metóxido de titanio Ti (OMe) 4 existe como un tetrámero, teniendo cada uno de los centros de metal de Ti IV un entorno de coordinación octaédrico. [6]
Isopropóxido de titanio
Con grupos alquilo voluminosos, Ti (O i Pr) 4, en contraste, existe como un monómero con un entorno tetraédrico alrededor del centro de Ti. Este menor grado de coordinación con el centro del metal se atribuye a la masa estérica de los grupos i Pr frente a los grupos n -alquilo, esto sirve para evitar las interacciones puente entre los centros del metal. [7]
Etóxido de circonio
El etóxido de circonio se puede preparar de una manera similar pero no idéntica al compuesto de titanio: [8]
- ZrCl 4 + 5 NaOEt + EtOH → NaH [Zr (OEt) 6 ] + 4 NaCl
- NaH [Zr (OEt) 6 ] + HCl → Zr (OEt) 4 + NaCl + 2 EtOH
Una síntesis más común del etóxido de circonio es tratar el tetracloruro de circonio con el alcohol y el amoníaco deseados: [8]
- ZrCl 4 + 4 ROH + 4 NH 3 → Zr (OR) 4 + 4 NH 4 Cl
El etóxido de circonio también se puede preparar con dicloruro de circonoceno: [9]
- Cp 2 ZrCl 2 + 4 EtOH + 2 Et 3 N → 2 CpH + 2 Et 3 NHCl + Zr (OEt) 4
Propóxido de circonio
Zr (O n Pr) 4 también adopta la estructura de etóxido de titanio. [4] [5]
Reacciones
Tanto los alcóxidos de Ti como los de Zr se pueden utilizar para depositar películas microestructuradas de TiO 2 o ZrO 2 :
- M (OEt) 4 + 2 H 2 O → MO 2 + 4 EtOH
Estas películas se forman por hidrólisis del alcóxido. Los óxidos resultantes son químicamente resilientes. [10] La estructura de las películas de óxido metálico que crecen en esta materia se ve afectada por la presencia de catalizadores básicos o ácidos para la hidrólisis. Generalmente, la catálisis ácida produce un sol en el que las cadenas de polímero están orientadas aleatoriamente y son lineales. En el caso de que se produzcan agrupaciones tupidas o redes reticuladas mediadas por bases, estas estructuras pueden atrapar solventes y subproductos de reacción y formar un recubrimiento de gel. [11] Los alcóxidos de Ti IV y Zr IV también son materiales de partida potenciales para los catalizadores de Ziegler-Natta utilizados en la polimerización de alquenos . [10]Se han cristalizado intermedios en la hidrólisis. Cuentan con óxidos interiores además del etóxido en el exterior de los racimos. [12]
Referencias
- ^ Ram C. Mehrotra ; Singh, Anirudh (1997). "Tendencias recientes en la química de los alcóxidos metálicos" . En Kenneth D. Karlin (ed.). Progreso en Química Inorgánica . 46 . John Wiley e hijos . págs. 239–454. doi : 10.1002 / 9780470166475.ch4 . ISBN 9780470167045.
- ^ a b F. Albert Cotton ; Geoffrey Wilkinson ; Murillo, C .; Bochmann, M. (1999). Química Inorgánica Avanzada (6ª ed.). Nueva York: John Wiley & Sons . ISBN 978-0-471-19957-1.
- ^ Sistema de base de datos espectral integrado de compuestos orgánicos, versión 2011. AIST: Japón, 2011 (consultado el 3 de octubre de 2011).
- ↑ a b James A. Ibers (1963). "Cristal y estructura molecular del etóxido de titanio (IV)". Naturaleza . 197 (4868): 686–687. Código Bibliográfico : 1963Natur.197..686I . doi : 10.1038 / 197686a0 . S2CID 4297907 .
- ^ a b Día, Victor W .; Klemperer, Walter G .; Pafford, Margaret M. (2001). "Aislamiento y caracterización estructural de tetra n propil zirconato en solución de hidrocarburo y el estado sólido". Inorg. Chem. 40 (23): 5738–5746. doi : 10.1021 / ic010776g . PMID 11681880 .
- ^ Wright, DA; Williams, DA (1968). "El cristal y la estructura molecular del tetrametóxido de titanio" . Acta Crystallographica B . 24 (8): 1107-1114. doi : 10.1107 / S0567740868003766 .
- ^ Ghosh, Rajshekhar; Nethaji, Munirathinam; Samuelson, Ashoka G. (2005). "Doble inserción reversible de isocianatos de arilo en el enlace Ti-O del isopropóxido de titanio (IV)". J. Organomet. Chem. 690 (5): 1282-1293. doi : 10.1016 / j.jorganchem.2004.11.038 .
- ^ a b Bradley, DC ; Wardlaw, W. (1951). "Alcóxidos de circonio". J. Chem. Soc. : 280–285. doi : 10.1039 / jr9510000280 .
- ^ Gray, Donald R .; Brubaker, Carl H. (1971). "Preparación y caracterización de una serie de compuestos de cloroalcoxobis (ciclopentadienil) circonio (IV) y dialcoxobis (ciclopentadienil) circonio (IV)". Inorg. Chem. 10 (10): 2143–2146. doi : 10.1021 / ic50104a010 .
- ↑ a b Greenwood, Norman N .; Earnshaw, Alan (1997). Química de los Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ^ Schubert, U. (2003). "Procesamiento Sol-Gel de compuestos metálicos". En McCleverty, JA; Meyer, TJ (eds.). Química Integral de Coordinación II . Módulo de referencia en Química, Ciencias Moleculares e Ingeniería Química. 7 . Pergamon . págs. 629–656. doi : 10.1016 / B0-08-043748-6 / 06213-7 . ISBN 978-0-12-409547-2.
- ^ Coppens, Philip; Chen, Yang; Trzop, Elżbieta (2014). "Cristalografía y propiedades de los nanoclusters de polioxotitanato". Revisiones químicas . 114 (19): 9645–9661. doi : 10.1021 / cr400724e . PMID 24820889 .
- Etoxidos
- Compuestos de titanio (IV)