Tritioacetona
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido Hexametil-1,3,5-tritiano | |
| Otros nombres Tritioacetona [1] | |
| Identificadores | |
Modelo 3D ( JSmol ) | |
| 5-19-09-00119 | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.011.438 |
| Número CE |
|
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 9 H 18 S 3 | |
| Masa molar | 222,42 g · mol −1 |
| Densidad | 1.0660 a 1.0700 g / mL [2] |
| Punto de fusion | 21,8 ° C [3] |
| Punto de ebullición | 107 ° C / 10 mmHg [2] |
Índice de refracción ( n D ) | 1.5390 a 1.5430 [2] |
| Riesgos | |
| Pictogramas GHS |  |
| Palabra de señal GHS | Advertencia |
| H315 , H319 , H335 | |
| P261 , P264 , P271 , P280 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , P405 , P501 | |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
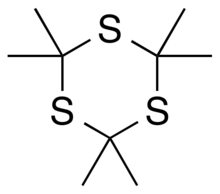
La tritioacetona ( 2,2,4,4,6,6-hexametil-1,3,5-tritiano ) es una sustancia química orgánica con fórmula C
9H
18S
3. Su estructura covalente es [–C (CH
3)
2-S-]
3, es decir, un anillo de seis miembros de átomos de carbono y azufre alternados , con dos grupos metilo unidos a cada carbono. [4] [2] Puede verse como un derivado del 1,3,5-tritiano , con sustituyentes de grupo metilo para todos los átomos de hidrógeno en esa estructura original.
El compuesto Tritioacetona es un trímero cíclico estable de tioacetona (propano-2-tiona), que en sí mismo es un compuesto inestable. [5] [6] En contraste, el compuesto análogo de trioxano , 2,2,4,4,6,6-hexametil-1,3,5-trioxano ( triacetona ), con átomos de oxígeno en lugar de átomos de azufre, parece inestable, mientras que su correspondiente monómero acetona (2-propanona) es estable.
Síntesis
La tritioacetona fue fabricada por primera vez en 1889 por Baumann y Fromm, mediante la reacción de sulfuro de hidrógeno con acetona. [6] En presencia de un ZnCl acidificado
2catalizador a 25 ° C, se obtiene un producto que es 60-70% de tritioacetona, 30-40% de 2,2-propanoditiol y pequeñas cantidades de dos impurezas isoméricas, 3,3,5,5,6,6-hexametil 1,2,4-tritiano y 4-mercapto-2,2,4,6,6-pentametil-1,3-ditiano . [6] El producto también se puede obtener mediante pirólisis de alil isopropil sulfuro . [7] [8]
Reacciones
La pirólisis de tritioacetona a 500-650 ° C y 5-20 mm de Hg da tioacetona, que puede recolectarse mediante una trampa fría a -78 ° C.
Usos
La tritioacetona se encuentra en algunos aromatizantes . Su número de FEMA es 3475. [9] [10] [11] [12]
Toxicidad
El LD 50 (oral) en ratones es 2,4 g / kg. [9] [3]
Ver también
- 2,4,6-trimetil-1,3,5-tritiano
- Hexametilciclotrisiloxano , un análogo con un anillo de silicio- oxígeno en lugar de uno de carbono-azufre.
- Hexametilciclotrisilazano , con anillo silicio- nitrógeno . [13]
- 2,2,4,4,6,6-hexametil-1,3,5-triselena-2,4,6-tristannaciclohexano , con un anillo de estaño - selenio . [14] [15]
Referencias
- ^ " Tritioacetona ". Hoja de datos químicos en línea, consultada el 1 de enero de 2020.
- ^ a b c d TCI America (2020): " Producto H1278: 2,2,4,4,6,6-Hexametil-1,3,5-tritiano ". Página del catálogo en línea, consultada el 1 de enero de 2020.
- ^ a b NCBI PubChem (2010): " 2,2,4,4,6,6-Hexametil-1,3,5-tritiano ". Hoja de datos químicos en línea, consultada el 1 de enero de 2020.
- ^ David S. Breslow , Herman Skolnik (2009): Heterociclos de cinco y seis miembros de azufre y azufre y oxígeno múltiples , parte 2; página 712. Volumen 68 de Química de compuestos heterocíclicos . ISBN 9780470188330
- ^ RD Lipscomb y WH Sharkey (1970): "Caracterización y polimerización de tioacetona". Journal of Polymer Science - Parte A: Química de polímeros , volumen 8, número 8, páginas 2187–2196. doi : 10.1002 / pol.1970.150080826
- ^ a b c William H. Sharkey (1979): "Polimerización a través del doble enlace carbono-azufre". Polimerización , serie Advances in Polymer Science , volumen 17, páginas 73-103. doi : 10.1007 / 3-540-07111-3_2
- ^ William J. Bailey y Hilda Chu (1965): "Síntesis de politioacetona". Preimpresiones de polímeros ACS , volumen 6, páginas = 145-155
- ^ Horst Bohme, Hans Pfeifer y Erich Schneider (1942): "Tiocetonas diméricas". Berichte der Deutschen Chemischen Gesellschaft , volumen 75B, número 7, páginas 900–909. doi : 10.1002 / cber.19420750722 Nota: Este primer informe confunde el trímero con el monómero.
- ^ a b E. J. Moran, OD Easterday y BL Oser (1980): "Toxicidad oral aguda de sustancias químicas de sabor seleccionadas". Toxicología farmacéutica y química , volumen 3, número 3, páginas 249-258. PMID 7449655 doi : 10.3109 / 01480548009002221
- ^ Organización Mundial de la salud (1999): " Tritioacetona ". Ficha de datos en línea de la Evaluación del Comité Mixto FAO / OMS de Expertos en Aditivos Alimentarios (JECFA) . Consultado el 2 de enero de 2020.
- ^ G. Ohloff e I. Flament (1979): "El papel de las sustancias heteroatómicas en los compuestos aromáticos de los productos alimenticios". En Fortschritte der Chemie Organischer Naturstoffe ( Progreso en la química de productos orgánicos naturales ), volumen 36, páginas 231-283. doi : 10.1007 / 978-3-7091-3265-4_2
- ^ EUR-Lex (2012): " Entrada de tabla 15.009: tritioacetona ". En el Reglamento de la UE nº 872/2012 , documento 32012R0872, Diario Oficial de la UE - Serie L , volumen 267, páginas 1–161.
- ^ Stuart D. Brewer y Charles P. Haber (1948): "Alkylsilazanes y algunos compuestos relacionados". Journal of the American Chemical Society , volumen 70, número 11, páginas 3888-3891. doi : 10.1021 / ja01191a106
- ^ BM Mikhova (2008), "Datos de RMN para carbono-13 - C6H18Se3Sn3" en Landolt-Börnstein - Materia condensada del grupo III , volumen 35 Datos de resonancia magnética nuclear , subvolumen D5, compuestos organometálicos . doi : 10.1007 / 978-3-540-74189-3_1362
- ^ Martin Dräger, Axel Blecher, Hans-Jürgen Jacobsen, Bernt Krebs (1978): "Molekül- und kristallstruktur von hexamethylcyclo-tristannaselenan [(CH
3)
2SnSe]
3". Journal of Organometallic Chemistry , volumen 161, número 3, páginas 319-325. Doi : 10.1016 / S0022-328X (00) 92243-5
- Heterociclos de azufre