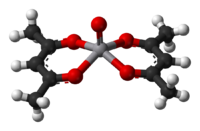
Acetilacetonatos de metales
Los acetilacetonatos de metal son complejos de coordinación derivados del anión acetilacetonato ( CH
3COCHCOCH-
3) e iones metálicos, generalmente metales de transición . El acetilacetonato de ligando bidentado a menudo se abrevia como acac. Normalmente, ambos átomos de oxígeno se unen al metal para formar un anillo de quelato de seis miembros. Los complejos más simples tienen la fórmula M (acac) 3 y M (acac) 2 . Los complejos de ligandos mixtos, por ejemplo, VO (acac) 2 , también son numerosos. También se han desarrollado variaciones de acetilacetonato con una miríada de sustituyentes en lugar de metilo (RCOCHCOR ′ - ). [1] Muchos de estos complejos son solubles en disolventes orgánicos , a diferencia de los haluros metálicos relacionados. Debido a estas propiedades, los complejos de acac a veces se utilizan como catalizador.precursores y reactivos. Las aplicaciones incluyen su uso como "reactivos de desplazamiento" de RMN y como catalizadores para síntesis orgánica , y precursores de catalizadores de hidroformilación industrial . C
5H
7O-
2en algunos casos también se une a los metales a través del átomo de carbono central; este modo de unión es más común para los metales de transición de la tercera fila como el platino (II) y el iridio (III).
La adición de base ayuda a eliminar un protón de la acetilacetona y cambia el equilibrio a favor del complejo. Ambos centros de oxígeno se unen al metal para formar un anillo de quelato de seis miembros. En algunos casos, el efecto quelato es tan fuerte que no se necesita una base adicional para formar el complejo. Algunos complejos se preparan mediante metátesis utilizando Tl (acac).
En la mayoría de sus complejos, acac forma anillos quelatos C 3 O 2 M de seis miembros . [3] El anillo de Macacc en plano con un plano de simetría que divide el anillo.
El anillo acacM tiene carácter aromático, consistente con la unión deslocalizada en la porción C 3 O 2 . De acuerdo con este escenario, en algunos complejos, el ligando acac es susceptible de sustitución electrofílica, similar a la sustitución aromática electrofílica (en esta ecuación Me = CH 3 ): [4]
En términos de recuento de electrones , el ligando acac bidentado neutro unido a O, O es un "ligando LX", es decir, una combinación de una base de Lewis (L) y un pseudohaluro (X).
El tratamiento de TiCl 4 con acetilacetona da cis -TiCl 2 (acac) 2 , un complejo octaédrico de color rojo con simetría C 2 :