Nitrato de metal alcalino
Los nitratos de metales alcalinos son compuestos químicos que consisten en un metal alcalino ( litio , sodio , potasio , rubidio y cesio ) y el ion nitrato . Solo dos son de gran valor comercial, las sales de sodio y potasio. [1] Son sales blancas solubles en agua con puntos de fusión que oscilan entre 255 ° C ( LiNO
3) hasta 414 ° C ( CsNO
3) en un espacio relativamente estrecho de sólo 159 ° C. [2]
| Compuesto | Fórmula química | Masa molar | Punto de fusion | Estructura |
|---|---|---|---|---|
| Nitrato de litio | LiNO 3 | 68,946 g / mol | 255 ° C (491 ° F; 528 K) |  |
| Nitrato de sodio | NaNO 3 | 84,9947 g / mol | 308 ° C (586 ° F; 581 ° K) | 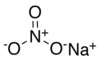 |
| Nitrato de potasio | KNO 3 | 101,1032 g / mol | 334 ° C (633 ° F; 607 K) |  |
| Nitrato de rubidio | RbNO 3 | 147,473 g / mol | 310 ° C (590 ° F; 583 K) |  |
| Nitrato de cesio | CsNO 3 | 194,91 g / mol | 414 ° C (777 ° F; 687 K) |  |
El punto de fusión de los nitratos de metales alcalinos tiende a aumentar de 255 ° C a 414 ° C (con una anomalía de que el rubidio no esté correctamente alineado en la serie) a medida que aumenta la masa atómica y el radio iónico ( catión desnudo ) del metal alcalino. , bajando en la columna. De manera similar, pero no presentada aquí en la tabla, la solubilidad de estas sales en agua también disminuye con la masa atómica del metal.
Aplicaciones
Los nitratos de sodio y potasio se utilizan comúnmente como fertilizantes . Como también son oxidantes fuertes , entran en composiciones pirotécnicas y en la fabricación de explosivos . [1]
Un uso menor es para colorear la luz emitida por los fuegos artificiales : [3]
- el nitrato de litio produce un color rojo,
- el nitrato de sodio produce un color amarillo / naranja,
- el nitrato de potasio y el nitrato de rubidio producen colores violetas,
- El nitrato de cesio produce un color índigo.
De manera general, el color emitido cambia progresivamente del rojo al violeta en el espectro de luz visible al descender en la columna de los metales alcalinos de la tabla periódica de Mendeleev . Corresponde a una disminución de la longitud de onda de la luz emitida durante el paso de desexcitación de electrones en los átomos llevados a alta temperatura. Los fotones emitidos por el cesio son más energéticos que los del litio .
Ver también
- Hidruro de metal alcalino
- Haluro de metal alcalino
- Nitrato de amonio
- Ácido nítrico
Referencias
- ^ a b Laue, Wolfgang; Thiemann, Michael; Scheibler, Erich; Wiegand, Karl (2000). "Nitratos y nitritos". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a17_265 .
- ^ "Propiedades termodinámicas de las sales de nitrato fundido" (PDF) .
- ^ "Fantasma de fuegos artificiales: Universidad de fuegos artificiales: compuestos pirotécnicos" . Fuegos artificiales fantasma . Archivado desde el original el 6 de agosto de 2020 . Consultado el 16 de octubre de 2016 .
- Nitratos
- Talones de química física
