Aminoácido aromático
Entre los 20 aminoácidos estándar, los siguientes se consideran clásicamente aromáticos: fenilalanina , triptófano y tirosina . Aunque la histidina contiene un anillo aromático, sus propiedades básicas hacen que se clasifique predominantemente como un aminoácido polar.
Los aminoácidos aromáticos absorben la luz ultravioleta a una longitud de onda superior a 250 nm y producen fluorescencia . Esta característica se utiliza en análisis cuantitativos, especialmente para determinar las concentraciones de estos aminoácidos en solución. [1] Esto se logró mediante la utilización de un espectrofotómero UV y la ecuación de la ley de Beer-Lambert . [2] La mayoría de las proteínas tendrán un máximo de absorción a 280 nm debido a la presencia de aminoácidos aromáticos en su estructura primaria. Sin embargo, debido a que existen varios aminoácidos aromáticos, este método tiene poca precisión; Para mitigar este problema, la proteína deseada debe ser pura y su absortividad molares conocida. Además, una proteína sin aminoácidos aromáticos no tendrá un máximo de absorción a aproximadamente 280 nm. La presencia de ácidos nucleicos en la proteína puede disminuir aún más la precisión del método debido a la presencia de anillos de purina y pirimidina , que tienen un máximo de absorción a aproximadamente 260 nm. La fenilalanina tiene una absorbancia relativamente débil en comparación con los otros aminoácidos aromáticos estándar; su presencia en una proteína solo puede detectarse si no hay triptófano y tirosina. [3] Su máxima absorción ocurre a 257 nm. [3] En consecuencia, tiene una fluorescencia relativamente débil. Triptófanotiene la absorbancia relativa más alta en comparación con los otros aminoácidos aromáticos estándar; su máxima absorción ocurre a 280 nm. [3] La cadena lateral del triptófano no titula. El máximo de absorción de tirosina se produce a 274 nm. [3] En reacciones químicas, la tirosina puede funcionar como nucleófilo. [4] Los aminoácidos aromáticos también juegan un papel crucial en las interacciones glucano-proteína .
Los aminoácidos aromáticos juegan un papel fundamental en la estabilización de las estructuras plegadas de muchas proteínas. [5] [6] Los residuos aromáticos se encuentran predominantemente secuestrados dentro de los núcleos de las proteínas globulares, aunque a menudo comprenden porciones clave de interfaces de interacción proteína-proteína o proteína-ligando en la superficie de la proteína.
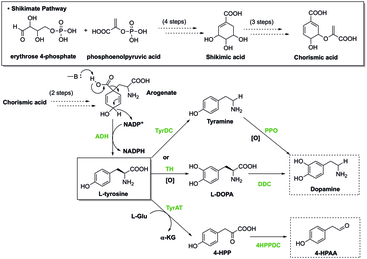
En las plantas, la vía del shikimato conduce primero a la formación de corismato , que es el precursor de la fenilalanina, la tirosina y el triptófano. Estos aminoácidos aromáticos son derivados de muchos metabolitos secundarios , todos esenciales para las funciones biológicas de una planta, como las hormonas salicilato y auxina . Esta vía contiene enzimas que pueden ser reguladas por inhibidores, que pueden detener la producción de corismato y, en última instancia, las funciones biológicas del organismo. Los herbicidas y antibióticos actúan inhibiendo estas enzimas involucradas en la biosíntesis de aminoácidos aromáticos, volviéndolos tóxicos para las plantas. [7] Glifosato, un tipo de herbicida, se utiliza para controlar la acumulación de hojas verdes en exceso. Además de destruir las verduras, el glifosato puede afectar fácilmente el mantenimiento de la microbiota intestinal en los organismos huésped al inhibir específicamente la 5-enolpiruvilinato-3-fosfato sintasa que previene la biosíntesis de aminoácidos aromáticos esenciales. La inhibición de esta enzima da como resultado trastornos como enfermedades gastrointestinales y enfermedades metabólicas. [8]
Los aminoácidos aromáticos a menudo sirven como precursores de otras moléculas. Por ejemplo, en la producción de epinefrina, la fenilalanina es la molécula de partida. La reacción se indica a continuación:
La tirosina también es un precursor de la síntesis de octopamina y melanina en numerosos organismos. [9] En la producción de tiroxina, la fenilalanina también sirve como precursor inicial: