 | |
 | |
| Datos clinicos | |
|---|---|
| Otros nombres | OCT, norsimpathol, norsinefrina, para- octopamina, beta-hidroxitiramina, para-hidroxi-fenil-etanolamina, α- (aminometil) -4 hidroxibencenometanol, 1- (p-hidroxifenil) -2-aminoetanol |
| Vías de administración | Oral |
| Código ATC | |
| Datos fisiológicos | |
| Tejidos de origen | sistemas nerviosos invertebrados; trazas de amina en vertebrados |
| Tejidos diana | en todo el sistema en invertebrados |
| Receptores | TAAR1 (mamíferos) OctαR, OctβR, TyrR (invertebrados), Oct-TyrR |
| Agonistas | Formamidinas (amitraz (AMZ) y clordimeform (CDM)) |
| Antagonistas | epinastina (clorhidrato de 3-amino-9, 13b-dihidro-1H-dibenz (c, f) imidazo (1,5a) azepina) |
| Precursor | tiramina |
| Biosíntesis | tiramina β-hidroxilasa ; dopamina β-hidroxilasa |
| Metabolismo | ácido p- hidroximandélico; [1] [2] N-acetiltransferasas ; feniletanolamina N-metiltransferasa |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | 99,42% |
| Metabolismo | ácido p- hidroximandélico; [1] [2] N-acetiltransferasas ; feniletanolamina N-metiltransferasa |
| Vida media de eliminación | 15 minutos en insectos. Entre 76 y 175 minutos en humanos |
| Excreción | Hasta el 93% de la octopamina ingerida se elimina por vía urinaria en 24 horas [1] |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| ChemSpider | |
| UNII |
|
| CHEBI |
|
| CHEMBL |
|
| Tablero CompTox ( EPA ) |
|
| Tarjeta de información ECHA | 100.002.890 |
| Datos químicos y físicos | |
| Fórmula | C 8 H 11 N O 2 |
| Masa molar | 153,181 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
Sonrisas
| |
InChI
| |
| | |
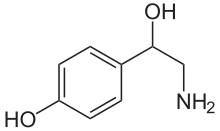
La octopamina (fórmula molecular C 8 H 11 NO 2 ; también conocida como norsinefrina , para -octopamina y otras) es una sustancia química orgánica estrechamente relacionada con la norepinefrina y sintetizada biológicamente por una vía homóloga. Su nombre deriva del hecho de que se identificó por primera vez en las glándulas salivales del pulpo.
En muchos tipos de invertebrados, la octopamina es un neurotransmisor y una hormona importante . En los protostomas (artrópodos, moluscos y varios tipos de gusanos) sustituye a la norefinfrina y realiza funciones aparentemente similares a las de la norepinefrina en los mamíferos, funciones que se han descrito como movilizar el cuerpo y el sistema nervioso para la acción. En los mamíferos, la octopamina se encuentra solo en pequeñas cantidades y no se ha establecido sólidamente ninguna función biológica para ella. También se encuentra naturalmente en numerosas plantas, incluida la naranja amarga . [3] [4] La octopamina se ha vendido bajo nombres comerciales como Epirenor , Norden y Norfen.para su uso como fármaco simpaticomimético , disponible con receta médica.
Funciones [ editar ]
Efectos celulares [ editar ]
La octopamina ejerce sus efectos al unirse y activar los receptores ubicados en la superficie de las células. Estos receptores se han estudiado principalmente en insectos, donde se pueden dividir en tres tipos: tipo alfa-adrenérgico (OctαR), que son estructural y funcionalmente similares a los receptores alfa-1 noradrenérgicos en mamíferos; similares a beta-adrenérgicos (OctβR), que son estructural y funcionalmente similares a los receptores beta noradrenérgicos en mamíferos; y receptores mixtos de octopamina / tiramina (TyrR), que son estructural y funcionalmente similares a los receptores alfa-2 noradrenérgicos en mamíferos. [5] Los receptores de la clase TyrR, sin embargo, son generalmente más fuertemente activados por la tiramina que por la octopamina. [5]
En los vertebrados no se han identificado receptores específicos de octopamina. La octopamina se une débilmente a los receptores de norepinefrina y epinefrina , pero no está claro si esto tiene algún significado funcional. Se une con más fuerza a trazas de receptores asociados a aminas (TAAR), especialmente TAAR1 . [5]
Invertebrados [ editar ]
La octopamina fue descubierta por primera vez por el científico italiano Vittorio Erspamer en 1948 [6] en las glándulas salivales del pulpo y desde entonces se ha descubierto que actúa como neurotransmisor , neurohormona y neuromodulador en invertebrados . Aunque Erspamer descubrió su ocurrencia natural y la nombró, la octopamina había existido durante muchos años como producto farmacéutico. [7] Es ampliamente utilizado en comportamientos que demandan energía por todos los insectos, crustáceos (cangrejos, langostas, cangrejos de río) y arañas. Tales comportamientos incluyen volar, [8] poner huevos, [9] y saltar. [10] [11]
La octopamina actúa como insecto equivalente a la norepinefrina y se ha implicado en la regulación de la agresión en invertebrados, con diferentes efectos en diferentes especies. Los estudios han demostrado que la reducción del neurotransmisor octopamina y la prevención de la codificación de la tiramina beta hidroxilasa (una enzima que convierte la tiramina en octopamina) disminuye la agresión en Drosophila sin influir en otros comportamientos. [12]
En los insectos, la octopamina es liberada por un número selecto de neuronas, pero actúa ampliamente en todo el cerebro central, en todos los órganos de los sentidos y en varios tejidos no neuronales. [13] [14] En los ganglios torácicos, la octopamina es liberada principalmente por las neuronas DUM (mediana dorsal no apareada) y VUM (mediana ventral no apareada), que liberan octopamina en objetivos neurales, musculares y periféricos. [15] [16] Estas neuronas son importantes para mediar los comportamientos motores que demandan energía, como el salto y el vuelo inducidos por el escape. Por ejemplo, la neurona de la langosta DUMeti libera octopamina en el músculo extensor de la tibia para aumentar la tensión muscular y aumentar la tasa de relajación. Estas acciones promueven la contracción eficiente de los músculos de las piernas para saltar. [13]Durante el vuelo, las neuronas DUM también están activas y liberan octopamina por todo el cuerpo para sincronizar el metabolismo energético, la respiración, la actividad muscular y la actividad de las interneuronas de vuelo. [8] La octopamina en las langostas está cuatro veces más concentrada en el axón que en el soma y disminuye el ritmo miogénico de la langosta . [17]
En la abeja melífera y la mosca de la fruta , la octopamina tiene un papel importante en el aprendizaje y la memoria. En la luciérnaga , la liberación de octopamina conduce a la producción de luz en la linterna. [18] [19]
En las langostas, la octopamina parece dirigir y coordinar las neurohormonas hasta cierto punto en el sistema nervioso central, y se observó que la inyección de octopamina en una langosta y cangrejo de río resultó en la extensión de las extremidades y el abdomen. [20]
Heberlein y col. [21] han realizado estudios de tolerancia al alcohol en moscas de la fruta; encontraron que una mutación que causó la deficiencia de octopamina también causó una menor tolerancia al alcohol. [22] [23] [24] [25]
La avispa cucaracha esmeralda pica al huésped por sus larvas (una cucaracha) en el ganglio de la cabeza (cerebro). El veneno bloquea los receptores de octopamina [26] y la cucaracha no muestra respuestas de escape normales, acicalándose excesivamente. Se vuelve dócil y la avispa la conduce a la guarida de la avispa tirando de su antena como una correa. [27]
En el nematodo , la octopamina se encuentra en altas concentraciones en adultos, disminuyendo los comportamientos de puesta de huevos y bombeo faríngeo con un efecto antagónico a la serotonina . [28]
Los nervios octopaminérgicos del molusco pueden estar presentes en el corazón, con altas concentraciones en el sistema nervioso. [29]
En las larvas del gusano soldado oriental , la octopamina es inmunológicamente beneficiosa, aumentando las tasas de supervivencia en poblaciones de alta densidad. [30]
Vertebrados [ editar ]
En los vertebrados , la octopamina reemplaza a la noradrenalina en las neuronas simpáticas con el uso crónico de inhibidores de la monoaminooxidasa . Puede ser responsable del efecto secundario común de la hipotensión ortostática con estos agentes, aunque también hay evidencia de que en realidad está mediado por niveles elevados de N- acetilserotonina .
Un estudio señaló que la octopamina podría ser una amina importante que influye en los efectos terapéuticos de inhibidores como los inhibidores de la monoaminooxidasa , especialmente porque se observó un gran aumento en los niveles de octopamina cuando los animales fueron tratados con este inhibidor. La octopamina se identificó positivamente en las muestras de orina de mamíferos como humanos, ratas y conejos tratados con inhibidores de la monoaminooxidasa . También se encontraron cantidades muy pequeñas de octopamina en ciertos tejidos animales. Se observó que dentro del cuerpo de un conejo, el corazón y el riñón tenían las concentraciones más altas de octopamina. Se encontró que la octopamina se eluye en un 93% por la orina dentro de las 24 horas posteriores a su producción en el cuerpo como un subproducto de Iproniazid en conejos. [7]
Farmacología [ editar ]
La octopamina se ha vendido bajo nombres comerciales como Epirenor , Norden y Norfen para su uso en medicina como fármaco simpaticomimético , disponible con receta médica. Sin embargo, existe muy poca información sobre su utilidad clínica o seguridad. [31]
En los mamíferos , la octopamina puede movilizar la liberación de grasa de los adipocitos (células grasas), lo que ha llevado a su promoción en Internet como ayuda para adelgazar. Sin embargo, es probable que la grasa liberada sea absorbida rápidamente por otras células y no hay evidencia de que la octopamina facilite la pérdida de peso. La octopamina también puede aumentar la presión arterial de manera significativa cuando se combina con otros estimulantes , como en algunos suplementos para bajar de peso . [32]
La Agencia Mundial Antidopaje enumera la octopamina como sustancia prohibida para uso en competición, como un "estimulante especificado" [33] en la Lista de Prohibiciones de 2019.
Insecticidas [ editar ]
El receptor de octopamina es un objetivo de los insecticidas, ya que su bloqueo conduce a niveles reducidos de AMPc. Los aceites esenciales pueden tener tal efecto neuroinsecticida, [34] y este mecanismo receptor de octopamina es utilizado naturalmente por plantas con fitoquímicos insecticidas activos. [35]
Mecanismos bioquímicos [ editar ]
Mamíferos [ editar ]
La octopamina es uno de los cuatro agonistas endógenos primarios del receptor 1 asociado a trazas de amina humana . [36]
Invertebrados [ editar ]
La octopamina se une a sus respectivos receptores acoplados a proteína G (GPCR) para iniciar una vía de transducción de señales celulares. Se han definido al menos tres grupos de octopamina GPCR. Los receptores OctαR (OCTOPAMINE1) están más estrechamente relacionados con los receptores α-adrenérgicos, mientras que los OctβR (receptores OCTOPAMINE2) están más estrechamente relacionados con los receptores β-adrenérgicos. Los receptores de octopamina / tiramina (incluido Oct-TyrR) pueden unirse a ambos ligandos y mostrar un acoplamiento específico de agonista. Oct-TyrR está incluido en los grupos de genes RECEPTORES DE TIRAMINA y OCTOPAMINA. [37]
Biosíntesis [ editar ]
En humanos [ editar ]
Vías biosintéticas para catecolaminas y aminas traza en el cerebro humano [38] [39] [40] |
Ver también [ editar ]
- Fenetilamina
- Feniletanolamina
- Traza de amina
Referencias [ editar ]
- ^ a b Hengstmann, JH; Konen, W; Konen, C; Eichelbaum, M; Dengler, HJ (1974). "La disposición fisiológica de p-octopamina en el hombre". Archivos de Farmacología de Naunyn-Schmiedeberg . 283 (1): 93–106. doi : 10.1007 / bf00500148 . PMID 4277715 . S2CID 35523412 .
- ↑ d'Andrea, Giovanni; Nordera, Gianpietro; Pizzolato, Gilberto; Bolner, Andrea; Colavito, Davide; Flaibani, Raffaella; León, Alberta (2010). "Traza el metabolismo de las aminas en la enfermedad de Parkinson: bajos niveles circulantes de octopamina en las primeras etapas de la enfermedad". Cartas de neurociencia . 469 (3): 348–51. doi : 10.1016 / j.neulet.2009.12.025 . PMID 20026245 . S2CID 12797090 .
- ^ Tang F, Tao L, Luo X, Ding L, Guo M, Nie L, Yao S (septiembre de 2006). "Determinación de octopamina, sinefrina y tiramina en hierbas cítricas mediante cromatografía 'verde' mejorada de líquido iónico". Journal of Chromatography A . 1125 (2): 182–8. doi : 10.1016 / j.chroma.2006.05.049 . PMID 16781718 .
- ^ Jagiełło-Wójtowicz E (1979). "Mecanismo de acción central de la octopamina". Revista polaca de farmacología y farmacia . 31 (5): 509–16. PMID 121158 .
- ↑ a b c Pflüger HJ, Stevensonb PA (2005). "Aspectos evolutivos de los sistemas octopaminérgicos con énfasis en artrópodos" . Estructura y desarrollo de artrópodos . 34 (3): 379–396. doi : 10.1016 / j.asd.2005.04.004 .Mantenimiento de CS1: utiliza el parámetro de autores ( enlace )
- ^ Erspamer, V. (2009). "Sustancias activas en las glándulas salivales posteriores de octópodos. II. Tiramina y octopamina (oxioctopamina)". Acta Pharmacologica et Toxicologica . 4 (3–4): 224–47. doi : 10.1111 / j.1600-0773.1948.tb03345.x .
- ↑ a b Kakimoto Y, Armstrong MD (febrero de 1962). "Sobre la identificación de octopamina en mamíferos". La Revista de Química Biológica . 237 : 422–7. PMID 14453200 .
- ^ a b Huerto, yo; Ramírez, JM; Lange, AB (enero de 1993). "Un papel multifuncional de la octopamina en el vuelo de la langosta". Revisión anual de entomología . 38 (1): 227–249. doi : 10.1146 / annurev.en.38.010193.001303 . ISSN 0066-4170 .
- ^ Lee, Hyun-Gwan; Seong, Chang-Soo; Kim, Young-Cho; Davis, Ronald L; Han, Kyung-An (1 de diciembre de 2003). "El receptor de octopamina OAMB es necesario para la ovulación en Drosophila melanogaster" . Biología del desarrollo . 264 (1): 179-190. doi : 10.1016 / j.ydbio.2003.07.018 . ISSN 0012-1606 . PMID 14623240 .
- ^ Pollack, Alan J .; Ritzmann, Roy E .; Westin, Joanne (1988). "Activación de interneuronas de células DUM por interneuronas gigantes ventrales en la cucaracha, periplaneta americana". Revista de neurobiología . 19 (6): 489–497. doi : 10.1002 / neu.480190602 . ISSN 1097-4695 . PMID 3171574 .
- ^ Orchard, Ian (1 de abril de 1982). "Octopamina en insectos: neurotransmisor, neurohormona y neuromodulador". Revista canadiense de zoología . 60 (4): 659–669. doi : 10.1139 / z82-095 . ISSN 0008-4301 .
- ^ Zhou C, Rao Y, Rao Y (septiembre de 2008). "Un subconjunto de neuronas octopaminérgicas son importantes para la agresión de Drosophila". Neurociencia de la naturaleza . 11 (9): 1059–67. doi : 10.1038 / nn.2164 . PMID 19160504 . S2CID 1134848 .
- ^ a b Atwood, HL; Klose, MK (1 de enero de 2009), "Modulación de transmisión neuromuscular en uniones neuromusculares de invertebrados" , en Squire, Larry R. (ed.), Encyclopedia of Neuroscience , Oxford: Academic Press, págs. 671–690, ISBN 978-0-08-045046-9, consultado el 10 de julio de 2020
- ^ Roeder, T. (diciembre de 1999). "Octopamina en invertebrados". Progresos en neurobiología . 59 (5): 533–561. doi : 10.1016 / s0301-0082 (99) 00016-7 . ISSN 0301-0082 . PMID 10515667 . S2CID 25654298 .
- ^ Eckert, Manfred; Rapus, Jürgen; Nürnberger, Asja; Penzlin, Heinz (1992). "Un nuevo anticuerpo específico revela inmunorreactividad similar a la octopamina en el cordón nervioso ventral de la cucaracha". Revista de Neurología Comparada (en francés). 322 (1): 1-15. doi : 10.1002 / cne.903220102 . ISSN 1096-9861 . PMID 1430305 . S2CID 41099770 .
- ^ Sinakevitch, Irina G .; Geffard, Michel; Pelhate, Marcel; Lapied, Bruno (abril de 1994). "Inmunorreactividad similar a la octopamina en las neuronas dorsal no apareadas medianas (DUM) que inervan la glándula accesoria de la cucaracha macho Periplaneta americana". Investigación de células y tejidos . 276 (1): 15-21. doi : 10.1007 / bf00354779 . ISSN 0302-766X . S2CID 23485136 .
- ^ Evans, PD; O'Shea, M. (abril de 1978). "La identificación de una neurona octopaminérgica y la modulación de un ritmo miogénico en la langosta" . La Revista de Biología Experimental . 73 : 235-260. ISSN 0022-0949 . PMID 25941 .
- ^ Greenfield MD (noviembre de 2001). "El eslabón perdido en la bioluminiscencia de la luciérnaga reveló: NO hay regulación de la respiración de los fotocitos". BioEssays . 23 (11): 992–5. doi : 10.1002 / bies.1144 . PMID 11746215 .
- ^ Trimmer BA, Aprille JR, Dudzinski DM, Lagace CJ, Lewis SM, Michel T, et al. (Junio de 2001). "Óxido nítrico y el control del flasheo de luciérnagas". Ciencia . 292 (5526): 2486–8. doi : 10.1126 / science.1059833 . PMID 11431567 . S2CID 1095642 .
- ^ Livingstone MS, Harris-Warrick RM, Kravitz EA (abril de 1980). "La serotonina y la octopamina producen posturas opuestas en las langostas" . Ciencia . 208 (4439): 76–9. Código Bibliográfico : 1980Sci ... 208 ... 76L . doi : 10.1126 / science.208.4439.76 . PMID 17731572 . S2CID 32141532 .
- ^ Heberlein U, Wolf FW, Rothenfluh A, Guarnieri DJ (agosto de 2004). "Análisis genético molecular de la intoxicación por etanol en Drosophila melanogaster". Biología Integrativa y Comparada . 44 (4): 269–74. CiteSeerX 10.1.1.536.262 . doi : 10.1093 / icb / 44.4.269 . PMID 21676709 . S2CID 14762870 .
- ^ Moore MS, DeZazzo J, Luk AY, Tully T, Singh CM, Heberlein U (junio de 1998). "Intoxicación por etanol en Drosophila: evidencia genética y farmacológica para la regulación por la vía de señalización de cAMP". Celular . 93 (6): 997–1007. doi : 10.1016 / S0092-8674 (00) 81205-2 . PMID 9635429 . S2CID 15312752 .
- ^ Tecott LH, Heberlein U (diciembre de 1998). "¿Bebemos?" . Celular . 95 (6): 733–5. doi : 10.1016 / S0092-8674 (00) 81695-5 . PMID 9865690 .
- ^ Williams, Ruth (22 de junio de 2005). "Bar Flies: lo que nuestros parientes insectos pueden enseñarnos sobre la tolerancia al alcohol" . Científico desnudo .
- ^ Vince, Gaia (22 de agosto de 2005). "El ' gen de la resaca' es clave para la tolerancia al alcohol" . Nuevo científico .
- ^ Hopkin, Michael (2007). "Cómo hacer una cucaracha zombie". Naturaleza . doi : 10.1038 / news.2007.312 .
- ^ Gal R, Rosenberg LA, Libersat F (diciembre de 2005). "La avispa parasitoide utiliza un cóctel de veneno inyectado en el cerebro para manipular el comportamiento y el metabolismo de su presa de cucarachas". Archivos de Bioquímica y Fisiología de Insectos . 60 (4): 198-208. doi : 10.1002 / arq.20092 . PMID 16304619 .
- ^ Horvitz, HR; Chalfie, M .; Trent, C .; Sulston, JE; Evans, PD (28 de mayo de 1982). "Serotonina y octopamina en el nematodo Caenorhabditis elegans" . Ciencia . 216 (4549): 1012–1014. doi : 10.1126 / science.6805073 . ISSN 0036-8075 . PMID 6805073 .
- ^ Dougan, DFH; Duffield, PH; Wade, DN; Duffield, AM (1 de enero de 1981). "Aparición y síntesis de octopamina en el corazón y ganglios del molusco Tapes watlingi" . Bioquímica y fisiología comparada Parte C: Farmacología comparada . 70 (2): 277–280. doi : 10.1016 / 0306-4492 (81) 90064-2 . ISSN 0306-4492 .
- ^ Kong, Hailong; Yuan, Lin; Dong, Chuanlei; Zheng, Minyuan; Jing, Wanghui; Tian, Zhen; Hou, Qiuli; Cheng, Yunxia; Zhang, Lei; Jiang, Xingfu; Luo, Lizhi (diciembre de 2020). "Regulación inmunológica por un gen receptor de octopamina de tipo β-adrenérgico en larvas apiñadas del gusano cogollero oriental, Mythmina separata" . Inmunología del desarrollo y comparada . 113 : 103802. doi : 10.1016 / j.dci.2020.103802 . ISSN 1879-0089 . PMID 32712170 .
- ^ Stohs SJ (enero de 2015). "Funciones fisiológicas y efectos farmacológicos y toxicológicos de la p-octopamina". Toxicología farmacológica y química . 38 (1): 106-12. doi : 10.3109 / 01480545.2014.900069 . PMID 24654910 . S2CID 21901553 .
- ^ Haller CA, Benowitz NL, Jacob P (septiembre de 2005). "Efectos hemodinámicos de los suplementos para bajar de peso sin efedra en humanos". La Revista Estadounidense de Medicina . 118 (9): 998–1003. doi : 10.1016 / j.amjmed.2005.02.034 . PMID 16164886 .
- ^ "Prohibido en competición - estimulantes" . AMA . Consultado el 6 de mayo de 2019 .
- ^ Enan, Essam (1 de noviembre de 2001). "Actividad insecticida de los aceites esenciales: sitios de acción octopaminérgicos" . Bioquímica y fisiología comparada Parte C: Toxicología y farmacología . 130 (3): 325–337. doi : 10.1016 / S1532-0456 (01) 00255-1 . ISSN 1532-0456 .
- ^ Rattan, Rameshwar Singh (1 de septiembre de 2010). "Mecanismo de acción de los metabolitos secundarios insecticidas de origen vegetal" . Protección de cultivos . 29 (9): 913–920. doi : 10.1016 / j.cropro.2010.05.008 . ISSN 0261-2194 .
- ^ Maguire JJ, Davenport AP (20 de febrero de 2018). "Receptor de trazas de amina: receptor TA 1 " . Guía IUPHAR / BPS de FARMACOLOGÍA . Unión Internacional de Farmacología Básica y Clínica . Consultado el 16 de julio de 2018 .
- ^ "Grupo de genes: RECEPTORES DE OCTOPAMINA" , FlyBase, 16 de octubre de 2018.
- ^ Broadley KJ (marzo de 2010). "Los efectos vasculares de las trazas de aminas y anfetaminas". Farmacología y terapéutica . 125 (3): 363–375. doi : 10.1016 / j.pharmthera.2009.11.005 . PMID 19948186 .
- ^ Lindemann L, Hoener MC (mayo de 2005). "Un renacimiento en trazas de aminas inspirado en una nueva familia GPCR". Tendencias en Ciencias Farmacológicas . 26 (5): 274–281. doi : 10.1016 / j.tips.2005.03.007 . PMID 15860375 .
- ^ Wang X, Li J, Dong G, Yue J (febrero de 2014). "Los sustratos endógenos del cerebro CYP2D". Revista europea de farmacología . 724 : 211–218. doi : 10.1016 / j.ejphar.2013.12.025 . PMID 24374199 .