 | |
 | |
| Datos clinicos | |
|---|---|
| Nombres comerciales | Strattera, otros |
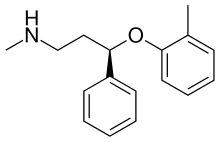
| Otros nombres | ( R ) - N -Metil-3-fenil-3- ( o -toliloxi) propan-1-amina |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a603013 |
| Datos de licencia |
|
| Categoría de embarazo |
|
| Vías de administración | Oral |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | 63 a 94% [2] [3] [4] |
| Enlace proteico | 98% [2] [3] [4] |
| Metabolismo | Hígado , a través de CYP2D6 [2] [3] [4] |
| Vida media de eliminación | 4.5-19 horas [2] [3] [4] [5] [6] |
| Excreción | Riñón (80%) y fecal (17%) [2] [3] [4] |
| Identificadores | |
| |
| Número CAS |
|
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL |
|
| Tablero CompTox ( EPA ) |
|
| Tarjeta de información ECHA | 100.120.306 |
| Datos químicos y físicos | |
| Fórmula | C 17 H 21 N O |
| Masa molar | 255,361 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
Sonrisas
| |
InChI
| |
| | |
La atomoxetina , que se vende bajo la marca Strattera , entre otros, es un medicamento que se usa para tratar el trastorno por déficit de atención con hiperactividad (TDAH). [7] Puede usarse solo o junto con psicoestimulantes . [8] [9] El uso de atomoxetina solo se recomienda para quienes tienen al menos seis años de edad. [7] Se toma por vía oral. [7] Fue aprobado para uso médico en los Estados Unidos en 2002. [7] En 2018, fue el 162º medicamento recetado con más frecuencia en los Estados Unidos, con más de 3 millones de recetas. [10] [11]
Los efectos secundarios comunes de la atomoxetina incluyen dolor abdominal, pérdida de apetito, náuseas, cansancio y mareos. [7] Los efectos secundarios graves pueden incluir angioedema , problemas hepáticos, accidente cerebrovascular , psicosis , problemas cardíacos, suicidio y agresión. [7] [12] Hay una falta de datos sobre su seguridad durante el embarazo ; a partir de 2019, su seguridad durante el embarazo y para su uso durante la lactancia no es segura. [13] [14]
La atomoxetina es un inhibidor de la recaptación de noradrenalina y se cree que actúa aumentando los niveles de noradrenalina y dopamina en el cerebro. [7] [5]
Usos médicos [ editar ]
Trastorno por déficit de atención con hiperactividad [ editar ]
La atomoxetina está aprobada para su uso en niños, adolescentes y adultos. [15] Sin embargo, su eficacia no se ha estudiado en niños menores de seis años. [3] Su principal ventaja sobre los tratamientos estimulantes estándar para el TDAH es que tiene poco potencial de abuso conocido. [3] Si bien se ha demostrado que reduce significativamente los síntomas de inatención e hiperactividad , las respuestas fueron más bajas que la respuesta a los estimulantes. Además, el 40% de los participantes que fueron tratados con atomoxetina experimentaron síntomas residuales de TDAH. [dieciséis]
Si bien su eficacia puede ser menor que la de los medicamentos estimulantes, [17] hay alguna evidencia de que puede usarse en combinación con estimulantes. [8] Los médicos pueden recetar no estimulantes, incluida la atomoxetina, cuando una persona tiene efectos secundarios molestos de los estimulantes; cuando un estimulante no fue eficaz; en combinación con un estimulante para aumentar la eficacia; [18] [19] o cuando existe preocupación sobre el potencial de abuso de psicoestimulantes en un paciente con antecedentes de trastorno por consumo de drogas .
A diferencia de los agonistas de los receptores adrenérgicos α 2 como la guanfacina y la clonidina , el uso de atomoxetina se puede interrumpir abruptamente sin que se observen efectos de interrupción significativos. [3]
Los efectos terapéuticos iniciales de la atomoxetina suelen tardar de 2 a 4 semanas en manifestarse. [2] Es posible que se requieran de 2 a 4 semanas más para que se observen los efectos terapéuticos completos. [20] La dosis diaria total máxima recomendada en niños y adolescentes de más de 70 kg y adultos es de 100 mg. [15]
Otro [ editar ]
La atomoxetina puede usarse en personas con TDAH y trastorno bipolar, aunque dicho uso no ha sido bien estudiado. [21] También se han observado algunos beneficios en personas con TDAH y autismo . [22]
Contraindicaciones [ editar ]
Las contraindicaciones incluyen: [3]
- Hipersensibilidad a la atomoxetina o cualquiera de los ingredientes inactivos del producto.
- Enfermedad cardiovascular sintomática que incluye:
- Moderada a severa hipertensión
- - fibrilación auricular
- - aleteo auricular
- - taquicardia ventricular
- - fibrilación ventricular
- - aleteo ventricular
- arteriosclerosis avanzada
- Trastornos cardiovasculares graves.
- Feocromocitoma
- Tratamiento concomitante con inhibidores de la monoaminooxidasa
- Glaucoma de ángulo estrecho
- Metabolizadores lentos (debido al metabolismo de la atomoxetina por CYP2D6 )
Efectos adversos [ editar ]
Los efectos secundarios comunes incluyen dolor abdominal, pérdida de apetito, náuseas, cansancio y mareos. [7] Los efectos secundarios graves pueden incluir angioedema , problemas hepáticos, accidente cerebrovascular , psicosis , problemas cardíacos, suicidio y agresión. [7] [12] Un metanálisis de 2020 encontró que la atomoxetina se asoció con anorexia , pérdida de peso e hipertensión , calificándola como un "agente potencialmente menos preferido según la seguridad" para el tratamiento del TDAH. [23] A partir de 2019, la seguridad durante el embarazo y la lactancia no está clara; [13]una revisión de 2018 indicó que, "[b] ebido a la falta de datos, el médico tratante debe considerar suspender el tratamiento con atomoxetina en mujeres con TDAH durante el embarazo". [14]
La Administración de Drogas y Alimentos de los Estados Unidos (FDA) ha emitido una advertencia de recuadro negro para conductas / ideas suicidas. [4] Se han emitido advertencias similares en Australia. [3] [24] A diferencia de los medicamentos estimulantes, la atomoxetina no tiene riesgo de abuso o el potencial de causar efectos de abstinencia en la interrupción abrupta. [3]
Incidencia de efectos adversos: [3] [4] [25] [26]
Los efectos adversos muy frecuentes (> 10% de incidencia) incluyen:
- Náuseas (26%)
- Xerostomía (boca seca) (20%)
- Pérdida de apetito (16%)
- Insomnio (15%)
- Fatiga (10%)
- Dolor de cabeza
- Tos
- Vómitos (en niños y adolescentes)
Los efectos adversos frecuentes (incidencia del 1 al 10%) incluyen:
- Estreñimiento (8%)
- Mareos (8%)
- Disfunción eréctil (8%)
- Somnolencia (somnolencia) (8%)
- Dolor abdominal (7%)
- Vacilación urinaria (6%)
- Taquicardia (frecuencia cardíaca alta) (5-10%)
- Hipertensión (presión arterial alta) (5 a 10%)
- Irritabilidad (5%)
- Sueños anormales (4%)
- Dispepsia (4%)
- Trastorno de la eyaculación (4%)
- Hiperhidrosis (aumento anormal de la sudoración) (4%)
- Vómitos (4%)
- Sofocos (3%)
- Parestesia (sensación de hormigueo, cosquilleo, etc.) (3%)
- Trastorno menstrual (3%)
- Pérdida de peso (2%)
- Depresión
- Dolor de cabeza por sinusitis
- Dermatitis
- Cambios de humor
Los efectos adversos poco frecuentes (incidencia del 0,1% al 1%) incluyen:
- Eventos relacionados con el suicidio
- Hostilidad
- Labilidad emocional
- Agresión
- Psicosis
- Síncope (desmayo)
- Temblor
- Migraña
- Hipoestesia
- Embargo
- Palpitaciones
- Taquicardia sinusal
- Prolongación del intervalo QT
- Aumento de la bilirrubina en sangre
- Reacciones alérgicas
Efectos adversos raros (incidencia de 0,01 a 0,1%) que incluyen:
- El fenómeno de Raynaud
- Pruebas de función hepática anormales / aumentadas
- Ictericia
- Hepatitis
- Daño hepático
- Insuficiencia hepática aguda
- Retención urinaria
- Priapismo [27]
- Dolor genital masculino
Sobredosis [ editar ]
La atomoxetina es relativamente no tóxica en sobredosis. Las sobredosis de un solo fármaco que implican más de 1500 mg de atomoxetina no han provocado la muerte. [3] Los síntomas más comunes de una sobredosis incluyen: [3]
- Síntomas gastrointestinales
- Somnolencia
- Mareo
- Temblor
- Comportamiento anormal
- Hiperactividad
- Agitación
- Boca seca
- Taquicardia
- Hipertensión
- Midriasis
Síntomas menos comunes: [3]
- Convulsiones
- Prolongación del intervalo QTc
El tratamiento recomendado para la sobredosis de atomoxetina incluye el uso de carbón activado para evitar una mayor absorción del fármaco. [3]
Interacciones [ editar ]
La atomoxetina es un sustrato de CYP2D6 . Se ha demostrado que el tratamiento concomitante con un inhibidor de CYP2D6 como bupropión , fluoxetina o paroxetina aumenta la atomoxetina plasmática en un 100% o más, así como los niveles de N -desmetilatomoxetina y disminuyen los niveles plasmáticos de 4-hidroxiatomoxetina en un grado similar. [28] [29] [30]
La atomoxetina se ha encontrado que inhiben directamente hERG corrientes de potasio con un IC 50 de 6,3 M, que tiene el potencial de causar arritmia . [29] [31] Se notificó prolongación del intervalo QT con atomoxetina en dosis terapéuticas y en sobredosis; Se sugiere que la atomoxetina no se use con otros medicamentos que puedan prolongar el intervalo QT , concomitantemente con inhibidores de CYP2D6, y se debe tener precaución para usar en metabolizadores lentos. [29]
Otras interacciones medicamentosas notables incluyen: [3]
- Agentes antihipertensivos , debido a que la atomoxetina actúa como simpaticomimético indirecto.
- -Acción indirecta simpatomiméticos , tales como pseudoefedrina , inhibidores de la recaptación de norepinefrina , o inhibidores de la MAO
- Simpaticomiméticos de acción directa, como la fenilefrina u otros agonistas de los receptores adrenérgicos α 1 , incluidos los presores como la dobutamina o la isoprenalina y los agonistas de los receptores adrenérgicos β 2
- Fármacos altamente unidos a proteínas plasmáticas: la atomoxetina tiene el potencial de desplazar estos fármacos de las proteínas plasmáticas que pueden potenciar sus efectos adversos o tóxicos. In vitro , la atomoxetina no afecta la unión a proteínas plasmáticas de aspirina , desipramina , diazepam , paroxetina , fenitoína o warfarina [5] [32]
Farmacología [ editar ]
Farmacodinámica [ editar ]
| Sitio | ATX | 4-OH-ATX | N-DM-ATX | |
|---|---|---|---|---|
| SERT | 77 | 43 | DAKOTA DEL NORTE | |
| NETO | 5 | 3 | 92 | |
| DAT | 1,451 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| 5-HT 1A | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| 5-HT 1B | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| 5-HT 1D | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| 5-HT 2 | 2.000 | 1.000 | 1.700 | |
| 5-HT 6 | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| 5-HT 7 | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| α 1 | 11,400 | 20.000 | 19.600 | |
| α 2A | 29.800 | > 30.000 | > 10,000 | |
| β 1 | 18.000 | 56,100 | 32,100 | |
| M 1 | > 100.000 | > 100.000 | > 100.000 | |
| M 2 | > 100.000 | > 100.000 | > 100.000 | |
| D 1 | > 10,000 | > 10,000 | > 10,000 | |
| D 2 | > 10,000 | > 10,000 | > 10,000 | |
| H 1 | 12,100 | > 100.000 | > 100.000 | |
| MOR | DAKOTA DEL NORTE | 422 | DAKOTA DEL NORTE | |
| INSECTO | DAKOTA DEL NORTE | 300 | DAKOTA DEL NORTE | |
| KOR | DAKOTA DEL NORTE | 95 | DAKOTA DEL NORTE | |
| σ 1 | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| GABA A | 200 | > 30.000 | > 10,000 | |
| NMDA | 3.470 una | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| K ir 3.1 / 3.2 | 10,900 b | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| K ir 3.2 | 12,400 b | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| K ir 3.1 / 3.4 | 6.500 b | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| hERG | 6.300 | 20.000 | 5.710 | |
| Los valores son K i (nM). Cuanto menor es el valor, más fuertemente se une el fármaco al sitio. Todos los valores son para receptores humanos a menos que se especifique lo contrario. una corteza de rata. b Ovocitos de Xenopus . Fuentes adicionales: [35] [36] [5] [32] | ||||
La atomoxetina inhibe el transportador presináptico de norepinefrina (NET), lo que evita la recaptación de norepinefrina en todo el cerebro e inhibe la recaptación de dopamina en regiones específicas del cerebro como la corteza prefrontal, donde la expresión del transportador de dopamina (DAT) es mínima. [5] En ratas, la atomoxetina aumentó las concentraciones de catecolaminas de la corteza prefrontal sin alterar los niveles de dopamina en el cuerpo estriado o el núcleo accumbens ; en contraste, se encontró que el metilfenidato , un inhibidor de la recaptación de dopamina , aumentaba los niveles de dopamina prefrontal, estriado y accumbal en el mismo grado.[35] En ratones, también se encontró que la atomoxetina aumenta los niveles de catecolaminas prefrontales sin afectar los niveles del estriado o accumbal. [37]
El estado de la atomoxetina como inhibidor del transportador de serotonina (SERT) a dosis clínicas en humanos es incierto. Un estudio de imágenes de PET en monos rhesus encontró que la atomoxetina ocupaba> 90% y> 85% de NET y SERT neurales, respectivamente. [38] Sin embargo, tanto los estudios de microdiálisis en ratones como en ratas no han logrado encontrar un aumento de la serotonina extracelular en la corteza prefrontal después del tratamiento con atomoxetina aguda o crónica. [35] [37] Respaldando la selectividad de la atomoxetina, un estudio en humanos no encontró efectos sobre la captación de serotonina plaquetaria (un marcador de inhibición de SERT) y la inhibición de los efectos presores de tiramina(un marcador de inhibición de NET). [39]
Se ha descubierto que la atomoxetina actúa como un antagonista del receptor de NMDA en neuronas corticales de rata a concentraciones terapéuticas. [40] [41] Causa un bloqueo de canal abierto dependiente del uso y su sitio de unión se superpone con el sitio de unión de Mg 2+ . [40] [41] La capacidad de la atomoxetina para aumentar la tasa de activación de la corteza prefrontal en ratas anestesiadas no podría bloquearse con antagonistas de los receptores adrenérgicos D 1 o α 2 , pero podría potenciarse con NMDA o un antagonista del receptor adrenérgico α 1 , lo que sugiere una presencia glutaminérgica. mecanismo. [42] En ratas Sprague Dawley, la atomoxetina reduce el contenido de proteína NR2B sin alterar los niveles de transcripción. [43] La función aberrante del glutamato y del receptor de NMDA se ha relacionado con la etiología del TDAH . [44] [45]
La atomoxetina también inhibe de forma reversible las corrientes GIRK en los ovocitos de Xenopus de una manera dependiente de la concentración, independiente del voltaje e independiente del tiempo. [46] Los canales iónicos K ir 3.1 / 3.2 se abren aguas abajo de la estimulación M 2 , α 2 , D 2 y A 1 , así como otros receptores acoplados a G i . [46] Las concentraciones terapéuticas de atomoxetina están dentro del rango de interacción con GIRK, especialmente en metabolizadores lentos de CYP2D6. [46] No se sabe si esto contribuye a los efectos terapéuticos de la atomoxetina en el TDAH.
Se ha encontrado que la 4-hidroxiatomoxetina, el principal metabolito activo de la atomoxetina en los metabolizadores rápidos del CYP2D6, tiene una afinidad submicromolar por los receptores opioides , actuando como antagonista en los receptores opioides μ y como agonista parcial en los receptores opioides κ . [36] No se sabe si esta acción en el receptor opioide kappa conduce a efectos adversos relacionados con el SNC.
Farmacocinética [ editar ]
La atomoxetina administrada por vía oral se absorbe rápida y completamente. [5] El metabolismo de primer paso por el hígado depende de la actividad de CYP2D6 , lo que resulta en una biodisponibilidad absoluta del 63% para los metabolizadores rápidos y del 94% para los metabolizadores lentos . [5] La concentración plasmática máxima se alcanza en 1 a 2 horas. [5] Si se toma con alimentos, la concentración plasmática máxima disminuye entre un 10 y un 40% y retrasa la t max en 1 hora. [5] Los fármacos que afectan el pH gástrico no tienen ningún efecto sobre la biodisponibilidad oral. [15]
La atomoxetina tiene un volumen de distribución de 0,85 L / kg, con una distribución limitada en los glóbulos rojos. [5] Se une en gran medida a las proteínas plasmáticas (98,7%), principalmente a la albúmina, junto con la glucoproteína ácida α 1 (77%) y la IgG (15%). [5] [32] Su metabolito N -desmetilatomoxetina se une en un 99,1% a las proteínas plasmáticas, mientras que la 4-hidroxiatomoxetina solo se une en un 66,6%. [5]
La vida media de la atomoxetina varía ampliamente entre individuos, con un rango promedio de 4.5 a 19 horas. [5] [6] Dado que la atomoxetina es metabolizada por CYP2D6, la exposición puede aumentar 10 veces en los metabolizadores lentos de CYP2D6. [6]
La atomoxetina, N -desmetilatomoxetina y 4-hidroxiatomoxetina producen una inhibición mínima o nula de CYP1A2 y CYP2C9 , pero inhiben CYP2D6 en microsomas hepáticos humanos en concentraciones entre 3.6-17 μmol / L. [ cita requerida ] Las concentraciones plasmáticas de 4-hidroxiatomoxetina y N -desmetilatomoxetina en estado de equilibrio son 1.0% y 5% de la atomoxetina en metabolizadores rápidos CYP2D6, y son 5% y 45% de atomoxetina en metabolizadores lentos CYP2D6. [15]
La atomoxetina se excreta inalterada en la orina a <3% tanto en metabolizadores rápidos como lentos de CYP2D6, y> 96% y 80% de la dosis total se excreta en orina, respectivamente. [5] Las fracciones excretadas en la orina como 4-hidroxiatomoxetina y su glucurónido representan el 86% de una dosis dada en los metabolizadores rápidos, pero solo el 40% en los metabolizadores lentos. [5] Los metabolizadores lentos del CYP2D6 excretan mayores cantidades de metabolitos menores, a saber, N -desmetilatomoxetina y 2-hidroximetilatomoxetina y sus conjugados . [5]
Farmacogenómica [ editar ]
Se ha descubierto que los adultos chinos homocigotos para el alelo CYP2D6 * 10 hipoactivo exhiben AUC dos veces más altas y concentraciones plasmáticas máximas 1.5 veces más altas en comparación con los metabolizadores rápidos. [5]
De manera similar, se ha encontrado que los hombres japoneses homocigotos para CYP2D6 * 10 experimentan un AUC dos veces mayor en comparación con los metabolizadores rápidos. [5]
Química [ editar ]
La atomoxetina, o (-) - metil [(3 R ) -3- (2-metilfenoxi) -3-fenilpropilamina, es un polvo granular blanco que es muy soluble en agua.
Cápsula Strattera 60 mg dorso
Parte delantera de la cápsula Strattera de 60 mg con el logotipo de Lilly
Síntesis [ editar ]
Detección en fluidos biológicos [ editar ]
La atomoxetina puede cuantificarse en plasma, suero o sangre completa para distinguir los metabolizadores lentos de los que reciben el fármaco de forma terapéutica, para confirmar el diagnóstico en posibles víctimas de intoxicación o para ayudar en la investigación forense en caso de sobredosis mortal. [49]
Historia [ editar ]
La atomoxetina se fabrica, comercializa y vende en los Estados Unidos como la sal de clorhidrato (atomoxetina HCl) bajo la marca Strattera por Eli Lilly and Company , la compañía original que presentó la patente y actual propietario de la patente estadounidense. La atomoxetina estaba inicialmente destinada a ser desarrollada como un antidepresivo, pero se encontró que no era lo suficientemente eficaz para tratar la depresión. Sin embargo, se descubrió que era eficaz para el TDAH y fue aprobado por la FDA en 2002 para el tratamiento del TDAH. Su patente expiró en mayo de 2017. [50] El 12 de agosto de 2010, Lilly perdió una demanda que impugnaba su patente sobre Strattera, aumentando la probabilidad de una entrada más temprana de un genérico en el mercado estadounidense. [51]El 1 de septiembre de 2010, Sun Pharmaceuticals anunció que comenzaría a fabricar un genérico en los Estados Unidos. [52] Sin embargo, en una conferencia telefónica del 29 de julio de 2011, el presidente de Sun Pharmaceutical declaró que "Lilly ganó ese litigio en apelación, así que creo que [el Strattera genérico] está aplazado". [53]
En 2017, la FDA aprobó la producción genérica de atomoxetina por cuatro compañías farmacéuticas. [54]
Sociedad y cultura [ editar ]
Nombres de marca [ editar ]
En la India, la atomoxetina se vende bajo marcas comerciales que incluyen Axetra, Axepta, Attera, Tomoxetin y Attentin. En Australia, Portugal, Italia y Rumania, la atomoxetina se vende bajo la marca Strattera. En Irán, la atomoxetina se vende bajo marcas comerciales que incluyen Stramox. En 2017, se aprobó una versión genérica en Estados Unidos. [54]
Investigación [ editar ]
Se ha sugerido que la atomoxetina podría ser un complemento útil en personas con depresión mayor , particularmente en casos con TDAH concomitante. [55]
Referencias [ editar ]
- ^ "Uso de atomoxetina (Strattera) durante el embarazo" . Drugs.com . 22 de agosto de 2019 . Consultado el 7 de febrero de 2020 .
- ^ a b c d e f "atomoxetina (Rx) - Strattera" . Referencia de Medscape . WebMD. Archivado desde el original el 10 de noviembre de 2013 . Consultado el 10 de noviembre de 2013 .
- ^ a b c d e f g h i j k l m n o p q "Strattera (clorhidrato de atomoxetina)" . Servicios de comercio electrónico de TGA . Eli Lilly Australia Pty. Limited. 21 de agosto de 2013. Archivado desde el original el 6 de abril de 2017 . Consultado el 10 de noviembre de 2013 .
- ^ a b c d e f g "Cápsula de CLORHIDRATO DE ATOMOXETINA [Mylan Pharmaceuticals Inc.]" . DailyMed . Mylan Pharmaceuticals Inc. Octubre de 2011. Archivado desde el original el 10 de noviembre de 2013 . Consultado el 10 de noviembre de 2013 .
- ^ a b c d e f g h i j k l m n o p q r s Sauer JM, Ring BJ, Witcher JW (2005). "Farmacocinética clínica de la atomoxetina". Farmacocinética clínica . 44 (6): 571–90. doi : 10.2165 / 00003088-200544060-00002 . PMID 15910008 . S2CID 25708096 .
- ↑ a b c Brown JT, Bishop JR (2015). "Farmacogenética de la atomoxetina: asociaciones con farmacocinética, respuesta al tratamiento y tolerabilidad". Farmacogenómica . 16 (13): 1513-20. doi : 10.2217 / PGS.15.93 . PMID 26314574 .
- ^ a b c d e f g h i "Monografía de clorhidrato de atomoxetina para profesionales" . Drugs.com . Sociedad Estadounidense de Farmacéuticos del Sistema de Salud. Archivado desde el original el 4 de abril de 2019 . Consultado el 22 de marzo de 2019 .
- ^ a b Treuer T, Gau SS, Méndez L, Montgomery W, Monk JA, Altin M, et al. (Abril 2013). "Una revisión sistemática de la terapia combinada con estimulantes y atomoxetina para el trastorno por déficit de atención con hiperactividad, incluidas las características del paciente, las estrategias de tratamiento, la eficacia y la tolerabilidad" . Revista de psicofarmacología infantil y adolescente . 23 (3): 179–93. doi : 10.1089 / cap.2012.0093 . PMC 3696926 . PMID 23560600 .
- ^ "Guía de medicamentos para padres: TDAH" . Asociación Estadounidense de Psiquiatría (Directrices (fuente terciaria)). Asociación Estadounidense de Psiquiatría y Academia Estadounidense de Psiquiatría Infantil y Adolescente (AACAP). Junio de 2013. Archivado desde el original el 2 de febrero de 2017 . Consultado el 1 de enero de 2017 .
Aunque no está aprobado por la FDA para el tratamiento combinado, la atomoxetina (Strattera) a veces se usa junto con estimulantes como una terapia de combinación no aprobada.
- ^ "El Top 300 de 2021" . ClinCalc . Consultado el 18 de febrero de 2021 .
- ^ "Clorhidrato de atomoxetina - estadísticas de uso de fármacos" . ClinCalc . Consultado el 18 de febrero de 2021 .
- ^ a b Formulario nacional británico: BNF 76 (76 ed.). Prensa farmacéutica. 2018. págs. 344–345. ISBN 9780857113382.
- ^ a b "Advertencias de embarazo y lactancia de atomoxetina" . Drugs.com . Archivado desde el original el 22 de marzo de 2019 . Consultado el 3 de marzo de 2019 .
- ^ a b Ornoy A (febrero de 2018). "Tratamiento farmacológico del trastorno por déficit de atención con hiperactividad durante el embarazo y la lactancia". Investigación farmacéutica (revisión). 35 (3): 46. doi : 10.1007 / s11095-017-2323-z . PMID 29411149 . S2CID 3663423 .
- ^ a b c d "Cápsulas de Strattera (atomoxetina) para uso oral" . DailyMed.gov . Eli Lilly y compañía. 29 de enero de 2020. Archivado desde el original el 7 de junio de 2018 . Consultado el 26 de febrero de 2020 .
- ^ Ghuman JK, Hutchison SL (noviembre de 2014). "La atomoxetina es una opción de tratamiento con medicamentos de segunda línea para el TDAH" . Salud mental basada en evidencias . 17 (4): 108. doi : 10.1136 / eb-2014-101805 . PMID 25165169 . S2CID 34067825 . Archivado desde el original el 8 de marzo de 2016 . Consultado el 8 de marzo de 2016 .
- ^ Kooij, JJS (2013). Evaluación y tratamiento de diagnóstico de TDAH en adultos . Springer London. doi : 10.1007 / 978-1-4471-4138-9 . ISBN 978-1-4471-4137-2. S2CID 51698077 .
- ^ "NIMH» Trastorno por déficit de atención con hiperactividad " . NIMH »Inicio . Este artículo incorpora material de dominio público de sitios web o documentos del Instituto Nacional de Salud Mental . Archivado desde el original el 25 de diciembre de 2016 . Consultado el 21 de julio de 2018 .
 CS1 maint: others (link)
CS1 maint: others (link) - ^ "NIMH» Medicamentos para la salud mental " . NIMH »Inicio . Archivado desde el original el 6 de abril de 2019 . Consultado el 17 de mayo de 2019 .
- ^ Taylor D, Paton C, Shitij K (2012). Las pautas de prescripción de Maudsley en psiquiatría . West Sussex: Wiley-Blackwell. ISBN 978-0-470-97948-8.
- ^ Perugi G, Vannucchi G (2015). "El uso de estimulantes y atomoxetina en adultos con TDAH comórbido y trastorno bipolar". Opinión de expertos sobre farmacoterapia . 16 (14): 2193-204. doi : 10.1517 / 14656566.2015.1079620 . PMID 26364896 . S2CID 28907560 .
- ^ Siegel M, Erickson C, Frazier JA, Ferguson T, Goepfert E, Joshi G, Humberd QM, King BH, Lutz A, Kraus L, Mao A, Robb A, Veenstra-VanderWeele J, Wang P, Head CJ, et al. . (Sociedad de Autismo de América) (2016). Guía de medicamentos para padres con trastornos del espectro autista (PDF) . Washington, DC: Academia Estadounidense de Psiquiatría Infantil y Adolescente. pag. 13. Archivado (PDF) desde el original el 11 de abril de 2017. La
atomoxetina (Strattera) también se ha investigado en estudios controlados para el tratamiento del TDAH en niños con autismo y mostró algunas mejoras, en particular para la hiperactividad y la impulsividad.
- ^ Solmi M, Fornaro M, Ostinelli EG, Zangani C, Croatiato G, Monaco F, et al. (Junio de 2020). "Seguridad de 80 antidepresivos, antipsicóticos, medicamentos contra el déficit de atención / hiperactividad y estabilizadores del estado de ánimo en niños y adolescentes con trastornos psiquiátricos: una meta-revisión sistemática a gran escala de 78 efectos adversos" . Psiquiatría mundial (metaanálisis). 19 (2): 214-232. doi : 10.1002 / wps.20765 . PMC 7215080 . PMID 32394557 .
- ^ "Atomoxetina y tendencias suicidas en niños y adolescentes" . Recetador australiano . 36 (5). Octubre de 2013. p. 166. Archivado desde el original el 10 de noviembre de 2013 . Consultado el 10 de noviembre de 2013 .
- ^ "Cápsulas duras de Strattera 10 mg, 18 mg, 25 mg, 40 mg, 60 mg, 80 mg o 100 mg" . Compendio electrónico de medicamentos . 28 de mayo de 2013. Archivado desde el original el 10 de noviembre de 2013 . Consultado el 10 de noviembre de 2013 .
- ^ "Inserto del producto Strattera" . Consultado el 8 de diciembre de 2013 .
- ^ "Guía de medicación de Strattera" (PDF) . EE.UU. Administración de Drogas y Alimentos (FDA) . Eli Lilly y compañía . 2003. Archivado desde el original (PDF) el 10 de diciembre de 2013 . Consultado el 17 de diciembre de 2013 .
- ^ Todor I, Popa A, Neag M, Muntean D, Bocsan C, Buzoianu A, et al. (Abril-junio de 2016). "Evaluación de una interacción fármaco-fármaco mediada por el metabolismo potencial entre atomoxetina y bupropión en voluntarios sanos" . Revista de Farmacia y Ciencias Farmacéuticas . 19 (2): 198-207. doi : 10.18433 / j3h03r . PMID 27518170 .
- ↑ a b c Kasi PM, Mounzer R, Gleeson GH (2011). "Efectos secundarios cardiovasculares de la atomoxetina y sus interacciones con inhibidores del sistema del citocromo p450" . Informes de casos en medicina . 2011 : 952584. doi : 10.1155 / 2011/952584 . PMC 3135225 . PMID 21765848 .
- ^ Belle DJ, Ernest CS, Sauer JM, Smith BP, Thomasson HR, Witcher JW (noviembre de 2002). "Efecto de la potente inhibición de CYP2D6 por paroxetina sobre la farmacocinética de atomoxetina". Revista de farmacología clínica . 42 (11): 1219–27. doi : 10.1177 / 009127002762491307 . PMID 12412820 . S2CID 40283275 .
- ^ Scherer D, Hassel D, Bloehs R, Zitron E, von Löwenstern K, Seyler C, et al. (Enero de 2009). "Atomoxetina inhibidor selectivo de la recaptación de noradrenalina bloquea directamente las corrientes de hERG" . Revista británica de farmacología . 156 (2): 226–36. doi : 10.1111 / j.1476-5381.2008.00018.x . PMC 2697834 . PMID 19154426 .
- ^ a b c "21-411 Strattera Clinical Pharmacology Biofarmaceutics Review Part 2" (PDF) . EE.UU. Administración de Drogas y Alimentos (FDA) . Archivado (PDF) desde el original el 1 de marzo de 2017 . Consultado el 6 de agosto de 2017 .
- ^ Roth BL, Driscol J. "Base de datos PDSP K i " . Programa de detección de drogas psicoactivas (PDSP) . Universidad de Carolina del Norte en Chapel Hill y el Instituto Nacional de Salud Mental de los Estados Unidos . Consultado el 14 de agosto de 2017 .
- ^ Upadhyaya HP, Desaiah D, Schuh KJ, Bymaster FP, Kallman MJ, Clarke DO, et al. (Marzo de 2013). "Una revisión de la evaluación del potencial de abuso de atomoxetina: un medicamento no estimulante para el trastorno por déficit de atención con hiperactividad" . Psicofarmacología . Springer Nature. 226 (2): 189-200. doi : 10.1007 / s00213-013-2986-z . PMC 3579642 . PMID 23397050 .
- ^ a b c Bymaster FP, Katner JS, Nelson DL, Hemrick-Luecke SK, Threlkeld PG, Heiligenstein JH, et al. (Noviembre de 2002). "La atomoxetina aumenta los niveles extracelulares de norepinefrina y dopamina en la corteza prefrontal de la rata: un mecanismo potencial de eficacia en el trastorno por déficit de atención / hiperactividad" . Neuropsicofarmacología . 27 (5): 699–711. doi : 10.1016 / S0893-133X (02) 00346-9 . PMID 12431845 .
- ↑ a b Creighton CJ, Ramabadran K, Ciccone PE, Liu J, Orsini MJ, Reitz AB (agosto de 2004). "Síntesis y evaluación biológica del principal metabolito de la atomoxetina: elucidación de un efecto agonista kappa-opioide parcial". Cartas de Química Bioorgánica y Medicinal . 14 (15): 4083–5. doi : 10.1016 / j.bmcl.2004.05.018 . PMID 15225731 .
- ^ a b Koda K, Ago Y, Cong Y, Kita Y, Takuma K, Matsuda T (julio de 2010). "Efectos de la administración aguda y crónica de atomoxetina y metilfenidato sobre los niveles extracelulares de noradrenalina, dopamina y serotonina en la corteza prefrontal y el cuerpo estriado de ratones" . Revista de neuroquímica . 114 (1): 259–70. doi : 10.1111 / j.1471-4159.2010.06750.x . PMID 20403082 .
- ^ Ding YS, Naganawa M, Gallezot JD, Nabulsi N, Lin SF, Ropchan J, et al. (Febrero 2014). "Las dosis clínicas de atomoxetina ocupan significativamente los transportes de norepinefrina y serotonina: implicaciones en el tratamiento de la depresión y el TDAH". NeuroImage . 86 : 164–71. doi : 10.1016 / j.neuroimage.2013.08.001 . PMID 23933039 . S2CID 16958660 .
La acción noradrenérgica también ejerce un efecto clínico importante en diferentes clases de antidepresivos como la desipramina y nortriptilina (tricíclicos, efecto noradrenérgico prevalente), reboxetina y atomoxetina (inhibidor de la recaptación de noradrenérgicos relativamente puros (NRI)), y antidepresivos de doble acción como la serotonina reotonina. inhibidores (IRSN), el inhibidor de la recaptación noradrenérgica y dopaminérgica (NDRI) bupropión y otros compuestos (p. ej., mianserina, mirtazapina), que mejoran la transmisión noradrenérgica
- ^ Zerbe RL, Rowe H, Enas GG, Wong D, Farid N, Lemberger L (enero de 1985). "Farmacología clínica de la tomoxetina, un potencial antidepresivo". La Revista de Farmacología y Terapéutica Experimental . 232 (1): 139–43. PMID 3965689 .
- ^ a b Ludolph AG, Udvardi PT, Schaz U, Henes C, Adolph O, Weigt HU, et al. (Mayo de 2010). "La atomoxetina actúa como bloqueador del receptor NMDA en concentraciones clínicamente relevantes" . Revista británica de farmacología . 160 (2): 283–91. doi : 10.1111 / j.1476-5381.2010.00707.x . PMC 2874851 . PMID 20423340 .
- ↑ a b Barygin OI, Nagaeva EI, Tikhonov DB, Belinskaya DA, Vanchakova NP, Shestakova NN (abril de 2017). "Inhibición de los canales del receptor NMDA y AMPA por antidepresivos y antipsicóticos". Investigación del cerebro . 1660 : 58–66. doi : 10.1016 / j.brainres.2017.01.028 . PMID 28167075 . S2CID 27647092 .
- ^ Di Miceli M, Gronier B (junio de 2015). "Los psicoestimulantes y la atomoxetina alteran la actividad electrofisiológica de las neuronas de la corteza prefrontal, interacción con los receptores NMDA de catecolaminas y glutamato". Psicofarmacología . 232 (12): 2191-205. doi : 10.1007 / s00213-014-3849-y . PMID 25572531 . S2CID 18339166 .
- ^ Udvardi PT, Föhr KJ, Henes C, Liebau S, Dreyhaupt J, Boeckers TM, Ludolph AG (2013). "La atomoxetina afecta la transcripción / traducción del receptor NMDA y el transportador de norepinefrina en el cerebro de rata - un estudio in vivo" . Diseño, desarrollo y terapia de fármacos . 7 : 1433–46. doi : 10.2147 / DDDT.S50448 . PMC 3857115 . PMID 24348020 .
- ^ Maltezos S, Horder J, Coghlan S, Skirrow C, O'Gorman R, Lavender TJ, et al. (Marzo del 2014). "Glutamato / glutamina e integridad neuronal en adultos con TDAH: un estudio de protón MRS" . Psiquiatría traslacional . 4 (3): e373. doi : 10.1038 / tp.2014.11 . PMC 3966039 . PMID 24643164 .
- ↑ Chang JP, Lane HY, Tsai GE (2014). "Trastorno por déficit de atención con hiperactividad y desregulación de N-metil-D-aspartato (NMDA)". Diseño Farmacéutico Actual . 20 (32): 5180–5. doi : 10.2174 / 1381612819666140110115227 . PMID 24410567 .
- ↑ a b c Kobayashi T, Washiyama K, Ikeda K (junio de 2010). "Inhibición de los canales de K + rectificadores internos activados por proteína G por los inhibidores selectivos de la recaptación de norepinefrina atomoxetina y reboxetina" . Neuropsicofarmacología . 35 (7): 1560–9. doi : 10.1038 / npp.2010.27 . PMC 3055469 . PMID 20393461 .
- ^ Una patente estadounidense 4018895 A , Bryan B. Molloy y Klaus K. Schmiegel, "Ariloxifenilpropilaminas en el tratamiento de la depresión", publicada el 19 de abril de 1977, asignada a Eli Lilly And Company
- ^ B1 Patente estadounidense EP0052492 B1 , Bennie Joe Foster & Edward Ralph Lavagnino, "3-aryloxy-3-phenylpropylamines", publicada el 29 de febrero de 1984, asignada a Eli Lilly And Company
- ^ Baselt RC (2008). Disposición de sustancias químicas y drogas tóxicas en el hombre (8ª ed.). Foster City, CA: Publicaciones biomédicas. págs. 118-20 . ISBN 978-0-931890-08-6.
- ^ "Resultados de búsqueda de patentes y exclusividad" . Libro naranja electrónico . EE.UU. Administración de Drogas y Alimentos (FDA). Archivado desde el original el 22 de marzo de 2012 . Consultado el 26 de abril de 2009 .
- ^ "El farmacéutico Eli Lilly pierde caso de patente sobre medicamento para el TDAH, reduce la perspectiva de ingresos" . Chicago Tribune .[ enlace muerto permanente ]
- ^ "Sun Pharma recibe la aprobación de la USFDA para cápsulas genéricas de Strattera" . Tiempos de negocios internacionales . Archivado desde el original el 7 de abril de 2011.
- ^ "Transcripción de la llamada de ganancias de Sun Pharma Q1 2011-12 10.00 am, 29 de julio de 2011" (PDF) . Archivado desde el original (PDF) el 29 de septiembre de 2011.
- ^ a b "La FDA aprueba el primer Strattera genérico para el tratamiento del TDAH" . EE.UU. Administración de Drogas y Alimentos (FDA) (Nota de prensa). 30 de mayo de 2017. Archivado desde el original el 4 de junio de 2017 . Consultado el 1 de enero de 2018 .
- ^ Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). Neurofarmacología molecular: una base para la neurociencia clínica (3ª ed.). Nueva York: McGraw-Hill Medical. ISBN 9780071827706.
Lectura adicional [ editar ]
- Dean L (2015). "Terapia de atomoxetina y genotipo CYP2D6" . En Pratt VM, McLeod HL, Rubinstein WS, et al. (eds.). Resúmenes de genética médica . Centro Nacional de Información Biotecnológica (NCBI). PMID 28520366 . ID de estantería: NBK315951.
Enlaces externos [ editar ]
- "Atomoxetina" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
- "Strattera (Atomoxetine) - Estudios publicados" . Druglib .