 | |
 | |
| Nombres | |
|---|---|
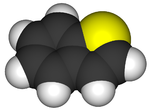
| Nombre IUPAC preferido 1-benzotiofeno | |
| Otros nombres Benzo [ b ] tiofeno tianafteno benzotiofurano | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA | 100.002.178 |
| Número CE |
|
PubChem CID |
|
| Número RTECS |
|
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 8 H 6 S | |
| Masa molar | 134,20 g · mol −1 |
| Apariencia | Blanco sólido |
| Densidad | 1,15 g / cm 3 |
| Punto de fusion | 32 ° C (90 ° F; 305 K) |
| Punto de ebullición | 221 ° C (430 ° F; 494 K) |
| Riesgos | |
| Pictogramas GHS |   |
| Palabra de señal GHS | Advertencia |
| H302 , H411 | |
| P264 , P270 , P273 , P301 + 312 , P330 , P391 , P501 | |
| punto de inflamabilidad | 110 ° C (230 ° F; 383 K) |
| Compuestos relacionados | |
Compuestos relacionados | Tiofeno , indeno , benzofurano , indol |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El benzotiofeno es un compuesto orgánico aromático con una fórmula molecular C 8 H 6 S y un olor similar al naftaleno (bolas de naftalina). Se produce de forma natural como componente de depósitos relacionados con el petróleo, como el alquitrán de lignito . El benzotiofeno no tiene uso doméstico. Además del benzo [b] tiofeno, se conoce un segundo isómero: benzo [c] tiofeno . [3]
El benzotiofeno se utiliza en la investigación como material de partida para la síntesis de estructuras más grandes, generalmente bioactivas. Se encuentra dentro de las estructuras químicas de fármacos como raloxifeno , zileutón y sertaconazol , y también BTCP . También se utiliza en la fabricación de tintes como el tioíndigo .
Síntesis
La mayoría de las síntesis de benzotiofeno crean benzotiofenos sustituidos como precursor de reacciones posteriores. Un ejemplo es la reacción de un 2-bromobenceno sustituido con alquino con sulfuro de sodio o sulfuro de potasio para formar benzotiofeno con una sustitución de alquilo en la posición 2. [4]

La tiourea se puede utilizar como reactivo en lugar de sulfuro de sodio o sulfuro de potasio. [5]

En presencia de un catalizador de oro, se puede sintetizar un benzotiofeno 2,3-disustituido más complejo. [6]

Referencias
- ^ Índice de Merck , 11ª edición, 9232
- ^ "Thianaphthene" . www.sigmaaldrich.com . Sigma Aldrich . Consultado el 12 de noviembre de 2020 .
- ^ Cava, Michael P .; Lakshmikantham, MV (1975). "Tiofenos condensados no clásicos". Cuentas de Investigación Química . 8 (4): 139–44. doi : 10.1021 / ar50088a005 .CS1 maint: uses authors parameter (link)
- ^ Sol, Lei-Lei; Deng, Chen-Liang; Tang, Ri-Yuan; Zhang, Xing-Guo (16 de septiembre de 2011). "Anulación catalizada por CuI / TMEDA de 2-bromo alquinilbencenos con Na2S: síntesis de benzo [b] tiofenos". La Revista de Química Orgánica . Sociedad Química Estadounidense (ACS). 76 (18): 7546–7550. doi : 10.1021 / jo201081v . ISSN 0022-3263 . PMID 21812478 .
- ^ Kuhn, Marius; Falk, Florian C .; Paradies, enero (5 de agosto de 2011). "Acoplamiento C-S catalizado por paladio: acceso a tioéteres, benzo [b] tiofenos y tieno [3,2-b] tiofenos". Letras orgánicas . Sociedad Química Estadounidense (ACS). 13 (15): 4100–4103. doi : 10.1021 / ol2016093 . ISSN 1523-7060 . PMID 21732682 .
- ^ Nakamura, Itaru; Sato, Takuma; Yamamoto, Yoshinori (3 de julio de 2006). "Carbotiolación intramolecular catalizada por oro de alquinos: síntesis de benzotiofenos 2,3-disustituidos a partir de (α-alcoxi alquil) (orto-alquinil fenil) sulfuros". Angewandte Chemie International Edition . Wiley. 45 (27): 4473–4475. doi : 10.1002 / anie.200601178 . ISSN 1433-7851 . PMID 16767784 .