N , N- diisopropiletilamina
 | |||
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido N- Etil- N - (propan-2-il) propan-2-amina | |||
Otros nombres
| |||
| Identificadores | |||
Modelo 3D ( JSmol ) | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.027.629 | ||
| Número CE |
| ||
| Malla | N, N-diisopropiletilamina | ||
PubChem CID | |||
| UNII | |||
| un numero | 2733 | ||
Tablero CompTox ( EPA ) | |||
| |||
| |||
| Propiedades | |||
| C 8 H 19 N | |||
| Masa molar | 129,247 g · mol −1 | ||
| Apariencia | Líquido incoloro | ||
| Olor | Pescado, amoniacal | ||
| Densidad | 0,742 g mL −1 | ||
| Punto de fusion | −50 a −46 ° C (−58 a −51 ° F; 223 a 227 K) | ||
| Punto de ebullición | 126,6 ° C; 259,8 ° F; 399,7 K | ||
| 4.01 g / L (a 20 ° C) | |||
| Presión de vapor | 4,1 kPa (a 37,70 ° C) | ||
Índice de refracción ( n D ) | 1.414 | ||
| Riesgos | |||
| Pictogramas GHS |    | ||
| Palabra de señal GHS | Peligro | ||
| H225 , H301 , H314 , H412 | |||
| P210 , P273 , P280 , P301 + 310 , P305 + 351 + 338 , P310 | |||
| punto de inflamabilidad | 10 ° C (50 ° F; 283 K) | ||
| Límites explosivos | 0,7–6,3% | ||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis media ) | 200-500 mg kg -1 (oral, rata) | ||
| Compuestos relacionados | |||
Aminas relacionadas |
| ||
Compuestos relacionados |
| ||
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |||
| Referencias de Infobox | |||
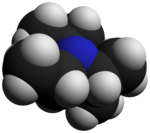
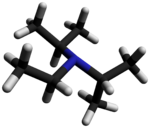
La N , N- diisopropiletilamina , o base de Hünig , es un compuesto orgánico y una amina . Lleva el nombre del químico alemán Siegfried Hünig. Se utiliza en química orgánica como base . Suele abreviarse como DIPEA, DIEA o i -Pr 2 NEt .
Estructura
DIPEA consta de un nitrógeno central que está unido a un grupo etilo y dos grupos isopropilo . Un solo par de electrones reside en el átomo de nitrógeno, que puede reaccionar con electrófilos. Sin embargo, como los dos grupos isopropilo y el grupo etilo ocupan gran parte del espacio que rodea al nitrógeno, solo pequeños electrófilos , como los protones, pueden reaccionar con el par único de nitrógeno.
Aparición y preparación
DIPEA está disponible comercialmente. Se prepara tradicionalmente mediante la alquilación de diisopropilamina con sulfato de dietilo . [1]
Pure DIPEA existe como un líquido incoloro, aunque las muestras comerciales pueden ser ligeramente amarillas. Si es necesario, el compuesto se puede purificar mediante destilación a partir de hidróxido de potasio [2] o hidruro de calcio . [3]
Usos y reacciones
DIPEA es una base orgánica estéricamente impedida que se emplea comúnmente como eliminador de protones. Así, como la 2,2,6,6-tetrametilpiperidina y la trietilamina , DIPEA es una buena base pero un nucleófilo pobre , una combinación de propiedades que lo convierte en un reactivo orgánico útil. [4]
Acoplamiento de amida
Se utiliza comúnmente como base impedida en reacciones de acoplamiento de amidas entre un ácido carboxílico (normalmente activado, por ejemplo, como un cloruro de ácido, como se ilustra a continuación) y una amina nucleófila. [5] Como DIPEA está impedido y es pobremente nucleofílico, no compite con la amina nucleofílica en la reacción de acoplamiento.
Alquilaciones
DIPEA se ha investigado para su uso como un reactivo selectivo en la alquilación de aminas secundarias a aminas terciarias por haluros de alquilo . Esto a menudo se ve obstaculizado por una reacción de Menshutkin no deseada que forma una sal de amonio cuaternario , pero está ausente cuando DIPEA está presente. [6]
Reacciones de acoplamiento cruzado catalizadas por metales de transición
DIPEA se puede utilizar como base en una serie de reacciones de acoplamiento cruzado catalizadas por metales de transición , como el acoplamiento de Heck y el acoplamiento de Sonogashira (como se ilustra a continuación). [7]
Oxidación de Swern
Aunque la trietilamina se emplea tradicionalmente como base impedida en las oxidaciones de Swern , en su lugar se puede utilizar la DIPEA estructuralmente similar, como se ejemplifica a continuación. [8]
Ejemplos de DIPEA utilizados como sustrato
DIPEA forma un compuesto heterocíclico complejo llamado escorpionina (bis ([1,2] ditiolo) - [1,4] tiazina) al reaccionar con dicloruro de disulfuro que es catalizado por DABCO en una síntesis en un solo recipiente . [9]
Comparación con trietilamina
DIPEA y trietilamina son estructuralmente muy similares, y ambos compuestos se consideran bases orgánicas impedidas. Debido a su similitud estructural, DIPEA y trietilamina se pueden usar indistintamente en la mayoría de las aplicaciones. El átomo de nitrógeno en DIPEA está más protegido que el átomo de nitrógeno en trietilamina. Sin embargo, la trietilamina es una base ligeramente más fuerte que DIPEA; los pK a s de los respectivos ácidos conjugados en dimetilsulfóxido son 9,0 y 8,5, respectivamente. [10]
Referencias
- ^ Hünig, S .; Kiessel, M. (1958). "Spezifische Protonenacceptoren als Hilfsbasen bei Alkylierungs- und Dehydrohalogenierungsreaktionen". Chemische Berichte . 91 (2): 380–392. doi : 10.1002 / cber.19580910223 .
- ↑ Armarego, WLF (17 de octubre de 2012). Purificación de productos químicos de laboratorio . Chai, Christina Li Lin (Séptima ed.). Amsterdam. ISBN 9780123821621. OCLC 820853648 .
- ^ Keiper, Sonja; Vyle, Joseph S. (12 de mayo de 2006). "Fotocontrol reversible de escisión de ARN catalizada por desoxirribozima en condiciones de rotación múltiple" . Angewandte Chemie International Edition . 45 (20): 3306–3309. doi : 10.1002 / anie.200600164 . ISSN 1433-7851 . PMID 16619331 .
- ^ Sorgi, KL (2001). "Diisopropiletilamina". Enciclopedia de reactivos para síntesis orgánica . doi : 10.1002 / 047084289X.rd254 . ISBN 978-0471936237.
- ^ Dunetz, Joshua R .; Magano, Javier; Weisenburger, Gerald A. (5 de febrero de 2016). "Aplicaciones a gran escala de reactivos de acoplamiento de amida para la síntesis de productos farmacéuticos". Investigación y desarrollo de procesos orgánicos . 20 (2): 140-177. doi : 10.1021 / op500305s . ISSN 1083-6160 .
- ^ Moore, JL; Taylor, SM; Soloshonok, VA (2005). "Una síntesis general eficaz y operativamente conveniente de aminas terciarias por alquilación directa de aminas secundarias con haluros de alquilo en presencia de la base de Huenig" . Arkivoc . 2005 (parte vi): 287–292. doi : 10.3998 / ark.5550190.0006.624 . EJ-1549C. Archivado desde el original el 4 de marzo de 2008 . Consultado el 16 de junio de 2006 .
- ^ Chinchilla, Rafael; Nájera, Carmen (2011). "Avances recientes en las reacciones de Sonogashira" . Reseñas de la Sociedad Química . 40 (10): 5084–5121. doi : 10.1039 / c1cs15071e . ISSN 0306-0012 . PMID 21655588 .
- ^ Walba, David M .; Thurmes, William N .; Haltiwanger, R. Curtis (1988). "Una ruta altamente estereocontrolada para el sistema de anillo espirocetal de monensina". La Revista de Química Orgánica . 53 (5): 1046–1056. doi : 10.1021 / jo00240a022 . ISSN 0022-3263 .
- ^ Rees, W .; Marcos, CF; Polo, C .; Torroba, T .; Rakitin OA (1997). "Desde la base de Hünig a Bis ([1,2] dithiolo) - [1,4] tiazinas en una olla: la ruta rápida a heterociclos altamente sulfurados". Angewandte Chemie International Edition . 36 (3): 281-283. doi : 10.1002 / anie.199702811 .
- ↑ Lepore, Salvatore D .; Khoram, Anita; Bromfield, Deborah C .; Cohn, Pamela; Jairaj, Vinod; Silvestri, Maximilian A. (2005). "Estudios sobre la isomerización mediada por manganeso de alquinil carbonilos a allenil carbonilos". La Revista de Química Orgánica . 70 (18): 7443–7446. doi : 10.1021 / jo051040u . ISSN 0022-3263 . PMID 16122274 .
- Alquilaminas
- Bases (química)
- Reactivos para química orgánica
- Bases no nucleofílicas
- Compuestos de diisopropilamino
- Aminas terciarias